Introdução: A fluoresceína intratecal tem sido efetiva no diagnóstico topográfico da rinoliquorréia. Entretanto, não há estudos no líquor após o uso de fluoresceína intratecal.
Objetivo: Estudo prospectivo visando avaliar o líquor, através de análise química e citológica, após injeção de fluoresceína.
Método: Análise prospectiva de 24 punções após injeção intratecal de fluoresceína para diagnóstico topográfico de fístula liquórica, coletado no momento da punção, 24 e 48 horas, divididos pela celularidade: grupo 1, com até 5 células e grupo 2 com mais de 5 células.
Resultado: A coloração amarelo-esverdeada do líquor permaneceu após 48 horas em 36%, evidenciando permanência de fluoresceína. Observou-se ausência de mudanças no nível de proteína e glicose entre 0-24 horas e 0-48 horas. No grupo 2, um aumento na contagem celular foi observado entre 24 e 48 horas (p = 0,019). No dois grupos juntos, observou-se um aumento de neutrófilos entre 0 e 48 horas (p = 0,048) e uma diminuição entre 24 e 28 horas (p = 0,05).
Conclusão: Fluoresceína intratecal provocou discretas reações meníngeas, como o aumento de células entre 24 e 48 horas e aumento dos neutrófilos em 24 horas com uma subsequente diminuição em 48 horas sem correlação com sintomas.
Introduction: Intrathecal fluorescein has been effective for topographic diagnosis of rhinoliquorrhea. Nonetheless, there are no reports on the study of cerebral spinal fluid (CSF) after use of intrathecal fluorescein.
Objective: A prospective study attempting to evaluate CSF through chemical and cytological analysis, after injection of fluorescein.
Methods: Prospective analysis of 24 samples of CSF after intrathecal injection of fluorescein for topographic diagnosis of CSF fistulae, collected at the time of puncture and after 24 and 48 h, divided by cellularity: Group 1, up to five cells, and Group 2, with more than five cells.
Results: The yellow-greenish color of CSF remained after 48 h in 36%, evidencing permanence of fluorescein. No changes in protein and glucose levels were observed between 0-24 h and 0- 48 h. In group 2, an increase in cell count was observed between 24 h and 48 h (p = 0.019). In both groups, there was an increase of neutrophils between 0 and 48 h (p = 0.048) and a decrease between 24 and 48 h (p = 0.05).
Conclusion: Intrathecal fluorescein provoked discreet meningeal reactions, such as an increase of cells between 24 and 48 h and an increase of neutrophils at 24 h, with a subsequent decrease at 48 h with no correlation with symptomatology.
Introdução
A fístula do líquido cefalorraquidiano (LCR) pode ocorrer a partir do nariz, do canal auditivo externo e de um defeito traumático ou operatório na base do crânio ou coluna vertebral. O vazamento de fluido é resultado de laceração dural e aracnoidal com formação de fístula. A rinoliquorreia (RLR) é classicamente definida como a presença de LCR na cavidade nasal, o que implica na existência de um defeito ósseo e dural comunicando o espaço subaracnoide com as cavidades das vias aéreas superiores.1 Estas situações exigem um diagnóstico preciso da etiologia e localização,2,3 em conjunto com um tratamento adequado, devido aos riscos aumentados de complicações neurológicas, principalmente meningites bacterianas.
Embora tenha havido vários avanços nos exames pré-operatórios e exames para diagnosticar uma RLR, o uso de fluoresceína, iniciado na década de 1960, tem-se revelado eficaz na detecção de locais da fístula liquórica.4-9
No entanto, existem poucos relatos de reações adversas, principalmente relacionadas com alta concentração de fluoresceína, e alguns centros ainda hesitam em usá-la no dia a dia.10-18 Em 2001, uma solução de fluoresceína foi descrita, a fim de facilitar e acelerar a identificação de locais de fístulas.19 Há trabalhos anteriores que descrevem o uso e a segurança da solução de fluoresceína intratecal hipodensa, mas eles raramente avaliam as mudanças que o seu uso induz no LCR.
O objetivo deste estudo foi determinar as alterações do LCR após o uso de solução hipodensa de fluoresceína. Foram avaliadas as mudanças na coloração, a celularidade, a dosagem de glicose e as proteínas no LCR de pacientes submetidos à sua utilização.
Método
Este é um estudo prospectivo de 24 pacientes consecutivos, com idade entre três e 54 anos (média 31 anos), submetidos à injeção intratecal de solução hipodensa de fluoresceína para o diagnóstico endoscópico intraoperatório de fístulas liquóricas da base anterior do crânio.
Todos os pacientes forneceram consentimento informado após uma discussão dos riscos, benefícios e alternativas. O estudo foi aprovado pelo comitê de ética da instituição sob o número Etic 075/00.
Treze pacientes eram do sexo masculino (54%) e 11 do sexo feminino (46%). A etiologia principal da RLR foi traumática em 14 pacientes (58%), espontânea em cinco (21%), e meningocele ou meningoencefalocele em cinco (21%). O critério de exclusão foi a ocorrência de meningite prévia num período de três meses. Não houve pacientes excluídos no estudo.
Todos os pacientes foram submetidos à punção lombar, sob anestesia geral, no início da cirurgia. Foi coletado LCR, neste momento, para análise química e citológica.
Após a coleta do LCR, se o paciente tinha mais do que 50 kg, 0,5 mL de uma solução a 5% de fluoresceína diluída com 10 mL de água destilada era injetada. Se o paciente tinha menos de 50 kg, ou em crianças, foi utilizado 0,1 mL / kg da solução descrita.19 Usamos o Fluidag® (fluoresceína de sódio, bicarbonato de sódio e nitrato de phenylmercuric), de Oftalmopharma, São Paulo, Brasil. Fludiag® é constituído por fluoresceína de sódio na concentração de 5% dissolvido em um tampão fisiologicamente compatível, contendo bicarbonato de sódio como um alcalinizante, a fim de manter o pH no intervalo de 8,0 a 9,8, nitrato fenilmercúrico em 0,0001% como conservante e água para injetáveis .
Logo após a injeção, que é realizada lentamente, durando dois ou três minutos, o paciente era posicionado em decúbito dorsal, com o dorso ligeiramente elevado em cerca de 30 graus, a cirurgia era iniciada.
Após a cirurgia, com o fechamento endoscópico da fístula do LCR, o cateter de drenagem lombar inserido para a injeção de fluoresceína foi mantido fechado. Amostras de LCR foram coletadas em 24 e 48 horas após o procedimento. Estas amostras foram submetidas à análise química e citológica.
A análise química do LCR constou de: cor (verde, amarelo -esverdeado ou límpido), dosagem de glicose e de proteína pelo método colorimétrico.
Na análise citológica utilizou-se o número total de eritrócitos e de células nucleadas (neutrófilos, linfócitos, monócitos, eosinófilos e basófilos). Foi utilizada a análise por citometria com a câmara de Neubauer.
Os pacientes foram divididos em dois grupos, de acordo com seu número inicial de células no LCR: grupo 1 (até cinco células por mL) e grupo 2 (mais de cinco células por mL). Estes grupos foram comparados, a fim de analisar a diferença entre os níveis de glicose, proteínas e celularidade.
No desenho do estudo não houve a formação de grupo controle, sem aplicação de fluoresceína.
Todos os resultados foram analisados estatisticamente por meio do coeficiente de Pearson, com significância estatística de 95% (p < 0,05).
Resultados
Em todos os casos, a fluoresceína hipodensa no campo cirúrgico endoscópico foi detectada, e a fístula de LCR fechada com sucesso. Não houve necessidade de utilização de filtros especiais de luz. Não foram observadas complicações, reações adversas ou meningites nos 24 pacientes. O grupo 1 contou com 14 pacientes, e o grupo 2, dez pacientes.
Coloração: O LCR colhido antes da injeção de fluoresceína foi límpido em todos os pacientes. Em 24 horas, a cor era predominantemente amarelo-esverdeado em 20 pacientes (80%), indicando a presença de fluoresceína. Em 48 horas, o LCR ainda estava amarelo-esverdeado em nove pacientes (36%).
Glicose: Os níveis de glicose não apresentaram diferença estatisticamente significativa entre os dois grupos analisados em conjunto, em 0 h (p = 0,5), 24h (p = 0,24) ou 48 h (p = 0,5).
Proteínas: Não houve diferença estatisticamente significativa em relação à dosagem de proteína entre os dois grupos analisados em conjunto, em 0h (p = 0,37) e 24 h (p = 0,16). Em 48h foi observada diferença estatisticamente significativa, com uma elevação dos níveis de proteína no grupo 1 (p = 0,032).
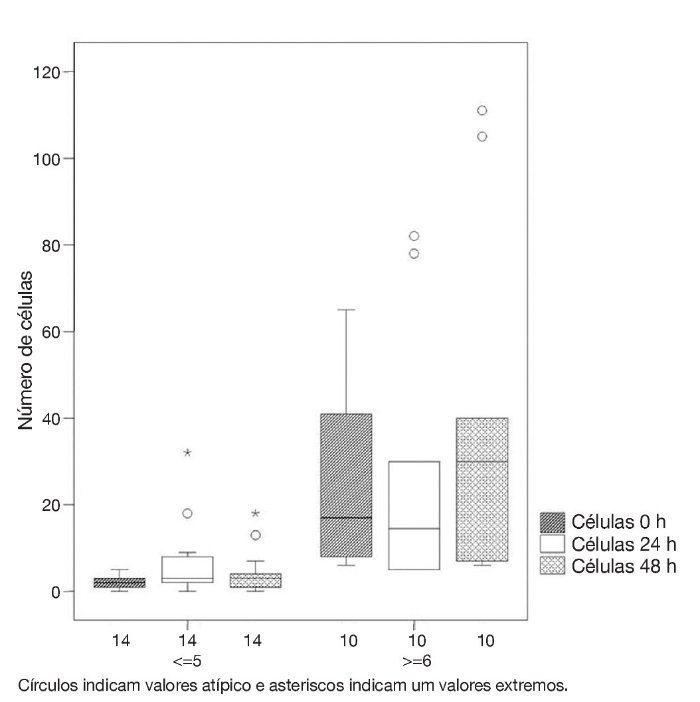
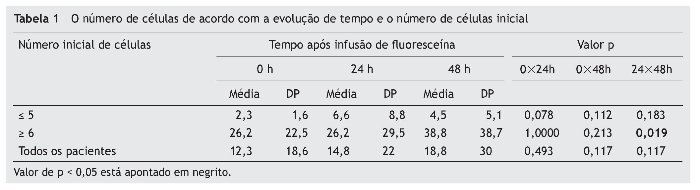
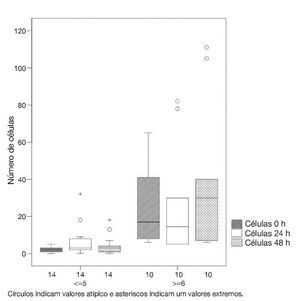
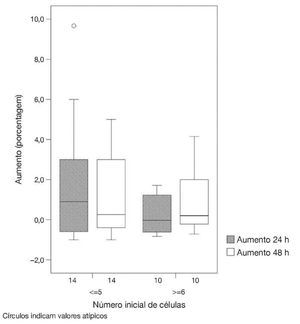
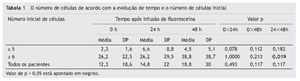
Número de células: Um aumento da contagem de células foi também observado. No grupo 1, quase todos os pacientes apresentaram um aumento de 600%, quando comparados os valores iniciais de células. Metade dos pacientes apresentou um aumento da contagem de células superior a 100% em ambos os grupos (figs. 1 e 2, tabela 1).
Figura 1 Celularidade em ambos os grupos (1 e 2), em relação aos tempos: 0h, 24 h e 48h.
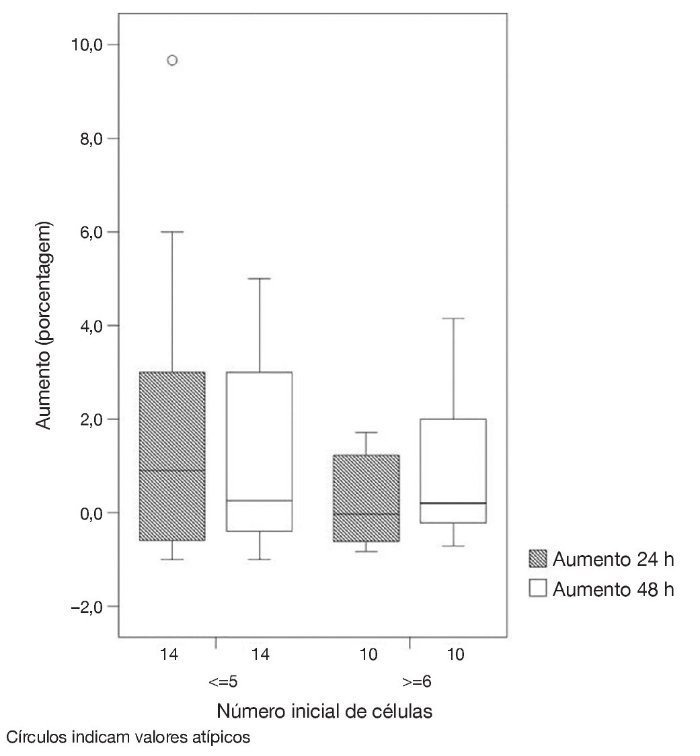
Figura 2 Percentagem de células nos dois grupos (1 e 2), em relação ao tempo: 0h, 24h e 48h.
Entre os pacientes do grupo 2, a contagem de células aumentou com significância estatística em 48 h.
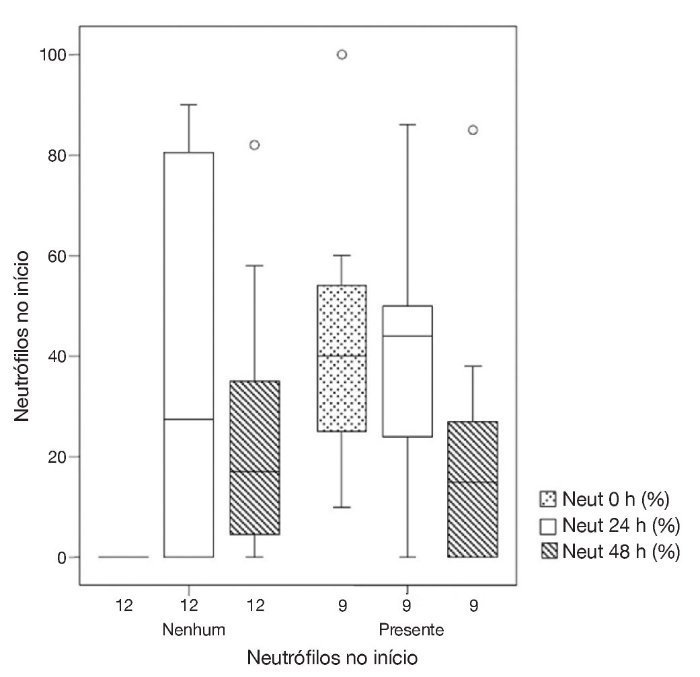
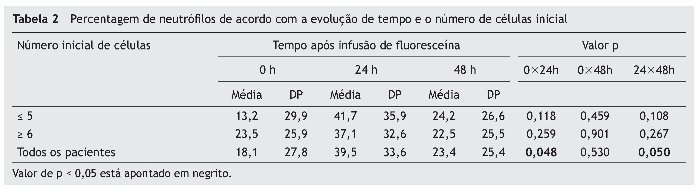
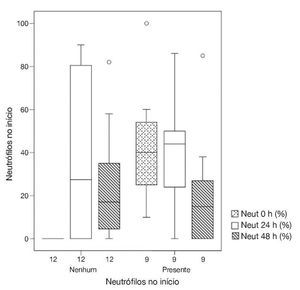
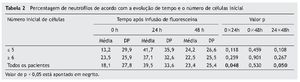
A percentagem de neutrófilos era semelhante em 24h e 48h, em ambos os grupos; em comparação com os valores iniciais, houve um aumento em 24h (p = 0,048) e uma redução em 48h (p = 0,05) (fig. 3, tabela 2).
Figura 3 Evolução do percentual de neutrófilos em 0h, 24h e 48h, em relação aos testes que apresentaram neutrófilos em 0h e os que não apresentaram quaisquer neutrófilos.
Discussão
A coloração intratecal do LCR com fluoresceína foi anteriormente descrita.6,7,12,15,16,19 Tal fato permite a detecção do LCR a partir do sangue ou secreções que estão presentes no campo operatório, justificando a ausência de grupo controle sem aplicação de fluoresceína.
Aplicação intratecal de fluoresceína representa um uso off-label do produto, e a sua utilização exige documentação e uma discussão específica com o paciente a respeito de seu consentimento informado.8 Vários eventos adversos, tais como convulsões, paralisia transitória e dor neuropática, foram esporadicamente atribuídos ao seu uso na literatura.11,12,15 A incidência de complicações permanece extremamente baixa e alguns autores descreveram taxas mais elevadas em pacientes que receberam doses maiores ou mais concentradas do que o descrito neste estudo.15-19 A fisiopatologia destes eventos permanece indefinida, mas pode ser secundária à inflamação das meninges, que altera a química LCR normal e compostos citológicos.8,12,15
O LCR normal tem um teor de proteína de cerca de 20- 45 mg/dL. A dosagem de glicose é cerca de 50-100 mg/dL, e pode conter até cinco células por mL. Nós usamos esses valores para realizar o presente estudo.20
Não foram observadas reações adversas utilizando a solução hipodensa de fluoresceína intratecal na dose descrita neste estudo, nem mesmo em crianças. Com essa dosagem, a visualização do defeito da base do crânio foi considerada eficaz.16,19
Apesar disso, as alterações químicas e citológicas do LCR ocorreram. Em 36% dos pacientes, a cor do LCR, que era transparente na primeira coleta, mudou com o uso de fluoresceína, até 48h após a injeção. Esta observação pode ser correlaciona com os achados de progressão celular e percentual de neutrófilos.
Presença de fluoresceína no CSF pode atuar como fator desencadeante para neutrofilia e aumento da contagem de células, bem como para a sua posterior redução após a diminuição dos níveis de fluoresceína no LCR.
Embora todos os pacientes tenham permanecido com um cateter de drenagem lombar, que foi utilizado somente para coleta de LCR, não podemos supor que essas reações eram apenas por causa da presença do dispositivo, que foi mantido por 48h. Nesse caso, o cateter provocaria um aumento da contagem de células em todos os pacientes, diretamente relacionada com o tempo de exposição, um fato não foi observado.20 Por outro lado, não se pode excluir a possibilidade de que o nitrato fenilmercúrico e o bicarbonato de sódio possam causar algumas das alterações verificadas neste estudo. No entanto, as alterações citológicas foram mínimas, não associadas a efeitos secundários, e que podem ser ainda menor, dependendo da presença destes compostos na solução utilizada.
Não houve alterações significativas nos níveis de glicose no LCR. Esta informação é importante, uma vez que nenhum dos pacientes apresentou qualquer sintoma de meningite bacteriana no estudo. Por outro lado, os níveis de proteína dos pacientes do grupo 1 aumentaram em 24 e 48h (p = 0,032), quando comparados com os pacientes do grupo 2, o que pode ser explicado pelo aumento do número de células presentes no líquido cefalorraquidiano de pacientes grupo1.
Conclusão
Com base nos resultados deste estudo, podemos concluir que a solução hipodensa de fluoresceína intratecal (Fluidag® -fluoresceína de sódio, bicarbonato de sódio e nitrato de phenylmercuric) produz mudanças químicas e citológicas no LCR: aumento do número de células (especialmente em 24h e 48 h) e aumento de neutrófilos em 24 h, com uma consequente diminuição em 48 h. Os níveis de proteína são aumentados em 24 e 48 h. Não houve alterações nos níveis de glicose. Apesar disso, essas mudanças não traduziram qualquer manifestação clínica.
Conflitos de interesse
Os autores declaram não haver conflitos de interesse.
Recebido em 29 de julho de 2013;
aceito em 13 de janeiro de 2014
DOI se refere ao artigo: http://dx.doi.org/10.1016/j.bjorl.2015.07.016
☆ Como citar este artigo: Guimarães RES, Stamm AEC, Giannetti AV, Crosara PFTB, Becker CG, Becker HMG. Chemical and cytological analysis of cerebral spinal fluid after intrathecal injection of hypodense fluorescein. Braz J Otorhinolaryngol. 2015;81:549-53.
☆☆ Instituição: Faculdade de Medicina da Universidade Federal de Minas Gerais (UFMG), Belo Horizonte, Minas Gerais, MG, Brasil.
* Autor para correspondência.
E-mail:resguimaraes@gmail.com (R.E.S. Guimarães).