Olfactory ensheathing cell is a unique kind of glia cells, which can promote axon growth. Little is known about the differences between olfactory mucosa olfactory ensheathing cells and olfactory bulb olfactory ensheathing cells in the capability to promote nerve regeneration.
ObjectiveTo study the recovery of the rat facial nerve after olfactory ensheathing cells transplantation, and to compare the differences between the facial nerve regeneration of olfactory mucosa-olfactory ensheathing and olfactory bulb olfactory ensheathing cells transplantation.
MethodsInstitutional ethical guideline was followed (201510129A). Olfactory mucosa ‐ olfactory ensheathing cells and olfactory bulb olfactory ensheathing cells were cultured and harvested after 7 days in vitro. 36 Sprague Dawley male rats were randomly divided into three different groups depending on the transplanting cells: group A: olfactory mucosa ‐ olfactory ensheathing cells, group B: olfactory bulb olfactory ensheathing cells, group C: DF-12 medium/fetal bovine serum. The main trunk of the facial nerve was transected and both stumps were inserted into a polylactic acid/chitosan conduit, then the transplanted cells were injected into the collagen in the conduits. After 4 and 8 weeks after the transplant, the rats of the three groups were scarified and the facial function score, facial nerve evoked potentials, histology analysis, and fluorescent retrograde tracing were tested and recorded, respectively, to evaluate the facial nerve regeneration and to analysis the differences among the three groups.
ResultsOlfactory ensheathing cells can promote the facial nerve regeneration. Compared with olfactory bulb olfactory ensheathing cells, olfactory mucosa olfactory ensheathing cells were more effective in promoting facial nerve regeneration, and this difference was more significant 8 weeks after the transplantation than 4 weeks.
ConclusionWe discovered that olfactory ensheathing cells with nerve conduit could improve the facial nerve recovery, and the olfactory mucosa olfactory ensheathing cells are more effective for facial nerve regeneration compared with olfactory bulb olfactory ensheathing cells 8 weeks after the transplantation. These results could cast new light in the therapy of facial nerve defect, and furnish the foundation of auto‐transplantation of olfactory mucosa olfactory ensheathing cells in periphery nerve injury.
A célula embainhante olfatória é um tipo especial de célula glial que pode promover o crescimento do axônio. Pouco se sabe sobre as diferenças entre as células embainhantes olfatórias da mucosa olfatória e as células embainhantes olfatórias do bulbo olfatório em relação à sua capacidade de promover a regeneração nervosa.
ObjetivoEstudar a regeneração do nervo facial de ratos após o transplante de células embainhantes olfatórias e comparar as diferenças entre a regeneração do nervo facial com o transplante de células embainhantes olfatórias da mucosa olfatória e de células embainhantes olfatórias do bulbo olfatório.
MétodoAs recomendações éticas da instituição (201510129A) foram seguidas. Células embainhantes olfatórias da mucosa olfatória e células embainhantes olfatórias do bulbo olfatório foram cultivadas in vitro e coletadas após sete dias. Trinta e seis ratos Sprague Dawley machos foram divididos aleatoriamente em três grupos, dependeu das células transplantadas: Grupo A, células embainhantes olfatórias da mucosa olfatória; Grupo B, células embainhantes olfatórias do bulbo olfatório; Grupo C, meio de DF‐12/soro fetal bovino. O tronco principal do nervo facial foi seccionado e ambos os cotos foram inseridos em um conduto de ácido polilático/quitosana; em seguida, as células transplantadas foram injetadas em colágeno nos condutos. Após quatro e oito semanas do transplante, os ratos dos três grupos foram agitados para a obtenção do escore da função facial, potenciais evocados do nervo facial, análise histológica e marcador fluorescente retrógrado, que foram testados e registrados, respectivamente, para avaliar a regeneração do nervo facial e analisar as diferenças entre os três grupos.
ResultadosCélulas embainhantes olfatórias podem promover a regeneração do nervo facial. Em comparação com as células embainhantes olfatórias do bulbo olfatório, as células embainhantes olfatórias da mucosa olfatória foram mais eficazes na promoção da regeneração do nervo facial e essa diferença foi mais significativa oito semanas após o transplante em comparação com quatro semanas.
ConclusãoVerificamos que células embainhantes olfatórias com conduto nervoso podem melhorar a recuperação do nervo facial e as células embainhantes olfatórias da mucosa olfatória são mais eficazes para a regeneração do nervo facial em comparação com as células embainhantes olfatórias do bulbo olfatório oito semanas após o transplante. Esses resultados podem lançar uma nova luz no tratamento de defeitos do nervo facial e fornecer a base do autotransplante de células embainhantes olfatórias da mucosa olfatória em lesões do nervo periférico.
Lesões no nervo facial podem afetar significativamente a qualidade de vida dos pacientes.1 Os tratamentos incluem procedimentos de reinervação cirúrgica (anastomose término‐terminal), enxertos de nervos autólogos etc. Entretanto, muitos tratamentos têm efeitos colaterais graves e a função motora facial dificilmente retorna ao normal após a cirurgia.2
Os nervos periféricos têm o potencial de regeneração após a ocorrência de lesão. As estratégias atuais para o reparo do sistema nervoso periférico lesionado se concentram no desenvolvimento de estruturas de ligação que podem direcionar a regeneração axonal através do local da lesão. Com o desenvolvimento da engenharia de tecidos, é possível usar conexões nervosas, material de preenchimento de enxertos e células germinativas adequadas para conectar o nervo periférico lesionado e promover a regeneração nervosa.2 Estudos anteriores mostraram que o resultado da regeneração de nervos periféricos com o uso de engenharia de tecidos é semelhante ao do transplante autógeno de nervos.3
A célula embainhante olfatória (OEC, do inglês Olfactory Ensheathing Cell) é um tipo especial de célula glial que pode promover o crescimento do axônio.4 As OECs podem manter a organização somatotópica após a lesão, promover a regeneração das fibras nervosas olfatórias e melhorar a organização, bem como a quantidade e a velocidade, da regeneração nervosa.5–7 Muitos estudos mostraram que o transplante de OECs tem um valor terapêutico promissor na lesão nervosa central e periférica, especialmente na lesão da medula espinhal.6,8
Encontrar uma fonte confiável de OECs que seja facilmente acessível e possa assegurar um número suficiente de células é um pré‐requisito importante para estudos sobre a regeneração nervosa mediada por OEC. A maioria dos estudos anteriores obteve OECs do bulbo olfatório (BO) dentro da cavidade craniana.5 Os OECs também podem ser isolados da mucosa olfatória (MO),9,10 a qual pode fornecer uma fonte mais prontamente disponível dessas células para o transplante autólogo. Estudos prévios mostraram que os OECs obtidos a partir da MO eram terapêuticos quando transplantados para o sistema nervoso central (SNC) lesionado ou sistema nervoso periférico (SNP) de pacientes e modelos animais.11–15 Além disso, não há comorbidade associada, pois já foi demonstrado que biópsias olfatórias não prejudicam o sentido do olfato.16
Estudos anteriores mostraram que OECs da MO (MO‐OECs) e OECs do BO (BO‐OECs) têm a capacidade de promover a regeneração dos nervos, mas pouco se sabe sobre suas diferenças. Neste estudo, transplantamos OECs de origens diferentes (MO‐OECs e BO‐OECs) em condutos de ácido polilático (PLA)/quitosana, para estabelecer uma ponte entre o nervo facial lesionado em ratos e comparamos as diferenças entre a função de induzir a regeneração nervosa das MO‐OECs e BO‐OECs. Testes comportamentais, eletrofisiológicos, histológicos e retrógrados foram usados para avaliar os resultados.
MétodoPreparação das OECsAs OECs da mucosa olfatória e do bulbo olfatório de ratos foram isoladas, cultivadas e purificadas, respectivamente.
As MO‐OECs foram cultivadas pelo método de Bianco et al.10 Resumidamente, as biópsias do septo posterior próximo à placa cribriforme do rato SD (Sprague Dawley) foram colocadas em gelo em meio de Eagle modificado por Dulbecco/Ham F12 (DF12; JRH), incubadas durante 45min a 37°C com dispase II (2,4 U/mL em solução de Puck; Boehringer, Mannheim, Alemanha) e em seguida a lâmina própria foi separada do epitélio e lavada em solução salina balanceada de Hanks (HBSS; JRH), depois cortada em pequenos pedaços e incubada em colagenase (0,25%; Tipo I; Sigma, St. Louis, MO) em DMEM/F12 durante 10min a 37°C. Os pellets de tecido foram obtidos por centrifugação, dissociados em células individuais por trituração e depois ressuspensos em DF12 suplementado com soro fetal de vitelo (FCS, 10%) e colocado em frascos de cultura de tecidos revestidos com poli‐L‐lisina (1μg/cm2; Sigma). As células foram cultivadas nesse meio a 37°C/5% CO2 por 48h e em seguida o meio foi mudado para DF12 suplementado com neurotrofina‐3 (50 ng/mL; Alamone Labs, Jerusalém, Israel), processo esse que aumenta a proliferação de OECs.10
As BO‐OECs foram cultivadas pelo método de Nash et al.17 Resumidamente, células das camadas externas do bulbo olfatório de rato SD foram coletadas em 10mL de solução de PBS. Os tecidos foram misturados com 1% de tripsina e depois lavados com meio de crescimento (DF12 50:50, Invitrogen Corp, Carlsbad, CA, EUA e 10% de FCS, Invitrogen). 20mL de solução de DNase foram adicionados aos tecidos e a suspensão foi triturada durante 10 minutos. As células foram então semeadas em placas revestidas com poli‐D‐lisina, com meio de crescimento renovado a cada quatro dias.
S100, GFAP e p75NTR foram usados como marcadores para identificar as OECs.
Preparação do conduto de PLA/quitosanaCondutos de PLA/quitosana e colágeno foram preparados com 3,5mm de comprimento, diâmetro externo de 1,4mm e diâmetro interno de 1,2mm, para estabelecer uma ponte com o defeito e simular a matriz extracelular (MEC) do nervo facial.
Transplante celularAs células foram raspadas da placa para produzir um pequeno bólus gelatinoso de aproximadamente 1mm de diâmetro, o qual foi colocado no local do transplante com uma agulha de ponta fina. Foram necessárias 1,0*107 células por transplante.
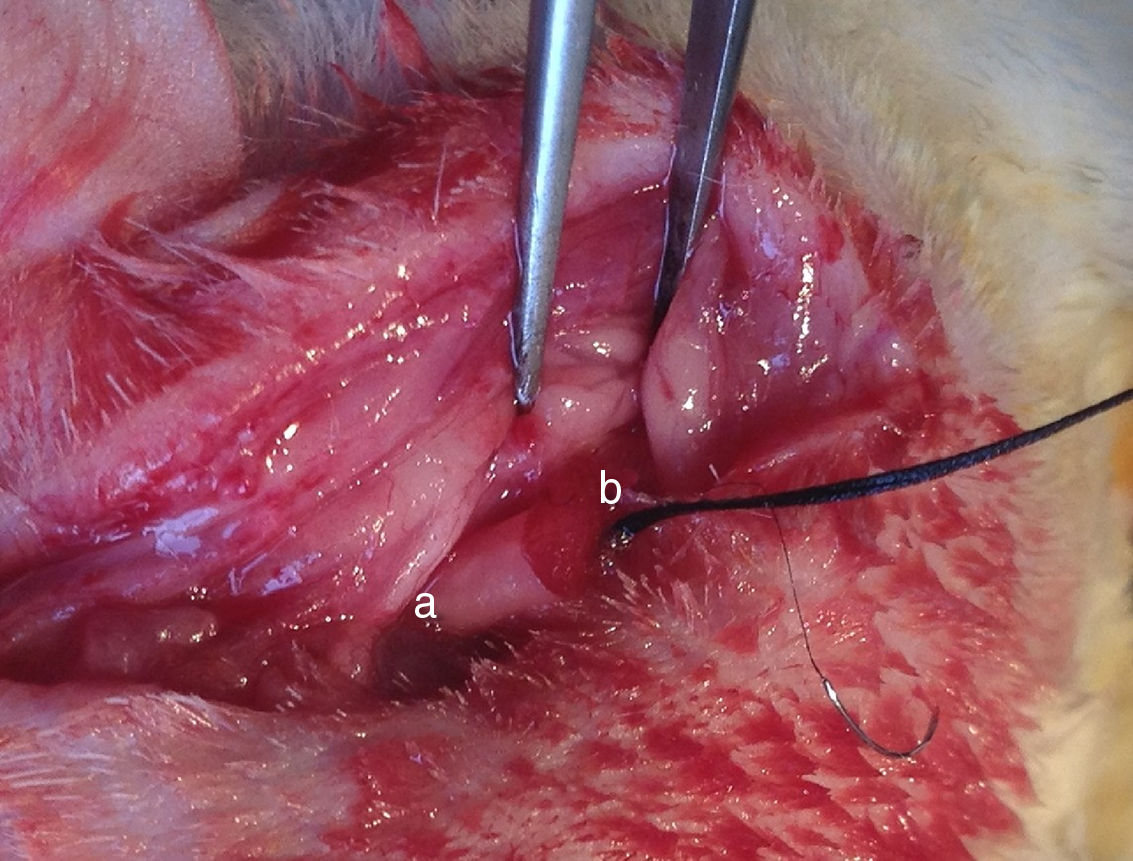
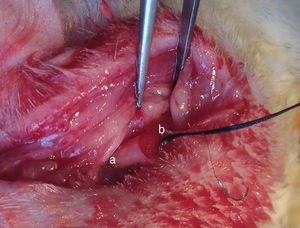
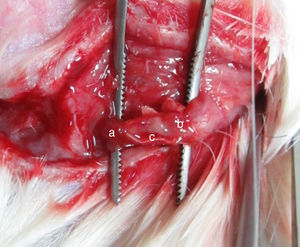
As recomendações institucionais sobre experimentação animal foram acatadas (201510129A). Trinta e seis ratos SD machos foram divididos aleatoriamente em três grupos, dependeu das células transplantadas (12 ratos por grupo): Grupo A, MO‐OECs; Grupo B, BO‐OECs; Grupo C, DF12/FBS. Os ratos foram anestesiados e submetidos ao seccionamento do nervo facial próximo ao seu ponto de emergência no forame mastoideo. O tronco principal do nervo facial foi seccionado e as duas extremidades foram encurtadas para formar uma lacuna de 5mm. A lacuna foi imediatamente ligada com o uso do conduto de PLA/quitosana e as extremidades e condutos foram suturados com a técnica de sutura epineural (fig. 1). Um bólus de células cultivadas reparadoras candidatas foi injetado na esponja de colágeno no conduto. No grupo controle, a parte proximal do nervo facial extracraniano foi exposta.
Após o transplante de OECs, os ratos dos três grupos foram divididos em dois subgrupos (seis ratos por grupo), dependeu do tempo de pós‐operatório a ser analisado: quatro semanas e oito semanas.
AvaliaçãoOs ratos foram agitados para a obtenção do escore da função muscular facial e submetidos a estudo neuroeletrofisiológico, análise histológica e traçador retrógrado fluorescente, respectivamente, para avaliar a regeneração do nervo facial e analisar as diferenças entre os três grupos.
Observação macroscópica e avaliação do escore funcional do músculo facialA função muscular facial foi avaliada através de um escore de 0 a 4. Resumidamente, foram observados o fechamento ocular e o reflexo do piscamento, o movimento e o posicionamento das vibrissas.
- 1.
Sem fechamento ocular, reflexo do piscamento e movimento de vibrissas, com posicionamento não paralelo das vibrissas;
- 2.
Fechamento dos olhos, reflexo de piscamento e movimento de vibrissas fracos, sem movimento voluntário, com posicionamento não paralelo das vibrissas;
- 3.
Fechamento dos olhos, reflexo de piscamento e movimento de vibrissas fracos, com movimento voluntário, com posicionamento não paralelo das vibrissas;
- 4.
Fechamento dos olhos, reflexo de piscamento e movimento das vibrissas quase normais, com posicionamento quase paralelo das vibrissas;
- 5.
Fechamento ocular, reflexo de piscamento e movimento das vibrissas normais, com posicionamento paralelo das vibrissas.
Após quatro e oito semanas da cirurgia, quatro ratos foram escolhidos aleatoriamente em cada grupo para testar os potenciais evocados do nervo facial. Os ratos foram anestesiados e uma incisão anterior foi feita para reexpor o conduto de PLA/quitosana e o nervo facial. O nervo facial normal do outro lado também foi exposto. Os potenciais evocados do nervo facial foram examinados com um testador eletrofisiológico (Keypoint, Frederiksberg, Dinamarca). Uma agulha estimuladora foi colocada entre a extremidade proximal do conduto e do nervo facial normal. Uma agulha de registro foi colocada no músculo orbicular da boca. A intensidade de estimulação foi de 2,0mA, a frequência de estimulação foi de 1Hz, a sensibilidade foi de 5ms/D e o tempo de estimulação foi de 0,1ms. O potencial de ação muscular composto foi medido e o período de latência e amplitude de pico foi registrado no nervo normal e no nervo regenerado.
Análise histológicaQuatro e oito semanas após a cirurgia e o exame eletrofisiológico, quatro ratos de cada grupo foram sacrificados para análise histológica. Os nervos faciais regenerados com condutos de PLA/quitosana foram removidos e examinados.
A área de secção total do nervo foi dividida em dois campos de amostragem, da extremidade distal à extremidade proximal. Um campo foi escolhido aleatoriamente para corte longitudinal e exame com microscopia ótica, enquanto o outro foi usado para corte transversal e análise com microscopia eletrônica.
Para o exame de microscopia ótica foram feitas secções de 1μm do nervo, fixado em formalina tamponada a 10% por 24 horas, desidratado e embebido em blocos de parafina. As secções foram desparafinizadas e coradas com hematoxilina e eosina para análise imuno‐histoquímica e examinadas com ampliação de 100x.
Para o exame de microscopia eletrônica, foram obtidas seções ultrafinas (0,1μm). As secções foram fixadas em glutaraldeído tamponado com cacodilato durante a noite, lavadas e depois armazenadas em tampão cacodilato. As amostras foram fixadas em tetróxido de ósmio, lavadas em séries graduadas de álcool, embebidas em Epon812, cortadas a 100nm em cada uma delas e então coradas com azul de toluidina. As secções foram observadas em um microscópio eletrônico de transmissão com várias ampliações. Foram usados cinco campos de visão selecionados aleatoriamente com aumento de 3600×para calcular o número total, o diâmetro da fibra e a espessura da bainha de mielina.
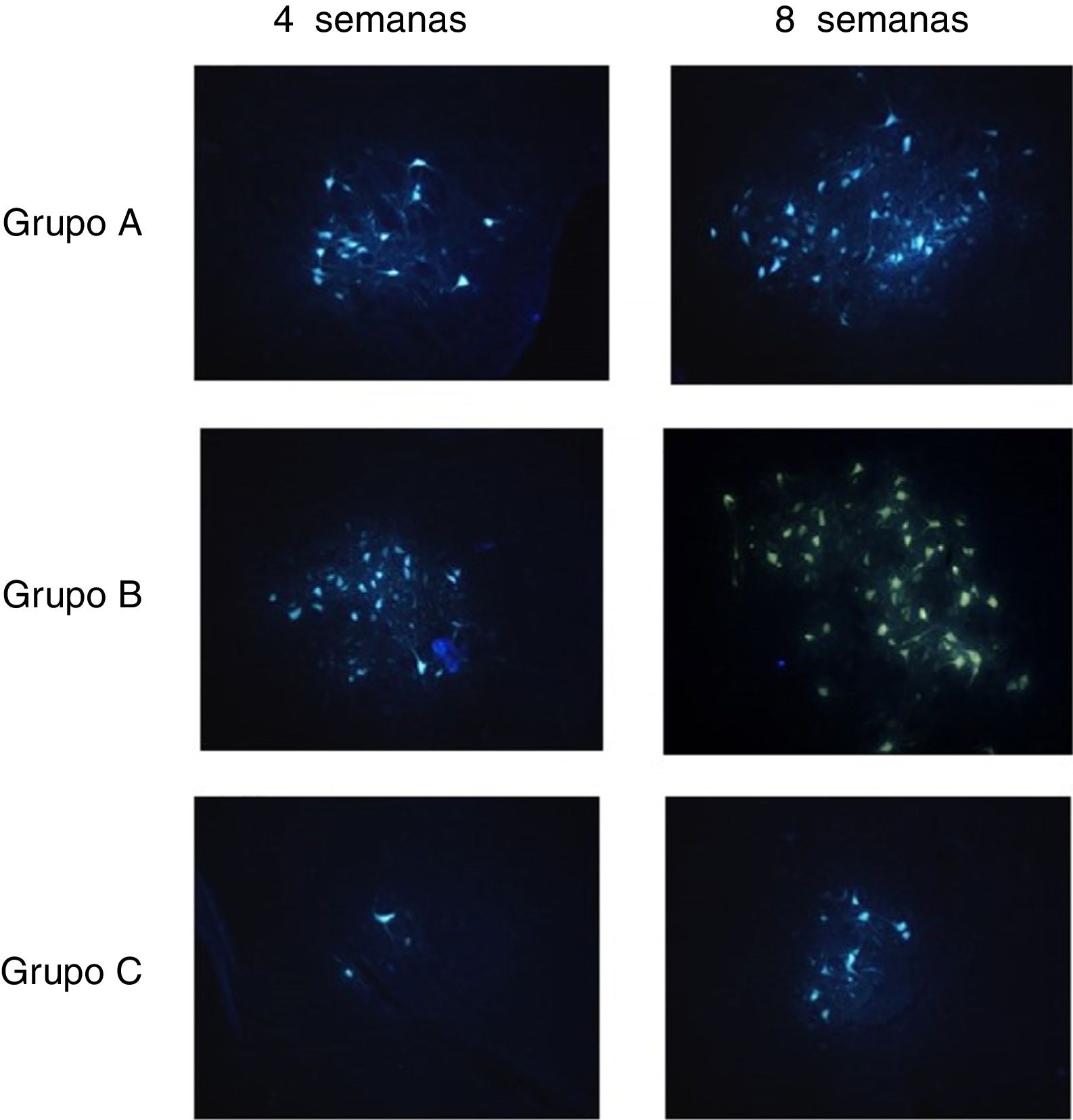
Marcador fluorescente retrógradoQuatro e oito semanas após a cirurgia, os dois ratos remanescentes de cada grupo foram testados para o traçador retrógrado fluorescente. Os ratos foram anestesiados e uma incisão anterior foi feita para reexpor os condutos de PLA/quitosana e o nervo facial regenerado. O nervo facial normal do outro lado também foi exposto. Foram injetados na extremidade distal do nervo facial regenerado 2 uL de solução a 3% de ouro fluorescente (FG, do inglês fluorescente gold) com uma microsseringa. A seguir as incisões foram suturadas. Os ratos sobreviveram 5d após o procedimento e depois foram sacrificados. Solução salina e, em seguida, 0,1 moL de PBS a 4°C com paraformaldeído a 4% e 0,5mL de glutaraldeído foram usados para a perfusão do apêndice atrial direito através da aorta ascendente. Os troncos encefálicos foram coletados e fixados com paraformaldeído a 4% por 24 horas, sacarose a 30% por 48h, enxaguados com água e embebidos em composto OCT (temperatura ótima de corte). Os troncos encefálicos foram então cortados em secções de 25μm e examinados através de microscópio de fluorescência. O número de células marcadas amarelo‐douradas fluorescentes com núcleos ou soma intactos e projeções óbvias foi contado.
Análise estatísticaOs dados foram apresentados como média±desvio‐padrão e analisados por Anova (teste post hoc de Tukey). O nível de significância foi definido em <0,05. O software GraphPad Prism versão 5.0 (GraphPad Software, Inc., San Diego, CA) foi usado.
ResultadosAs OECs de MO e BO de ratos foram isoladas com sucesso e cultivadas e foram obtidas OECs altamente purificadas e estáveis. Todos os ratos sobreviveram à cirurgia.
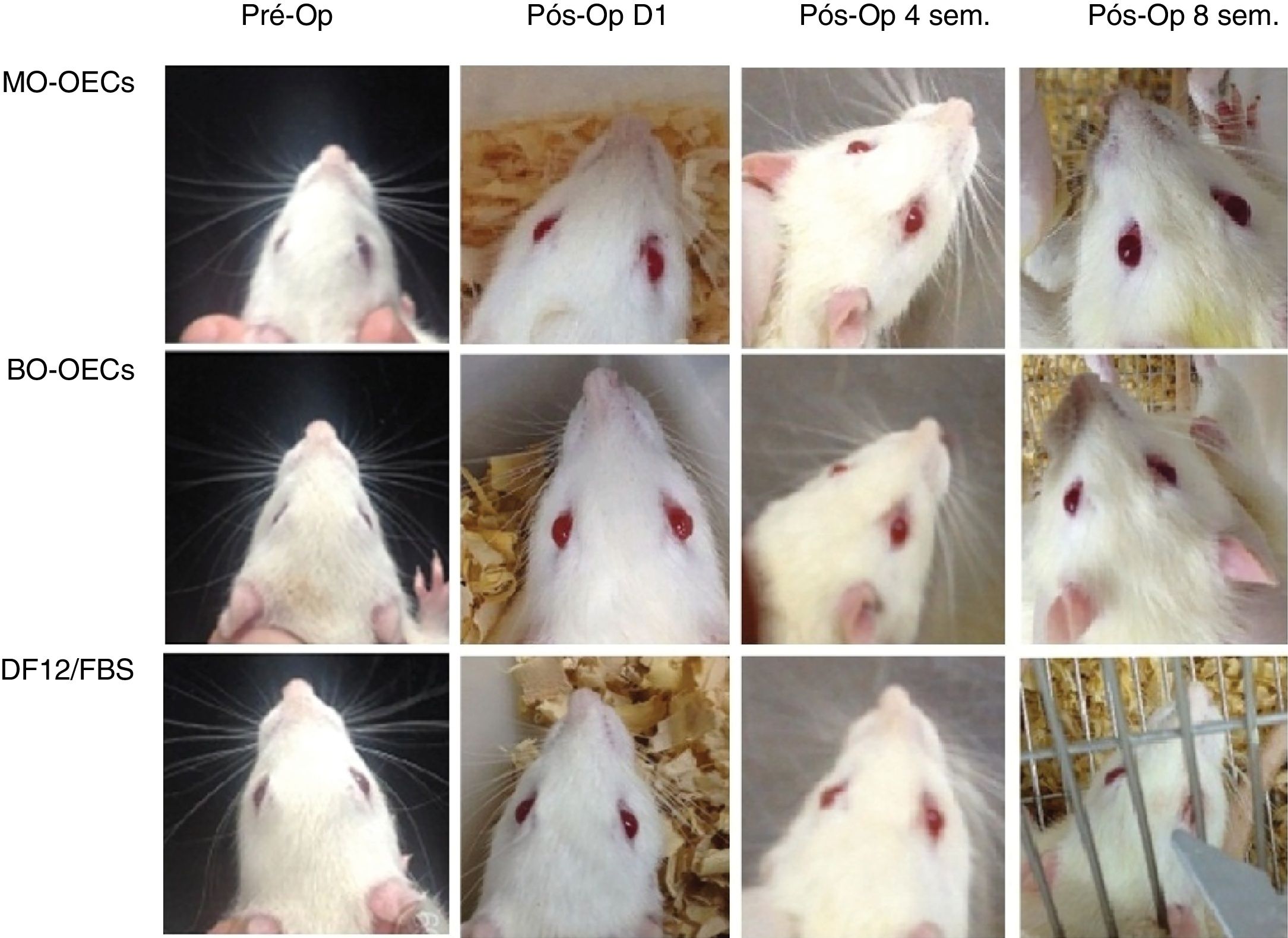
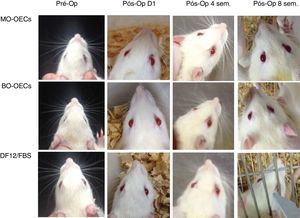
Escore da função de músculo facialImediatamente após a lesão do nervo facial, todos os ratos apresentaram paralisia facial completa do lado da cirurgia, com falha na movimentação da área dos bigodes, pálpebras, região da barba caída e reflexo do piscamento enfraquecido. Nas semanas seguintes, a função facial melhorou em todos os grupos, mas o movimento muscular permaneceu pior em comparação com o lado saudável (fig. 2).
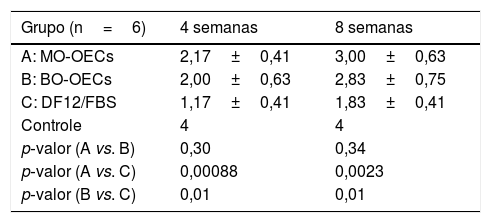
O escore da função facial no Grupo A, B e C, após quatro e oito semanas, foi mostrado na tabela 1. Após quatro e oito semanas, houve diferenças significativas nos escores da função do nervo facial entre os Grupos A, B e C e não houve diferenças entre os grupos A e B (tabela 1).
Resultados do EMGNa eletromiografia, todos os ratos mostraram o prolongamento da latência do tempo e a diminuição da amplitude da tensão nos estímulos após a lesão. Diminuição da latência de tempo e limiar e aumento da amplitude foram observados durante a recuperação.
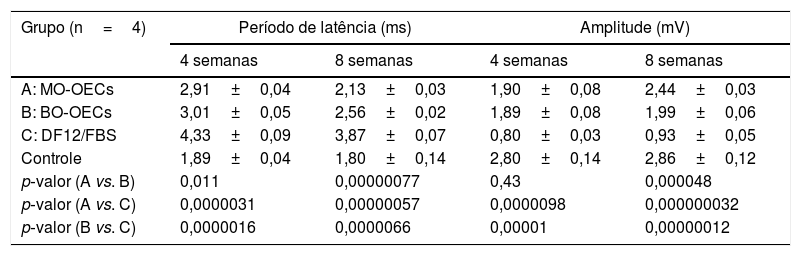
A latência dos potenciais evocados do nervo facial e a amplitude dos potenciais evocados do nervo facial nos grupos A, B e C, após quatro semanas e oito semanas são mostrados na tabela 2. Após quatro semanas, houve diferenças significativas na latência e amplitude entre os Grupos A, B e C e não houve diferenças entre os Grupos A e B. Após oito semanas, houve diferenças significativas na latência e amplitude entre os grupos A, B e C, latência em A˂ B ˂ C, amplitude em A ˃ B ˃ C (tabela 2).
Potenciais evocados do nervo facial (x±s)
| Grupo (n=4) | Período de latência (ms) | Amplitude (mV) | ||
|---|---|---|---|---|
| 4 semanas | 8 semanas | 4 semanas | 8 semanas | |
| A: MO‐OECs | 2,91±0,04 | 2,13±0,03 | 1,90±0,08 | 2,44±0,03 |
| B: BO‐OECs | 3,01±0,05 | 2,56±0,02 | 1,89±0,08 | 1,99±0,06 |
| C: DF12/FBS | 4,33±0,09 | 3,87±0,07 | 0,80±0,03 | 0,93±0,05 |
| Controle | 1,89±0,04 | 1,80±0,14 | 2,80±0,14 | 2,86±0,12 |
| p‐valor (A vs. B) | 0,011 | 0,00000077 | 0,43 | 0,000048 |
| p‐valor (A vs. C) | 0,0000031 | 0,00000057 | 0,0000098 | 0,000000032 |
| p‐valor (B vs. C) | 0,0000016 | 0,0000066 | 0,00001 | 0,00000012 |
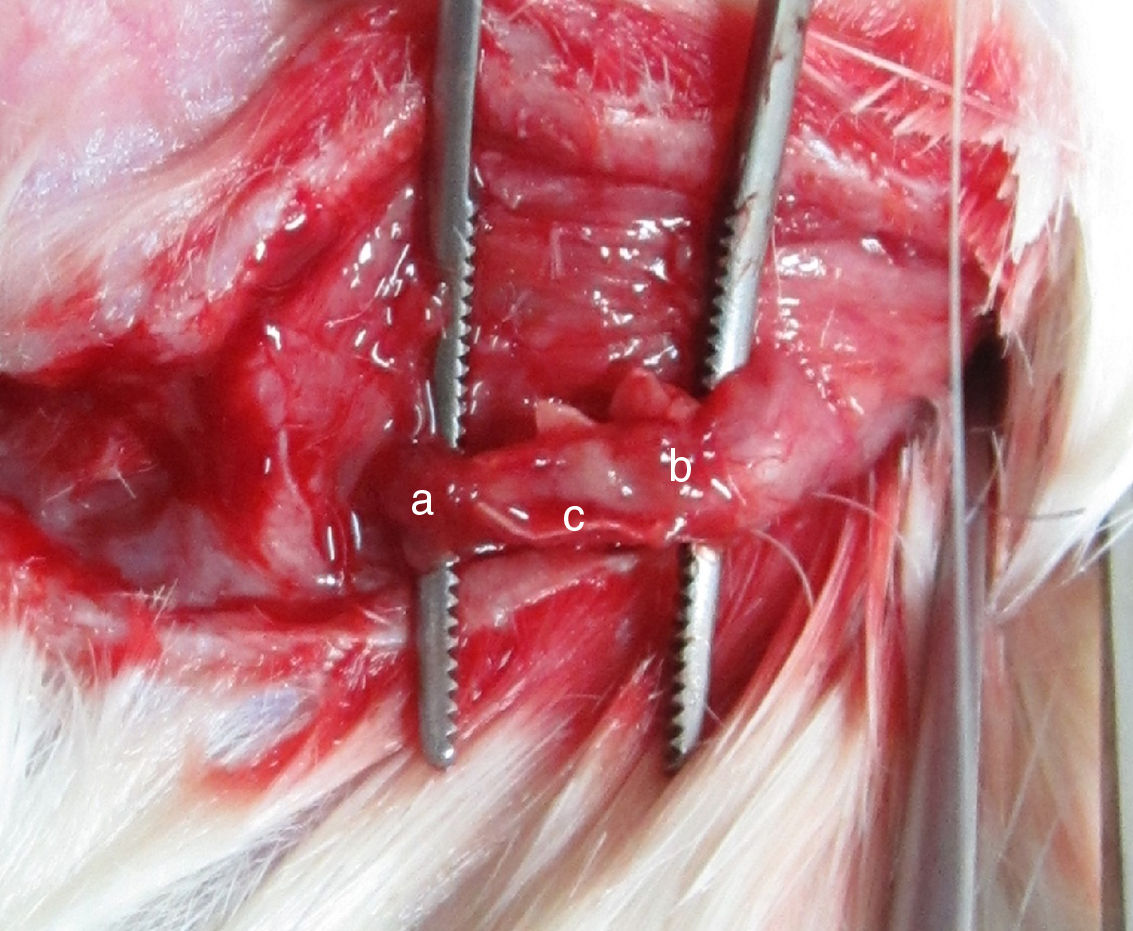
Quatro semanas após a cirurgia, as lesões nos nervos se encontravam reparados através da regeneração nervosa em todos os grupos. Não houve dificuldade ao separar os nervos, pois não houve adesões, nem formação de tecido cicatricial. Não houve formação de neuroma nas extremidades proximal e distal do nervo regenerado. Os condutos de PLA/quitosana ficaram mais finos e fáceis de fraturar, mas ainda estavam intactos. Oito semanas após a cirurgia, os condutos de PLA/quitosana foram parcialmente absorvidos e suas paredes não se encontravam intactas. Nos Grupos A e B, o nervo facial regenerado apresentava boa continuidade, sem diminuição da espessura e firmeza. A aparência dos nervos regenerados era semelhante à do nervo normal (fig. 3).
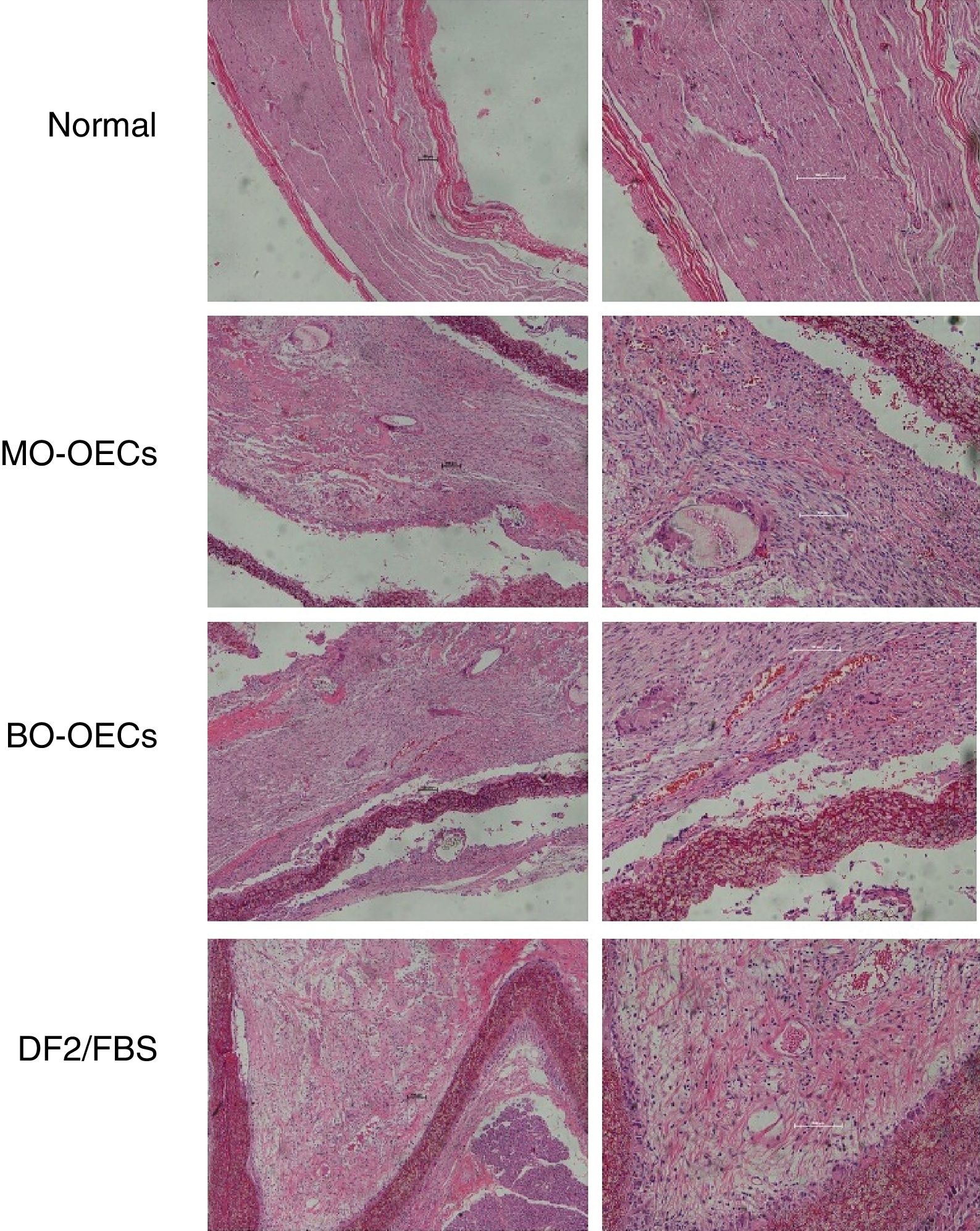
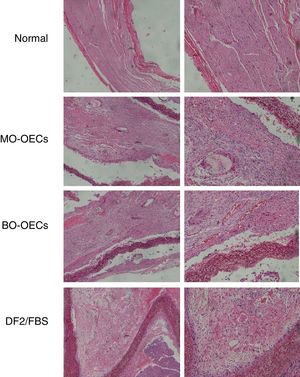
Achados à microscopia ópticaO nervo facial normal tem axônios mielinizados, com uma camada de mielina espessa e uniforme, composta de um a cinco fascículos envolvidos por epineuro com células fusiformes, e os axônios apresentam organização regular e diâmetros similares (Aumento original 2000x).
Quatro semanas após a cirurgia, no Grupo A, os axônios mielinizados de grande diâmetro estavam quase normais, mas os axônios mielinizados de pequeno diâmetro se encontravam irregulares. No Grupo B, ocasionalmente um axônio mielinizado apresentava‐se com muitas células de Schwann e morfologia variável. No Grupo C, havia uma grande quantidade de aglomerados de mielina escura degenerados, sem axônios (bandas de Büngner) e fibrose grave, e o perineuro era uma condensação de tecido conjuntivo frouxo.
Oito semanas após a cirurgia, a maturidade do nervo regenerado apresentava melhoria em todos os grupos em comparação com aquela vista após quatro semanas. No grupo A, os feixes nervosos regenerados eram semelhantes aos nervos normais, com tamanho uniforme. As mielinas eram densas, sem deterioração. As células de Schwann estavam bem distribuídas, com núcleos de células de tamanho e formato similares. No Grupo B, vasos abundantes foram vistos no epineuro, bem como fibras nervosas regeneradas agrupadas e muita neovascularização nos feixes de fibras nervosas. No Grupo C, havia menos axônios regenerados com distribuição desigual e desenvolvimento deficiente e tecido conjuntivo fibroso abundante (fig. 4).
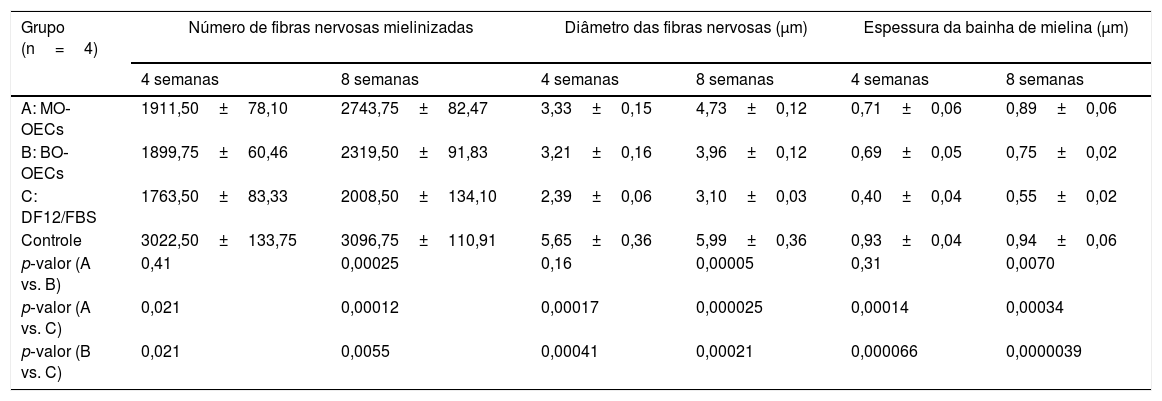
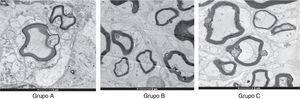
Achados à microscopia eletrônicaA tabela 3 mostra o número de fibras nervosas mielinizadas, o diâmetro da fibra nervosa e a espessura da bainha de mielina nos Grupos A, B e C, após quatro semanas e oito semanas, respectivamente.
Achados à microscopia eletrônica (x±s)
| Grupo (n=4) | Número de fibras nervosas mielinizadas | Diâmetro das fibras nervosas (μm) | Espessura da bainha de mielina (μm) | |||
|---|---|---|---|---|---|---|
| 4 semanas | 8 semanas | 4 semanas | 8 semanas | 4 semanas | 8 semanas | |
| A: MO‐OECs | 1911,50±78,10 | 2743,75±82,47 | 3,33±0,15 | 4,73±0,12 | 0,71±0,06 | 0,89±0,06 |
| B: BO‐OECs | 1899,75±60,46 | 2319,50±91,83 | 3,21±0,16 | 3,96±0,12 | 0,69±0,05 | 0,75±0,02 |
| C: DF12/FBS | 1763,50±83,33 | 2008,50±134,10 | 2,39±0,06 | 3,10±0,03 | 0,40±0,04 | 0,55±0,02 |
| Controle | 3022,50±133,75 | 3096,75±110,91 | 5,65±0,36 | 5,99±0,36 | 0,93±0,04 | 0,94±0,06 |
| p‐valor (A vs. B) | 0,41 | 0,00025 | 0,16 | 0,00005 | 0,31 | 0,0070 |
| p‐valor (A vs. C) | 0,021 | 0,00012 | 0,00017 | 0,000025 | 0,00014 | 0,00034 |
| p‐valor (B vs. C) | 0,021 | 0,0055 | 0,00041 | 0,00021 | 0,000066 | 0,0000039 |
Após quatro semanas, o número de fibras nervosas regeneradas, o diâmetro da fibra e a espessura da bainha de mielina nos Grupos A e B eram superiores aos do Grupo C e não houve diferenças entre os Grupos A e B. Após oito semanas, o número de fibras nervosas regeneradas, o diâmetro da fibra e a espessura da bainha de mielina no Grupo A eram superiores aos do Grupo B e os do Grupo B eram superiores aos do Grupo C (fig. 5).
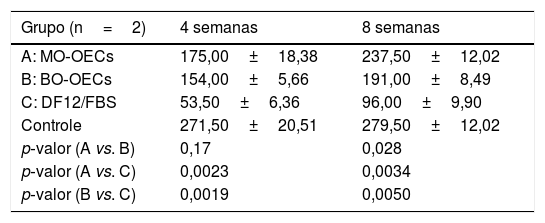
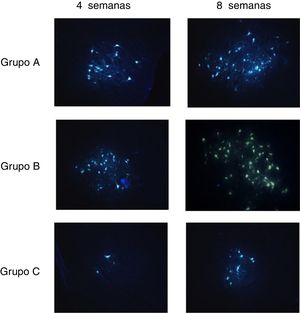
Marcador fluorescente retrógradoA tabela 4 mostra os números médios de células marcadas com FG no núcleo facial quatro e oito semanas após o transplante de células nos Grupos A, B e C, respectivamente.
Número de células marcadas com FG (x±s)
| Grupo (n=2) | 4 semanas | 8 semanas |
|---|---|---|
| A: MO‐OECs | 175,00±18,38 | 237,50±12,02 |
| B: BO‐OECs | 154,00±5,66 | 191,00±8,49 |
| C: DF12/FBS | 53,50±6,36 | 96,00±9,90 |
| Controle | 271,50±20,51 | 279,50±12,02 |
| p‐valor (A vs. B) | 0,17 | 0,028 |
| p‐valor (A vs. C) | 0,0023 | 0,0034 |
| p‐valor (B vs. C) | 0,0019 | 0,0050 |
Após quatro semanas, houve diferenças significativas no número de células marcadas com FG entre os grupos A, B e C e não houve diferenças entre os grupos A e B. Após oito semanas, houve diferenças significativas no número de células marcadas com FG entre os grupos A B e C; A ˃ B ˃ C (p < 0,01) (tabela 4) (fig. 6).
DiscussãoO transplante de células gliais tem sido frequentemente usado para promover a regeneração axonal no sistema nervoso central e periférico (SNC/SNP). As células formadoras de mielina geralmente usadas para transplante são as células de Schwann, as células embainhantes olfatórias, et al.18 As OECs são um tipo especial de célula glial que compartilham algumas propriedades com astrócitos e células de Schwann, mas têm algumas propriedades intrínsecas. Estudos mostraram que as OECs podem mediar os efeitos neurotróficos e neuroprotetores através da secreção de quimiocinas, aumentar a regeneração axonal e produzir mielina após o transplante.4 Foi observado que as OECs podem promover a regeneração axonal de neurônios do SNC e do SNP em cultura e in vivo,6 o que as torna candidatas ideais para o transplante de células.
O bulbo olfatório (BO) é a fonte mais comumente usada para obter OECs na maioria dos estudos. Entretanto, não é um sítio preferido clinicamente para a obtenção de OECs autólogas devido à morbidade associada ao acesso cirúrgico e destruição dos bulbos olfatórios na obtenção das células. As OECs também podem ser isoladas da mucosa olfatória (MO). Estudos anteriores mostraram que MO‐OECs também têm a capacidade de promover a regeneração nervosa,13 mas há poucos estudos sobre as diferenças entre MO‐OECs e BO‐OECs em relação aos seus efeitos na regeneração nervosa.
Sabe‐se que o sistema nervoso periférico tem a capacidade de alcançar recuperação funcional após lesão nervosa e os neurônios faciais de ratos são capazes de preencher lacunas de até 10mm. Existem alguns estudos sobre diferentes métodos para facilitar a regeneração do nervo facial19–24 e alguns autores estudaram o transplante de OECs na lesão do nervo facial,23,24 mas a maioria dos estudos concentrou‐se na ramificação colateral de axônios do nervo facial regenerado. Recentemente, um estudo sobre células‐tronco olfatórias humanas de MO mostrou melhoria na recuperação da lesão do nervo facial de ratos em relação a duas medidas: análise do movimento dos bigodes e da eletroneuronografia.24 Em nosso estudo, tentamos usar diferentes medidas para melhor avaliar o resultado da regeneração nervosa no transplante de OECs com diferentes orientações após a lesão do SNP.
A função do músculo facial é o resultado mais objetivo da regeneração nervosa. A recuperação da função muscular facial é o último passo da regeneração nervosa, o que significa que o nervo regenerado tem a capacidade de controlar o músculo‐alvo. Após quatro e oito semanas, foram observadas diferenças significativas nos escores de função do nervo facial entre os Grupos A, B e C e não houve diferenças entre os Grupos A e B. O resultado significa que as funções musculares faciais foram semelhantes nos Grupos A e B. Entre os três grupos, os ratos do Grupo C mostraram a pior função facial. Pode‐se concluir a partir dos resultados que tanto as MO‐OECs quanto as BO‐OECs podem estimular a regeneração do nervo facial lesionado.
O potencial evocado do nervo facial é o índice mais efetivo para mostrar o grau de regeneração do nervo lesionado. A melhoria dos potenciais evocados significa que o nervo regenerado foi capaz de conduzir potenciais de ação ao tecido‐alvo. Após quatro semanas, houve diferenças significativas na latência e amplitude entre os Grupos A, B e C e não houve diferença entre os Grupos A e B. Após oito semanas, a latência em A ˂ B ˂ C, enquanto a amplitude em A ˃ B ˃ C. Estudos mostraram que o potencial evocado do nervo facial é o primeiro sinal a demonstrar alteração após a regeneração nervosa efetiva, enquanto a função muscular é a última a demonstrar a alteração,25 o que explica o fato de que após oito semanas houve diferenças significativas na latência e amplitude entre os Grupos A, B e C, mas não houve diferenças entre os Grupos A e B em relação aos escores da função muscular facial.
A análise histológica fornece uma observação direta da regeneração nervosa. Os achados da microscopia óptica mostram que a regeneração no Grupo A foi melhor do que no Grupo B e o Grupo B foi melhor do que o Grupo C. Após oito semanas, os nervos regenerados do Grupo A foram semelhantes aos normais. Foram calculados os valores do número de fibras nervosas, o diâmetro da fibra da bainha de mielina e as alterações na bainha de mielina nos três grupos sob microscopia eletrônica. Os resultados estavam de acordo com os achados da microscopia óptica. Essas observações histológicas revelaram que o transplante de OECs pode levar à regeneração do tecido nervoso com grande número de fibras nervosas mielinizadas, fibras brutas e maior espessura e volume de mielina no enxerto transplantado e o transplante de MO‐OECs parece apresentar melhores resultados em longo prazo.
Os resultados do marcador fluorescente retrógrado mostraram que os nervos regenerados tinham estabelecido uma conexão eficiente com o núcleo facial. A estrutura histológica do nervo regenerado conectando as duas extremidades do nervo lesionado é apenas o primeiro passo para a recuperação funcional completa. Isso não significa que o nervo regenerado tenha alcançado a restauração funcional completa, apenas que o nervo regenerado tem uma conexão eficiente com o núcleo facial, o que significa que a passagem pelo nervo está estabelecida.26 Neste estudo, contamos as células marcadas com FG no núcleo facial quatro e oito semanas após o transplante de células. Os resultados mostraram que o transplante de OECs estimulou a conexão entre o nervo regenerado e o núcleo facial e que o transplante de MO‐OECs teve um efeito melhor na conexão nervosa em comparação com BO‐OECs em longo prazo.
Neste estudo, a regeneração do nervo facial foi avaliada de quatro maneiras: avaliação funcional do órgão terminal, eletrofisiologia, histologia (qualitativa e quantitativa), avaliação da via de conexão nervosa total. Quase todas as quatro avaliações tiveram resultados semelhantes: as OECs podem promover a regeneração do nervo facial lesionado. Em comparação com BO‐OECs, as MO‐OECs foram mais eficazes na promoção da regeneração nervosa e essa diferença foi mais significativa oito semanas após o transplante do que depois de quatro semanas.
Esses resultados mostraram que o transplante de OECs com nervos em condutos pode atuar como uma ferramenta poderosa para reforçar a regeneração nervosa periférica sob condições adversas, por exemplo, um longo espaço entre as duas extremidades, e as MO‐OECs podem ser uma fonte mais conveniente e eficaz para o transplante. Ainda há questões remanescentes que precisam ser abordadas. Por exemplo, a síndrome pós‐paralítica (movimentos anormalmente associados após a transecção do nervo facial) é causada por um dado grupo muscular reinervado por ramificações axonais mal orientadas. Demonstrou‐se que as células embainhantes olfatórias reduzem a brotação axonal e estimulam a regeneração axonal após o transplante na medula espinhal. O transplante de OECs também poderia reduzir o surgimento de um nervo motor periférico puro danificado? O transplante de OECs é mais eficaz em comparação com a anastomose facial‐facial simples? Qual é o mecanismo das OECs transplantadas que promove a regeneração nervosa?
ConclusãoVerificamos que o uso das OECs com o nervo em um conduto poderia melhorar a recuperação do nervo facial lesionado e que as MO‐OECs são mais eficazes para a regeneração do nervo facial em comparação com as BO‐OECs oito semanas após o transplante. Esses resultados podem lançar uma nova luz sobre a descoberta de novos tratamentos para defeitos do nervo facial e fornecer a base para o autotransplante de OECs da mucosa olfatória na lesão do nervo periférico. Mais estudos são necessários para confirmar nossos achados e desvendar os mecanismos subjacentes.
FinanciamentoNational Natural Science Foundation of China (n° 81300837).
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Li M, Zhu Q, Liu J. Olfactory ensheathing cells in facial nerve regeneration. Braz J Otorhinolaryngol. 2020;86:525–33.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.