Serum‐ and glucocorticoid‐inducible kinase 3, a serine/threonine kinase that functions downstream of the PI3K signaling pathway, plays a critical role in neoplastic processes. It is expressed by various tumors and contributes to carcinogenesis.
ObjectiveThe objective was to investigate serum‐ and glucocorticoid‐inducible kinase 3 expression in nasopharyngeal carcinoma, to study the anti‐tumor effects of serum‐ and glucocorticoid‐inducible kinase 3 shRNA by inhibiting its expression in nasopharyngeal carcinoma cells and to discuss the potential implications of our findings.
MethodsSerum‐ and glucocorticoid‐inducible kinase 3 protein expression in nasopharyngeal carcinoma cell lines (CNE‐1, CNE‐2, HNE‐1, HONE‐1, and SUNE‐1) and the human immortalized nasopharyngeal epithelium cell line NP69 were assayed by western blotting. Serum‐ and glucocorticoid‐inducible kinase 3 expression in 42 paraffin‐embedded nasopharyngeal carcinoma tissues were performed by immunohistochemistry. MTT assay, flow cytometry, and scratch tests were performed after CNE‐2 cells were transfected with the best serum‐ and glucocorticoid‐inducible kinase 3 shRNA plasmid selected by western blotting using lipofectamine to study its effect on cell proliferation, apoptosis, and migration.
ResultsSerum‐ and glucocorticoid‐inducible kinase 3 was overexpressed in human nasopharyngeal carcinoma tissues and cells. Serum‐ and glucocorticoid‐inducible kinase 3 expression decreased markedly after CNE‐2 cells were transfected with the serum‐ and glucocorticoid‐inducible kinase 3 shRNA, leading to strong inhibition of cell proliferation and migration. In addition, the apoptosis rate increased in CNE‐2 cells after serum‐ and glucocorticoid‐inducible kinase 3 knockdown.
ConclusionSerum‐ and glucocorticoid‐inducible kinase 3 expression was more frequently observed as the nasopharyngeal epithelium progresses from normal tissue to carcinoma. This suggests that serum‐ and glucocorticoid‐inducible kinase 3 contributes to the multistep process of NPC carcinogenesis. Serum‐ and glucocorticoid‐inducible kinase 3 represents a target for nasopharyngeal carcinoma therapy, and a basis exists for the further investigation of this adjuvant treatment modality for nasopharyngeal carcinoma.
A quinase 3 sérica induzida por glicocorticoide, uma serina/treonina quinase que funciona downstream da via de sinalização PI3K, desempenha um papel crítico nos processos neoplásicos. É expressa por vários tumores e contribui para a carcinogênese.
ObjetivoInvestigar a expressão de quinase 3 sérica induzida por glicocorticoide no carcinoma nasofaríngeo, estudar os efeitos antitumorais do shRNA da quinase 3 sérica induzida por glicocorticoide, que inibem sua expressão em células de carcinoma nasofaríngeo, e discutir as implicações potenciais de nossos achados.
MétodoA expressão de proteína quinase 3 sérica induzida por glicocorticoide em linhagens de células de carcinoma nasofaríngeo (CNE‐1, CNE‐2, HNE‐1, HONE‐1 e SUNE‐1) e a linhagem de células humanas imortalizadas do epitélio nasofaríngeo NP69 foram avaliadas por Western blot. A expressão da quinase 3 sérica induzida por glicocorticoide em 42 tecidos de CNF embebidos em parafina foi feita por imuno‐histoquímica. Testes com MTT, citometria de fluxo e testes de raspagem foram feitos após as células CNE‐2 terem sido transfectadas com o melhor plasmídeo shRNA da quinase 3 sérica induzida por glicocorticoide selecionado por Western blot, com o uso de lipofectamina para estudar seu efeito na proliferação, apoptose e migração celular.
ResultadosFoi observada uma sobre‐expressão da quinase 3 sérica induzida por glicocorticoide em tecidos e células de carcinoma nasofaríngeo humanas. A expressão de quinase 3 sérica induzida por glicocorticoide diminuiu acentuadamente após as células CNE‐2 terem sido transfectadas com o shRNA da quinase 3 sérica induzida por glicocorticoide, conduzindo a forte inibição de proliferação e migração celular. Além disso, a taxa de apoptose aumentou nas células CNE‐2 após o knockdown da quinase 3 sérica induzida por glicocorticoide.
ConclusãoA expressão de quinase 3 sérica induzida por glicocorticoide foi observada com maior frequência à medida que o epitélio nasofaríngeo progride de tecido normal para carcinoma. Isso sugere que a quinase 3 sérica induzida por glicocorticoide contribui para o processo multietapas da carcinogênese do carcinoma nasofaríngeo. A quinase 3 sérica induzida por glicocorticoide representa um alvo para a terapia do carcinoma nasofaríngeo e há uma base para a investigação adicional dessa modalidade de tratamento adjuvante para o carcinoma nasofaríngeo.
O carcinoma de nasofaringe (CNF) é um dos tumores de cabeça e pescoço mais comuns, origina‐se da mucosa da nasofaringe.1 Sua ocorrência é frequente no sul da China e no sudeste da Ásia devido à sua distribuição regional e agregação familiar.2 O CNF é especialmente comum na China, com uma incidência de 20/100.000, mas extremamente raro nos países ocidentais, com uma incidência de menos de 1/100.000.3
Os tipos histopatológicos de CNF são em sua maioria carcinomas de células escamosas pouco diferenciados, que exibem um alto grau de metástase linfonodal cervical e malignidade no estágio inicial.4 Estima‐se que ocorreram 60.600 casos incidentes de CNF e 34.100 mortes relatadas na China em 2015.5 Além disso, o número de novos casos de CNFs tem aumentado exponencialmente.
O tratamento abrangente consiste em radioterapia combinada com quimioterapia, é atualmente a principal estratégia de tratamento clínico para CNF,6 a recidiva local e a metástase a distância são as principais razões para o insucesso do tratamento de CNF.7 A patogênese do CNF não é clara e fatores adicionais podem estar envolvidos, como histórico familiar, suscetibilidade genética, fatores ambientais ou estocásticos e infecção pelo vírus Epstein‐Barr (EBV).3 No entanto, os processos moleculares envolvidos na patogênese do CNF ainda não foram bem definidos. Uma melhor compreensão dos mecanismos moleculares da progressão do CNF contribuirá para o desenvolvimento de novas abordagens terapêuticas e a melhoria da sobrevivência de pacientes com CNF.
Quinases séricas induzidas por glicocorticoide (SGKs) são serina/treonina quinases que funcionam downstream da via de sinalização do fosfoinositídeo 3‐quinase (PI3‐K). 8 As SGKs têm 3 isoformas em mamíferos (SGK1, SGK2 e SGK3) e pertencem à família da AGC quinase (proteína quinase A, proteína quinase G e proteína quinase C), semelhantemente à proteína quinase B/AKT.9 As SGKs compartilham grande homologia no domínio da quinase com AKT,10 estão envolvidas na via PI3‐K e regulam processos celulares semelhantes à AKT. Como membro da família SGK, a ativação e a fosforilação da SGK3 na Thr320 pela quinase dependente de fosfoinositídeos‐1 (PDK1) são consideradas uma forma de sinalização independente da AKT no câncer.11 Foi sugerido que a SGK3 desempenha um papel fundamental na gênese e no desenvolvimento de muitos tumores.12–16 Entretanto, pouca atenção tem sido dada aos seus efeitos no CNF.
Neste artigo, analisamos a expressão e os papéis potenciais da SGK3 no CNF humano. Nossos estudos identificam a SGK3 como um novo potencial promotor do desenvolvimento de CNF humano e sugerem um novo alvo terapêutico para o tratamento da doença.
MétodoMaterialAs linhagens de células humanas de CNF (CNE‐1, CNE‐2, HNE‐1, HONE‐1 e SUNE‐1) e a linhagem de células humanas imortalizadas do epitélio nasofaríngeo NP69 foram preservadas pelo nosso laboratório. A CNE1 é uma linhagem de carcinoma de células escamosas bem diferenciada de carcinoma nasofaríngeo; CNE2, HNE1, HONE1, SUNE1 são linhagens de células escamosas pouco diferenciadas de carcinoma nasofaríngeo; a NP69 é uma linhagem de células epitelial nasofaríngeas imortalizadas, apresenta crescimento epitelioide e aderente escamoso, com características normais do epitélio nasofaríngeo. As cinco linhas de células CNF foram cultivadas em meio RPMI‐1640 (Gibco, Life Technologies Inc., Carlsbad, CA, EUA), contêm 10% de soro fetal bovino (FBS, Tianhang Biotechnology Co., Ltd., Zhejiang, China). As células NP69 foram cultivadas em meio queratinócito/isento de soro (K‐SFM; Gibco) suplementado com extrato de pituitária bovina (BPE; Gibco) e fator de crescimento epidérmico (EGF, recombinante humano; Gibco).
Todas as células foram cultivadas a 37 com 5% de CO2. Os plasmídeos SGK3 shRNA foram todos produzidos por GeneCopoeia Inc., Rockville, MD, EUA e incluíram sh1025, sh1132, sh1206 e sh1284; as sequências são 5’‐GCTAGTGCATTGGGTTACTTA‐3’, 5’‐GCTTTGTAAAGAAGGAATTGC‐3’, 5’‐GCCGAGATGTTGCTGAAATGT‐3’, e 5’‐GGTCCATTCTGGAAGAACTCC‐3’, respectivamente. O plasmídeo de controle negativo (CN), sequência 5’‐GCTTCGCGCCGTAGTCTTA‐3’, também foi adquirido da GeneCopoeia Inc. Para se obter a melhor sequência do plasmídeo no silenciamento do gene, as células foram semeadas antes de ser transfectadas e seu crescimento foi permitido até a densidade de 60% no segundo dia. O polímero catiônico PEI (adquirido da Aladdin Inc.) foi usado para transfectar os plasmídeos com diferentes sequências de ShRNA (local silencioso diferente de SGK3) nas células. Após 72 horas, as proteínas das células foram extraídas e Western blot foi usado para observar os efeitos de silenciamento de ShRNA em SGK3 e selecionar o plasmídeo com a melhor sequência de silenciamento. A melhor sequência é 5’‐GCTAGTGCATTGGGTTACTTA‐3’.
Equipamentos principaisA incubadora de dióxido de carbono foi produzida pela Thermo Fisher Scientific Inc., EUA. Micrótomo rotativo HM340E‐ e equipamento de coloração de hematoxilina‐eosina (HE) totalmente automático foram produzidos pela MICROM Inc., Alemanha. O aparelho de eletroforese vertical e o sistema transmembrana foram produzidos pela Bio‐Rad Inc., Hercules, Califórnia, EUA. O sistema de imagem por quimiluminescência ChemiDocTM XRS + também foi produzido pela Bio‐Rad Inc. O citômetro de fluxo BD FACSCaliburTM foi produzido pela BD Biosciences Inc. California, EUA. O microscópio de fluorescência invertida foi produzido por Carl Zeiss Co. Ltd., Alemanha.
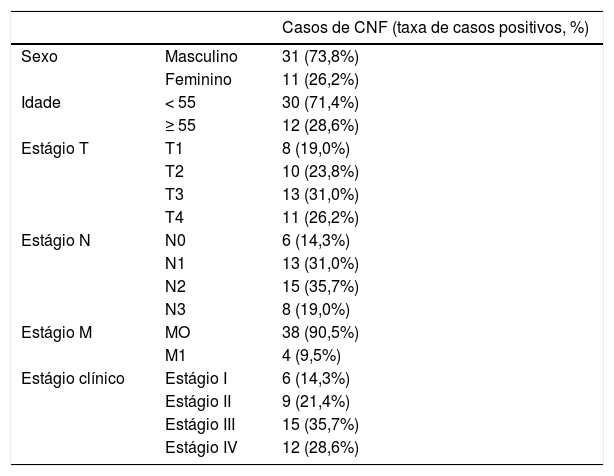
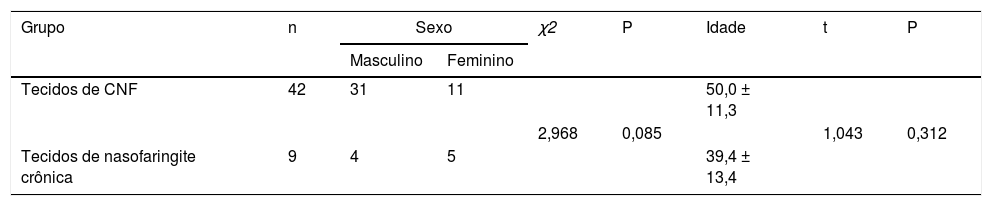
Imuno‐histoquímicaQuarenta e duas amostras de tecido embebidas em parafina de CNF e nove amostras de tecido de nasofaringite crônica foram obtidas do Departamento de Otorrinolaringologia do Zhujiang Hospital. Os dados clinicopatológicos são apresentados nas tabelas 1 e 2. A expressão de SGK3 nas amostras foi analisada através de imuno‐histoquímica com o kit de detecção de duas fases Elivision (Kit‐0015; Fuzhou Maixin Biotech. Co., Ltd., China). Essas amostras foram desparafinizadas e pré‐tratadas ao ferver as lâminas em solução tampão citrato (pH 6.0) por 10min. As amostras foram então imersas em peróxido de hidrogênio a 3% por 10min à temperatura ambiente para bloquear a atividade da peroxidase endógena tecidual. Após a lavagem com solução salina tamponada com fosfato (PBS), as amostras foram incubadas com anticorpo policlonal de coelho SGK3 (catálogo n° ab153981; 1: 200; Abcam Company, EUA) a 4°C durante a noite e então as amostras foram incubadas com 50μL de polímero amplificador (reagente A) e 50μL de IgG anticamundongo/coelho conjugado com peroxidade de horseradish (reagente B) durante 30min à temperatura ambiente. Após a lavagem com PBS, as amostras foram coradas com solução cromogênica de diaminobenzidina (DAB) e contrastadas com hematoxilina, diferenciadas com ácido clorídrico em etanol, coradas em azul pela lavagem com água e seladas com resina convencional.17 Os resultados foram avaliados pelo método HSCORE, que incluiu tanto a intensidade quanto o escore de distribuição da coloração específica, avaliados por dois patologistas de forma independente.18 Os escores de distribuição da expressão de SGK3 foram registrados como porcentagens de células coradas positivamente em cada uma das quatro categorias de intensidade, que foram classificadas como 0 (sem coloração), 1 (coloração fraca), 2 (coloração acentuada) e 3 (coloração forte). O HSCORE de cada tecido foi derivado pela soma dos quatro escores de distribuição (D) de cada categoria multiplicados pelos escores de intensidade (i) como mostrado a seguir: HSCORE = ∑D (i), onde D variou de 0% a 100% e i = 0, 1, 2, ou 3. O HSCORE máximo foi 300 e o mínimo foi 0. Um HSCORE = 75 foi usado como o ponto de corte para distinguir entre a expressão positiva e a negativa.
Características clínico‐patológicas de pacientes e tecidos de CNF
| Casos de CNF (taxa de casos positivos, %) | ||
|---|---|---|
| Sexo | Masculino | 31 (73,8%) |
| Feminino | 11 (26,2%) | |
| Idade | < 55 | 30 (71,4%) |
| ≥ 55 | 12 (28,6%) | |
| Estágio T | T1 | 8 (19,0%) |
| T2 | 10 (23,8%) | |
| T3 | 13 (31,0%) | |
| T4 | 11 (26,2%) | |
| Estágio N | N0 | 6 (14,3%) |
| N1 | 13 (31,0%) | |
| N2 | 15 (35,7%) | |
| N3 | 8 (19,0%) | |
| Estágio M | MO | 38 (90,5%) |
| M1 | 4 (9,5%) | |
| Estágio clínico | Estágio I | 6 (14,3%) |
| Estágio II | 9 (21,4%) | |
| Estágio III | 15 (35,7%) | |
| Estágio IV | 12 (28,6%) |
Este estudo foi aprovado pelo comitê de ética (n° 2016‐EBYHK‐002).
Análise do Western blotAs proteínas totais foram extraídas de células com tampão de lise RIPA (Kaiji Biotechnology Co., Ltd., Jiangsu, China). As concentrações de proteína foram determinadas com ensaios de proteína (Beyotime Biotechnology Co., Ltd., Xangai, China). As proteínas purificadas (50μL) foram separadas por eletroforese em gel de poliacrilamida com dodecil sulfato de sódio (SDS‐PAGE) e transferidas para membranas de difluoreto de polivinilideno (Millipore, Bedford, MA, EUA). As membranas foram bloqueadas durante 2 horas à temperatura ambiente em leite desnatado a 5% e incubadas durante a noite a 4°C com anticorpo anti‐SGK3 (Abcam Company, 1:1000). Após a incubação com Horseradish Peroxidase (HRP), anticorpo secundário ligado (Biosharp Biotechnology Co., Ltd., Hefei, China) (1:5000), as membranas foram lavadas e as proteínas foram visualizadas com ‐se um kit de quimiluminescência melhorado (PerkinElmer Inc., Waltham, MA, EUA). Os resultados do Western blot foram analisados semiquantitativamente com o software Image Pro Plus.19
Transfecção de plasmídeos e triagemAs células CNE‐2 de fase logarítmica foram semeadas em placas de seis poços durante 24 horas antes da transfecção atingir 80%‐90% de confluência. As células em cada poço foram transfectadas com 4μg de shRNA SGK3 ou plasmídeo CN e 10μL de Lipofectamina 2000 (Invitrogen, Life Technologies Inc., Carlsbad, Califórnia, EUA). Células não tratadas foram usadas como controle. Todas as células foram cultivadas a 37°C por 24 horas. Após determinar o sucesso da transfecção de acordo com o grau de proteína fluorescente verde (GFP, do inglês Green Fluorescent Protein) por microscopia de fluorescência, as células foram cultivadas por mais 48 horas e colhidas para análise de Western blot para identificar o plasmídeo com o maior efeito sobre o knockdown de SGK3.20 As células tratadas foram colhidas para experimentos subsequentes. As células transfectadas com sucesso com o plasmídeo shRNA do SGK3 ou CN foram chamadas de grupo shSGK3 ou CN, respectivamente. As células CNE‐2 serviram como controle branco (grupo controle). Todos os experimentos in vitro foram feitos para cada grupo.
Ensaio da taxa de crescimentoAs células CNE‐2 nos três grupos foram cultivadas em placas de 96 poços (5.000 células/poço em 5 poços). O crescimento celular foi avaliado com um ensaio de MTT (brometo de [3‐(4,5‐dimetiltiazol‐2‐il)‐2,5‐difeniltetrazólio) com uma placa conduzida nos pontos temporais indicados durante três dias consecutivos. Cada poço continha 20μL de reagente MTT e foi então cultivado a 37°C por 4 horas. O meio foi descartado e os cristais que se formaram foram dissolvidos em 150μL de dimetil‐sulfóxido (DMSO). As células viáveis em cada poço foram determinadas a cada dia através da medida de um comprimento de onda de absorbância de 490nm. Cada experimento foi repetido de forma independente por três vezes. As curvas de crescimento celular foram subsequentemente geradas.20
Análise do ciclo celularAs células CNE‐2 nos três grupos foram semeadas em placas de seis poços (50.000 células/poço) e cultivadas por 48 horas. No fim da incubação, todas as células foram tripsinizadas, lavadas duas vezes com solução salina pré‐resfriada tamponada com fosfato (PBS, HyClone, Logan, UT, EUA), coletadas e ressuspensas em 100μL de tampão de ligação. Em seguida, 5μL de anexina V‐APC e 5μL de PI foram adicionados e as placas foram incubadas por 30 minutos no escuro à temperatura ambiente. As células foram imediatamente examinadas por citometria de fluxo. Os dados foram analisados pelo software ModFit LT 2.0.21
Testes de raspagemAs células CNE‐2 foram adicionadas a placas de seis poços (50.000 células/poço). Uma vez que as células cresceram até aproximadamente 100% de confluência, os testes de foram feitos com uma ponta de pipeta estéril de 200μL para raspar a monocamada confluente. A área raspada foi lavada com PBS até as células separadas serem removidas. Adicionou‐se meio isento de soro e as células foram cultivadas a 37°C. A distância entre as células na área raspada em 0, 24 e 48 horas foi medida por microscopia.22 A migração celular horizontal foi analisada através do software Image J e calculada com a seguinte fórmula: mobilidade relativa = 1 (largura imediata da raspagem/ largura da raspagem original).
Análise estatísticaA avaliação estatística foi feita no programa SPSS 22.0 ou Graph Pad Prism 6. Todos os dados foram adquiridos de pelo menos três experimentos independentes e os resultados são apresentados como média ± desvio padrão. Análise de variância (Anova) de um fator e testes t de Student foram usados para comparar as diferenças de médias entre os grupos.
A associação da expressão de SGK3 com as características clínicas em CNF foi avaliada por análise de regressão logística. Um valor de p < 0,05 indicou uma diferença significante.
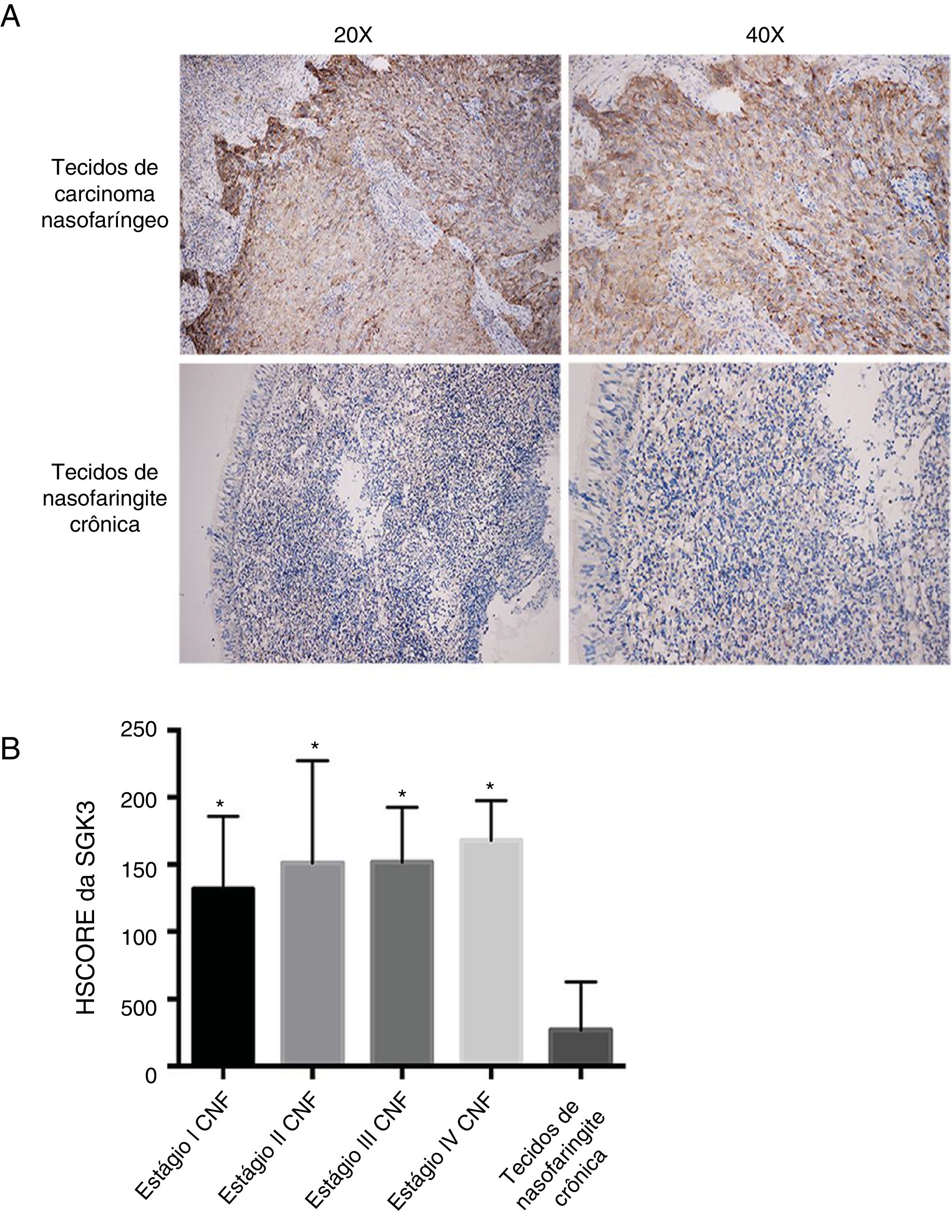
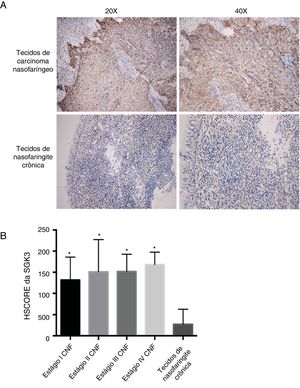
ResultadosExpressão de SGK3 em tecidos de CNFA figura 1A mostra a expressão da proteína SGK3 nos tecidos. As taxas de expressão positiva de SGK3 nos tecidos de CNF e nos tecidos de nasofaringite crônica foram 90,50% (38/42) e 11,10% (1/9), respectivamente. A taxa de expressão de SGK3 em diferentes fases de CNF e nos tecidos de nasofaringite crônica foi avaliada de acordo com o HSCORE.
Coloração imuno‐histoquímica representativa da SGK3 em tecidos de CNF. (A) Os resultados imuno‐histoquímicos mostraram que a expressão da proteína SGK3 estava localizada principalmente no citoplasma, com expressão fortemente positiva de SGK3 em tecidos de câncer de CNF e sem expressão ou expressão fraca em tecidos de nasofaringite crônica. (B) Taxa de expressão da SGK3 em diferentes estágios de CNF e tecidos de nasofaringite crônica de acordo com o HSCORE. A expressão da SGK3 nos tecidos de CNF de estágio I, II, III e IV foi significativamente maior do que nos tecidos de nasofaringite crônica (p < 0,01). No entanto, não houve diferença significativa entre os diferentes estágios do CNF (p > 0,05).
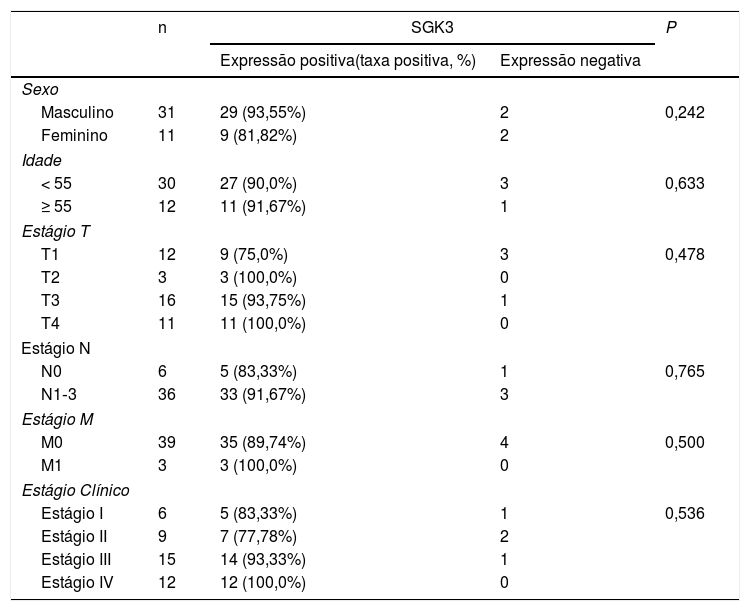
O nível de expressão da SGK3 foi significantemente maior em CNF do que na nasofaringite crônica (p < 0,01) (fig. 1B), indicou que a expressão da SGK3 está relacionada à carcinogênese do CNF. Entretanto, a expressão de SGK3 não foi correlacionada com sexo, idade, estágio TNM ou estágio clínico (p > 0,05) (tabela 3).
Correlação da expressão de SGK3 em tecidos de CNF (n = 42)
| n | SGK3 | P | ||
|---|---|---|---|---|
| Expressão positiva(taxa positiva, %) | Expressão negativa | |||
| Sexo | ||||
| Masculino | 31 | 29 (93,55%) | 2 | 0,242 |
| Feminino | 11 | 9 (81,82%) | 2 | |
| Idade | ||||
| < 55 | 30 | 27 (90,0%) | 3 | 0,633 |
| ≥ 55 | 12 | 11 (91,67%) | 1 | |
| Estágio T | ||||
| T1 | 12 | 9 (75,0%) | 3 | 0,478 |
| T2 | 3 | 3 (100,0%) | 0 | |
| T3 | 16 | 15 (93,75%) | 1 | |
| T4 | 11 | 11 (100,0%) | 0 | |
| Estágio N | ||||
| N0 | 6 | 5 (83,33%) | 1 | 0,765 |
| N1‐3 | 36 | 33 (91,67%) | 3 | |
| Estágio M | ||||
| M0 | 39 | 35 (89,74%) | 4 | 0,500 |
| M1 | 3 | 3 (100,0%) | 0 | |
| Estágio Clínico | ||||
| Estágio I | 6 | 5 (83,33%) | 1 | 0,536 |
| Estágio II | 9 | 7 (77,78%) | 2 | |
| Estágio III | 15 | 14 (93,33%) | 1 | |
| Estágio IV | 12 | 12 (100,0%) | 0 | |
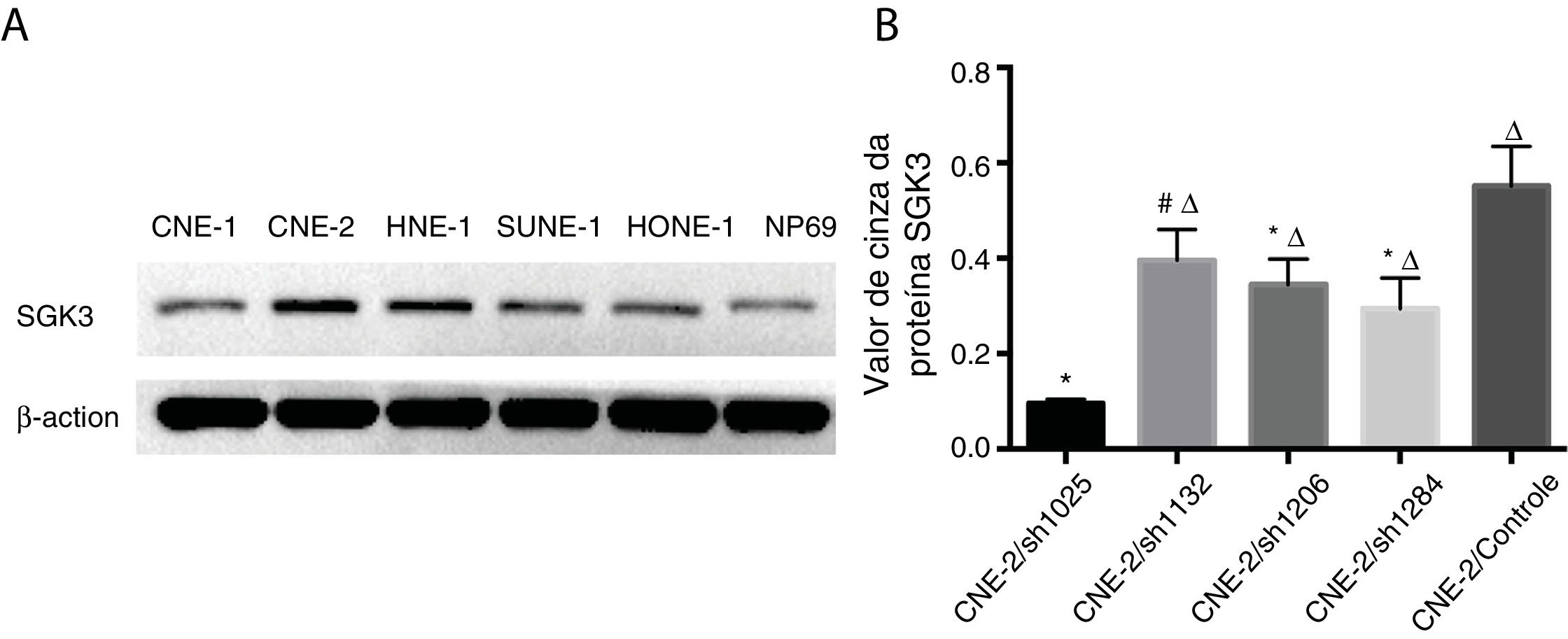
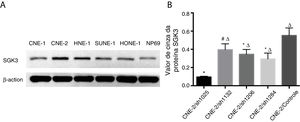
A expressão da proteína SGK3 em diferentes linhagens celulares de CNF e células NP69 é mostrada na figura 2. A SGK3 foi mais altamente expressa na maioria das células de CNF (CNE‐2, HNE‐1, SUNE‐1) do que em células NP69 (p < 0,01). Além disso, as células CNE‐2 e HNE‐1 exibiram níveis mais altos de expressão de SGK3 do que outras linhagens de células de CNF (p < 0,01). Os resultados da análise de Western blot foram consistentes com os da análise imuno‐histoquímica. Esses resultados também indicaram que o SGK3 pode estar intimamente relacionado ao desenvolvimento de CNF.
Detecção da expressão da proteína SGK3 em linhagens de células de CNF. (A) Expressão representativa da proteína SGK3 em diferentes linhagens celulares de CNF e células NP69 detectadas por análise de Western blot. (B) Análise do valor de cinza da expressão da proteína SGK3 como a proporção entre a SGK3 e a p‐actina nos resultados de Western blot; a SGK3 foi mais altamente expressa na maioria das linhagens de células de CNF (CNE‐2, HNE‐1, SUNE‐1) do que nas células NP69 (p < 0,01).
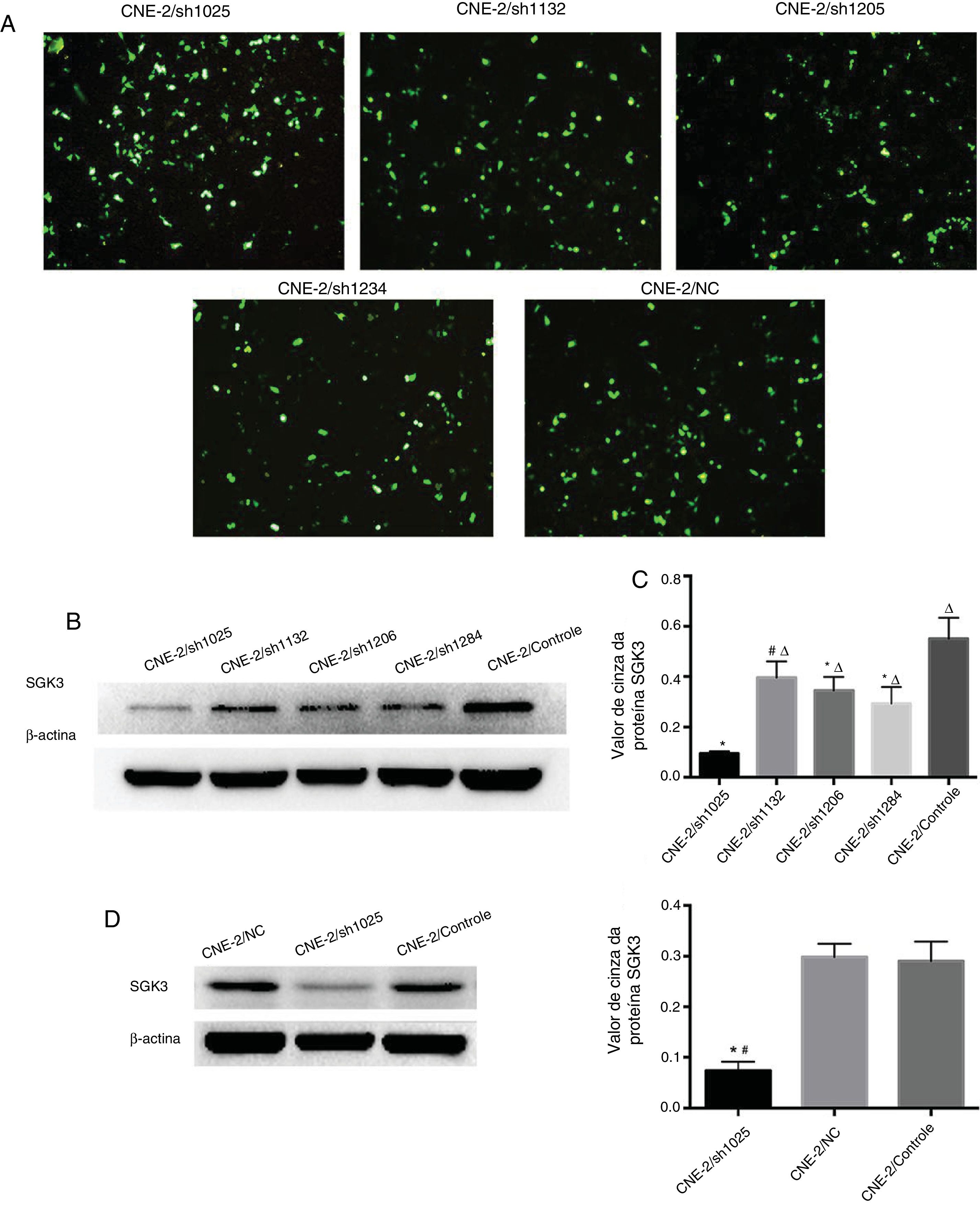
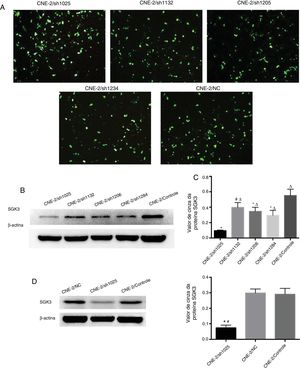
Os plasmídeos SGK3 shRNA e NC foram transfectados com sucesso para as células CNE‐2 (fig. 3A). Os resultados de triagem do plasmídeo shRNA mais eficaz que teve como alvo a SGK3 (shSGK3) são apresentados na figura 3B, que mostra que a proteína SGK3 foi notavelmente reduzida no grupo sh1025 em comparação com os outros grupos de plasmídeo e controle (p < 0,01) (fig. 3B e C). O plasmídeo sh1025 teve o efeito mais significativo no knockdown de SGK3; portanto, as células do grupo sh1025 foram chamadas de grupo hSGK3 e usadas em experiências subsequentes. Os resultados do Western blot mostraram que o nível da proteína SGK3 foi acentuadamente reduzido no grupo shSGK3 em comparação com o grupo CN e controle (p < 0,01) (fig. 3D e E) e nenhuma diferença significativa na expressão de SGK3 foi observada entre o grupo CN e o grupo de controle.
Melhor rastreamento de shRNA da SGK3 e eficiência do silenciamento da SGK3 pelo shRNA específico em células CNE‐2. (A) Expressão verde fluorescente da proteína em células CNE‐2 observada por microscopia de fluorescência após transfecção com o shRNA da SGK3 ou plasmídeo NC. (B) Expressão representativa da proteína SGK3 em células CNE‐2 tratadas com diferentes plasmídeos de shRNA da SGK3 determinadas por análise de Western blot. (C) Análise do valor de cinza de expressão da proteína SGK3 como a proporção entre a SGK3 e a p‐actina em resultados de Western blot. O plasmídeo sh1025 mostrou o efeito mais significativo no knockdown da SGK3 (p < 0,01). (D) Expressão representativa da proteína SGK3 nos grupos shSGK3, NC e controle determinados por análise de Western blot. (E) Análise do valor cinza da expressão da proteína SGK3 como a proporção entre a SGK3 e a β‐actina nos resultados de Western blot; a expressão da SGK3 no grupo shSGK3 foi obviamente reduzida em comparação com a dos grupos NC e controle (*#p < 0,01).
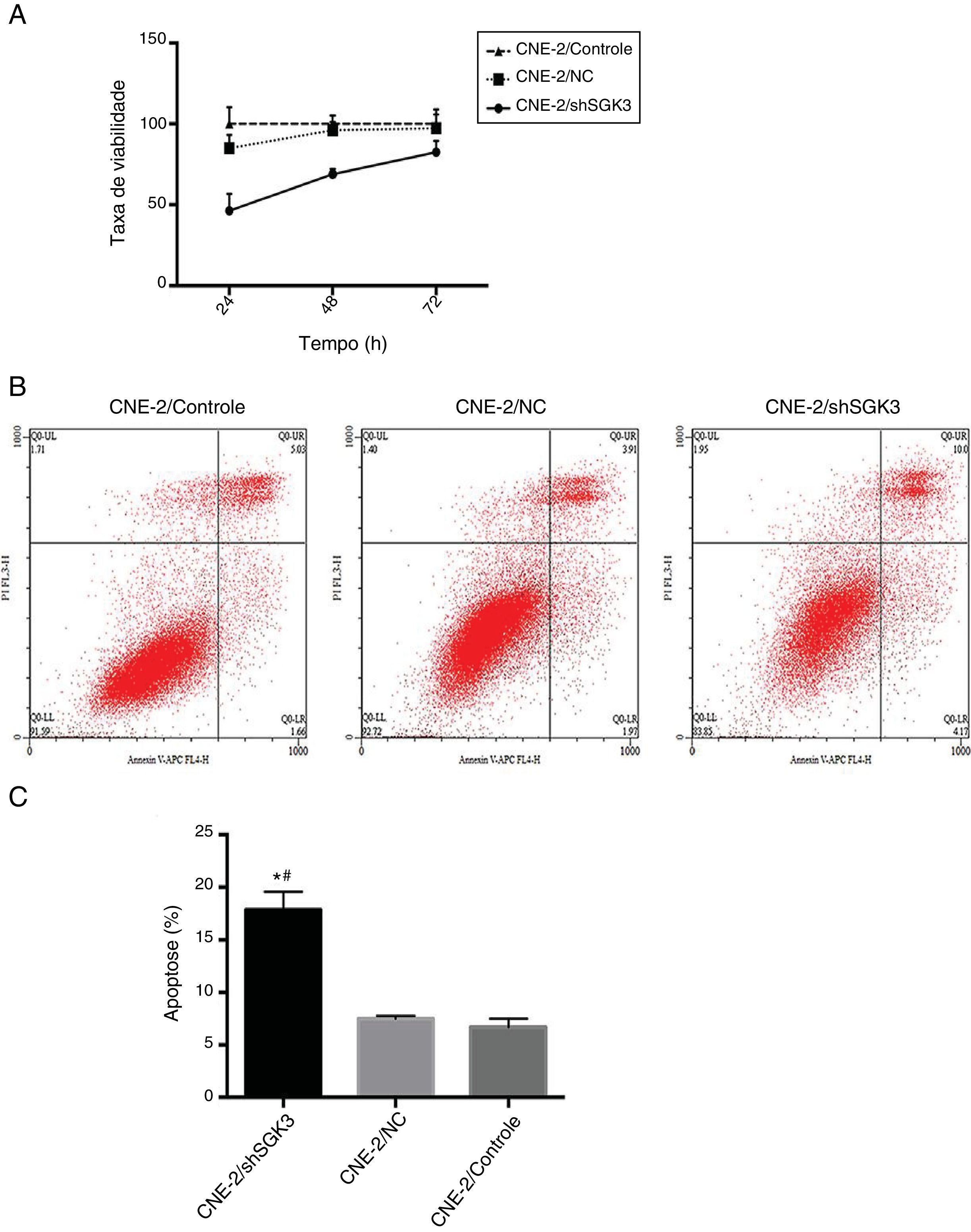
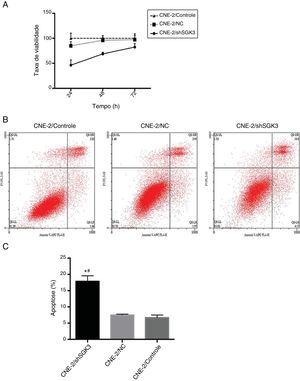
Para confirmar o efeito de inibição celular de shRNA SGK3, seus efeitos citotóxicos foram avaliados. A figura 4A mostra uma falha de toxicidade no grupo CN e óbvia citotoxicidade no grupo shSGK3 às 24, 48 e 72 horas (p < 0,01).
Efeito da down‐regulação da SGK3 na capacidade proliferativa e apoptose de células CNE‐2. Ensaio MTT (A) e análise de apoptose (B e C) por citometria de fluxo nos diferentes grupos. A taxa de viabilidade celular no grupo shSGK3 estava obviamente reduzida em comparação com a dos grupos NC e controle e a taxa de apoptose celular no grupo shSGK3 estava obviamente aumentada em comparação com a dos grupos NC e controle. (*#p < 0,01).
Para determinar se shRNA SGK3 poderia efetivamente induzir a apoptose celular, determinamos a porcentagem de apoptose celular após as células CNE‐2 terem sido transfectadas com shRNA SGK3. Como mostrado na figura 4B, as células CNE‐2 exibiram apoptose limitada no grupo CN em comparação com o grupo controle, o que foi consistente com os resultados da análise de citotoxicidade. As porcentagens de apoptose celular (inclusive apoptose precoce e tardia) no grupo shSGK3, no grupo NC e no grupo controle após 48 horas foram de 17,85%, 7,49% e 6,70%, respectivamente. As células tratadas com shRNA SGK3 exibiram um aumento mais óbvio na apoptose (p < 0,01) (fig. 4C).
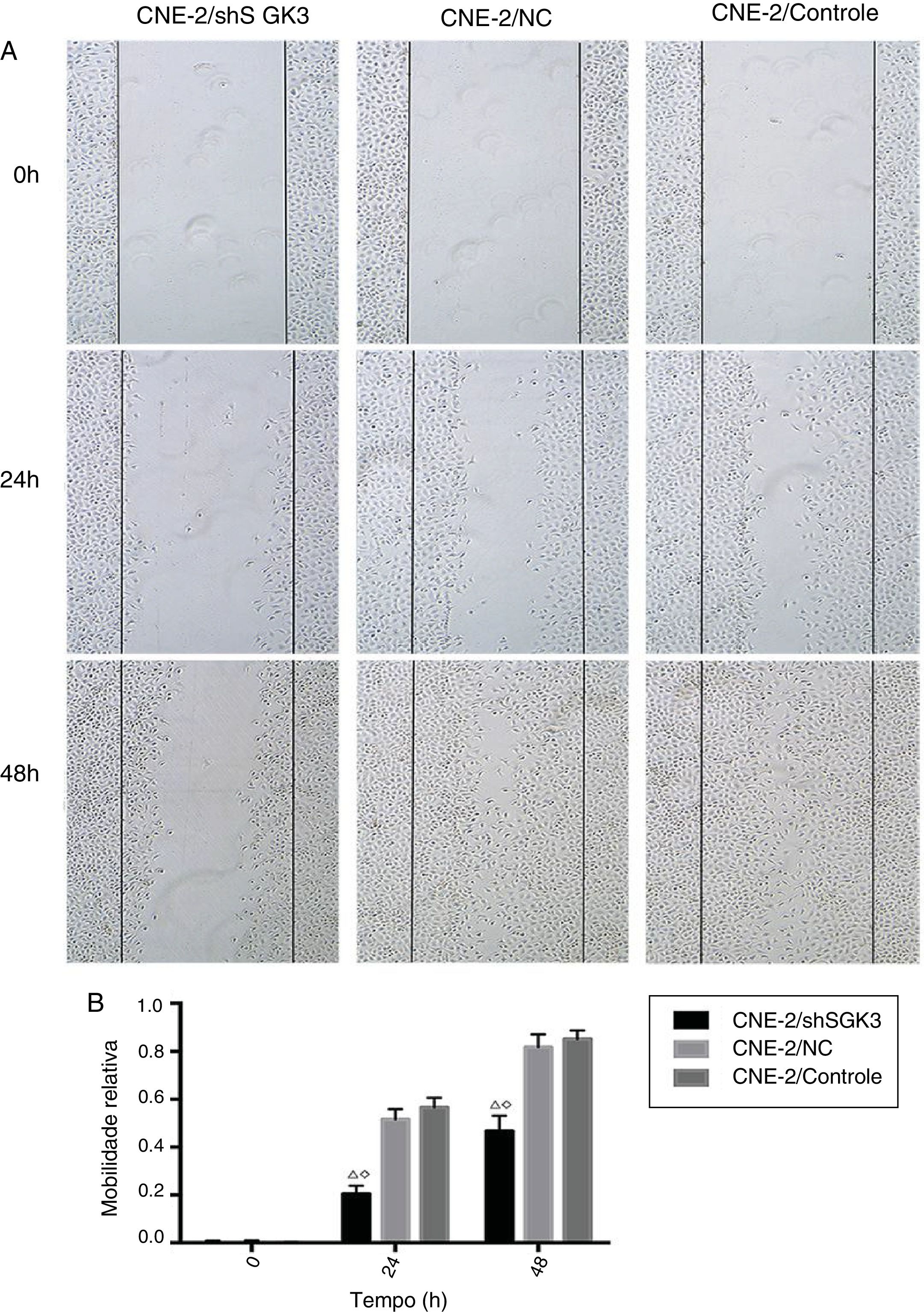
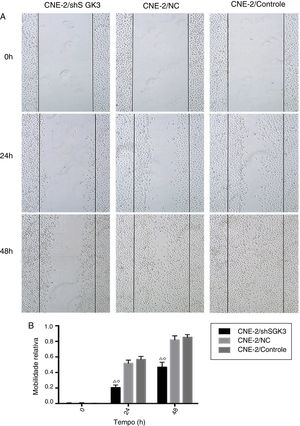
Teste de raspagem celularPara detectar a capacidade de invasão e metástase das células tumorais, o teste de raspagem celular foi feito no grupo controle, no grupo CN e no grupo shSGK3. Como mostrado na figura 5A, a taxa de migração horizontal de células no grupo shSGK3 após 24 horas foi de 20,50%, enquanto essas taxas foram de 51,60% e 56,60% no grupo CN e controle, respectivamente. Após 48 horas, as células do grupo shSGK3 ainda não haviam se recuperado do dano. A taxa de migração celular horizontal foi de 46,70%, mas os arranhões no grupo CN e no grupo controle eram pouco visíveis. Esses resultados sugerem que a capacidade migratória das células tratadas com shSGK3 foi obviamente diminuída em comparação com a do grupo CN e do grupo controle (p < 0,01) (fig. 5B).
O efeito da down‐regulação da SGK3 na motilidade das células CNE‐2. (A) Distância em diferentes momentos após o teste da raspagem (ampliação original: X 5). As distâncias das raspagens no grupo shSGK3 não mudaram de maneira óbvia após 24 horas, enquanto as células nos grupos NC e controle exibiram taxas de migração mais altas (p < 0,01). Após 48 horas, as células do grupo shSGK3 ainda não haviam se recuperado do dano (p < 0,01), mas as raspagens celulares dos grupos NC e controle dificilmente eram visíveis. (B) Comparação das taxas de migração celular em diferentes momentos pelo teste de arranhadura; as taxas de migração celular no grupo shSGK3 foram maiores do que as dos grupos NC e controle após 24 e 48 horas (△◊p < 0,01).
O desenvolvimento e a progressão dos tumores são processos biológicos complexos que envolvem vários genes e vias moleculares. A ativação anormal da via PI3K/AKT e seus alvos downstream foi observada em uma ampla variedade de malignidades humanas, inclusive o CNF.23–25 A SGK3 é uma serina/treonina quinase que funciona downstream de PI3K, compartilha sua similaridade funcional e de sequência com a família AKT e desempenha um papel crítico na sinalização oncogênica independente de AKT.26 Embora muitos estudos mostrem que o SGK3 desempenha um papel importante na regulação da proliferação e migração celular,27–31 as funções do SGK3 no CNF humano permanecem desconhecidas.
Liu M observou que a sobre‐expressão de SGK3 estava significativamente associada a um prognóstico ruim e era mais comum do que a sobre‐expressão de AKT em carcinoma hepatocelular.32 Além disso, Xu J estudou a expressão de SGK3 em 1.340 tumores de mama humanos e descobriu que o SGK3 desempenha um papel importante na sinalização oncogênica independente de AKT.33 Outro estudo mostrou que apenas 36% de ativação de SGK3 foram detectados em um painel de amostras de tumor ovariano, apresentaram baixos níveis de AKT fosforilada, mas com altos níveis de PIK3CA, um gene codificador da subunidade alfa P110 na classe I PI3‐K, e nenhuma correlação foi encontrada entre a fosforilação de SGK3 e a sobre‐expressão de PIK3CA fosforilada ou ativação de AKT.34
No estudo, também encontramos maior expressão de SGK3 em células e tecidos de CNF humanos e a expressão de SGK3 não se correlacionou com sexo, idade, estágio TNM ou estágio clínico. A expressão de SGK3 não se correlacionou de maneira significativa com o prognóstico do CNF, sugeriu que o SGK3 provavelmente não está implicado na sinalização oncogênica aberrante de PI3‐K. No entanto, o número de amostras em nosso estudo não foi suficiente; maiores coortes de pacientes em estudos futuros são necessárias para esclarecer o papel da SGK3 na sinalização oncogênica aberrante de PI3‐K.
Como descrito acima, a SGK3 desempenha um papel importante na regulação da proliferação e migração de células cancerígenas. Pesquisas demonstraram que a Di‐hidrotestosterona (DHT) pode fazer a up‐regulação da expressão de SGK3 via receptor de andrógeno (RA) e promover a proliferação de células de câncer de próstata.35 Sun X descobriu que a sobre‐expressão de SGK3 podia promover a proliferação, sobrevivência, invasão e migração de células de câncer de mama.36 Um experimento funcional in vitro mostrou que a sobre‐expressão da SGK3 podia promover o crescimento celular, a clonogenicidade e o crescimento independente de ancoragem no carcinoma hepatocelular.32 Em contraste, o knockdown da SGK3 poderia inibir significativamente esses processos celulares. Além disso, o estudo também verificou que a sobre‐expressão de SGK3 em células de carcinoma hepatocelular aumentou significativamente a formação e progressão tumoral em camundongos nude em comparação com o uso de células de controle de vetor vazio.
Devido aos altos níveis de expressão de SGK3 nos tecidos e células de CNF, e às funções de SGK3 no processo celular, exploramos ainda mais os efeitos de SGK3 em células de CNF. Silenciamos com sucesso a expressão de SGK3 em células de CNF. Os resultados da transfecção foram verificados por análise de Western blot de diferentes grupos de células. Os ensaios de taxa de crescimento revelaram que as células do grupo shSGK3 apresentavam taxas de proliferação mais baixas na mesma fase logarítmica dos grupos CN e controle. Além disso, as células SGK3 silenciadas apresentavam maiores taxas de apoptose do que as células CN e grupo controle. Além disso, os testes de raspagem verificaram que as células do CNF no grupo shSGK3 eram menos resistentes a danos externos e sua capacidade migratória estava obviamente diminuída. Esses resultados indicam que a expressão de SGK3 exógena pode alterar o comportamento das células de CNF e melhorar significativamente a multiplicação e invasão de células de CNF.
ConclusãoNosso estudo demonstra que SGK3 apresenta uma sobre‐expressão em células e tecidos de CNF humano e que o silenciamento de SGK3 poderia suprimir a proliferação, sobrevivência e migração de células de CNF. Ele indicou que SGK3 pode contribuir para a patogênese do CNF. SGK3 pode ser um marcador potencial e um alvo terapêutico eficaz no CNF humano.
FinanciamentoFundação Nacional de Ciências Naturais da China (n° 81573000, 81260406 e 51573071).
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Chen J, Li HL, Li BB, Li W, Ma D, Li YH, et al. Serum‐ and glucocorticoid‐inducible kinase 3 is a potential oncogene in nasopharyngeal carcinoma. Br J Otorhinolaryngol. 2018. https://doi.org/10.1016/j.bjorl.2018.05.012
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.