O edema e a equimose no pós‐operatório da cirurgia plástica facial constituem um problema preocupante para pacientes e cirurgiões. Considera‐se que a administração de corticosteroides diminua o período de recuperação e reduza essas complicações. Os dados sobre a eficácia da administração de corticosteroides permanecem controversos entre os cirurgiões.
ObjetivoFizemos essa revisão sistemática e metanálise para determinar o efeito da administração de corticosteroides nos períodos pré‐ e pós‐operatório sobre as complicações pós‐operatórias em pacientes submetidos à cirurgia reconstrutiva facial apoiada em diferentes análises de subgrupos.
MétodoFoi feita uma busca abrangente de artigos nos bancos de dados PubMed, Cochrane Central, Scopus e Ebsco até outubro de 2019. Incluímos todos os ensaios clínicos cujos pacientes foram submetidos a qualquer tipo de cirurgia plástica facial para estudar o efeito dos corticosteroides nas complicações pós‐operatórias. Fizemos a análise de subgrupos de acordo com os tipos e as doses de preparação de corticosteroides, além de uma análise de subgrupos de uso de corticosteroides pré ou pós‐operatório. Todas as análises estatísticas foram feitas no software RevMan.
ResultadosDezenove estudos foram incluídos nesta revisão sistemática, mas apenas 10 deles foram elegíveis para a metanálise. Os escores de edema periorbital e equimoses reduziram significantemente no grupo de corticosteroides em comparação com o placebo: ‐0,82, IC95% (‐1,37, ‐0,26) e ‐0,95, IC95% (‐1,32, ‐0,57), respectivamente. Essas diferenças significantes não se mantiveram nos dias 3 e 7. Doses menores de corticosteroides (8mg e 10mg) foram associadas a menores diferenças no escore médio de edema e equimoses palpebrais superiores e inferiores, enquanto as doses mais altas foram associadas a diferenças maiores. Além disso, o corticosteroide pré‐operatório reduziu significantemente o sangramento intraoperatório quando comparado ao placebo para doses maiores > 50mg por dia (p < 0,0001), mas não para 8mg de corticosteroide (p = 0,06). O uso de corticosteroides no pós‐ e pré‐operatório foi associado a uma diminuição maior de edema e equimoses do que no pré‐operatório isoladamente.
ConclusãoEsta metanálise abrangente confirma um benefício estatisticamente significante do uso de corticosteroides no pré‐operatório. Além disso, a manutenção dos esteroides no pós‐operatório está associada à redução das complicações em longo prazo. Doses mais altas de corticosteroides estão associadas a uma redução mais significativa no edema e nas equimoses, mas estudos adicionais são recomendados para determinar os efeitos colaterais pós‐operatórios como infecção do sítio cirúrgico e atraso na cicatrização.
As cirurgias plásticas faciais são uma das cirurgias mais feitas no mundo todo. A cirurgia facial inclui muitos tipos de procedimentos cirúrgicos, como o lifting facial, a rinoplastia e a cirurgia plástica maxilofacial.1–3 Entretanto, edema, equimose e sangramento intraoperatório são as complicações pós‐operatórias mais comuns após essas cirurgias.4
A gravidade do edema e das equimoses é a preocupação mais importante, pois pode atrasar o processo de cicatrização dos tecidos envolvidos e alterar o resultado estético final esperado.5 Vários métodos e conceitos com resultados de sucesso variáveis foram desenvolvidos para evitar essas condições.6
Acredita‐se que a administração de corticosteroides diminua o período de recuperação e reduza o edema e a equimose no pós‐operatório.7 Eles têm propriedades anti‐inflamatórias, inibem o processo inicial de inflamação que envolve a migração de linfócitos, deposição de fibrina, dilatação capilar e atividade fagocítica.8 Entretanto, alguns estudos relatam que a administração pré‐operatória de esteroides é eficaz, enquanto o mesmo não é verdade para a administração pós‐operatória.6,9
Os dados referentes à eficácia da administração de corticosteroides permanecem controversos entre os cirurgiões, com um debate sobre os benefícios em longo prazo da administração de corticosteroides no intra‐ ou pós‐operatório em pacientes submetidos à cirurgia plástica facial.10–12 Na maioria desses estudos, várias doses e vias de administração foram usadas. Griffies et al. foram os primeiros a investigar o efeito dos corticosteroides no edema e equimose da cirurgia plástica facial através de um estudo clínico prospectivo randomizado.13 Eles relataram que um bolus único de 10mg de dexametasona podia diminuir significantemente o inchaço facial quando comparado ao placebo. Em 1991, Hoffmann et al. avaliaram o uso de 10mg de dexametasona no pré e pós‐operatório e verificaram uma redução significativa no edema palpebral pós‐operatório, para edema intranasal e equimose.14 Por outro lado, Berinstein et al.15 concluíram que os pacientes submetidos a rinoplastia que receberam dexametasona apresentaram aumento do edema pós‐operatório quando comparados aos controles; avaliados por ressonância magnética.
Tuncel et al. em 2013 relataram que 10mg de dexametasona no pré e pós‐operatório com hipotensão controlada reduziram consideravelmente o edema pós‐operatório e a equimose da rinoplastia, bem como o sangramento intraoperatório.16 O estudo feito na Turquia por Gurlek et al. demonstrou que os esteroides (betametasona 8mg, dexametasona 8mg e metilprednisolona 40mg) não foram eficazes na prevenção ou redução de edema e equimoses após rinoplastia aberta com osteotomias, sem diferenças nos níveis de equimoses ou edema observados entre o grupo que recebeu esteroides, o grupo que recebeu tenoxicam e o grupo placebo.2
Recentemente, em 2018, Sanober et al. mostraram que o uso de 8mg de dexametasona no pré‐operatório diminuiu o edema periorbital em 50%, em comparação com 33,3% do grupo placebo. No 7° dia de pós‐operatório, apenas 3,3% no grupo de dexametasona apresentaram edema de grau III em comparação com 13,3% no grupo placebo.
Considerando o quão comuns e importantes são os procedimentos de cirurgia facial, fizemos esta revisão sistemática e metanálise para resolver as conclusões conflitantes relatadas anteriormente e determinar o efeito dos corticosteroides administrados nos períodos pré e pós‐operatório nas complicações pós‐operatórias em pacientes submetidos à cirurgia reconstrutiva facial.
MétodoFizemos todas as etapas desta revisão sistemática em estrita conformidade com o Cochrane Handbook for Systematic Reviews of Interventions.17 Também seguimos o método PRISMA (Preferred Reporting Items for Systematic Reviews and Meta‐Analyses) durante a redação do manuscrito.18
Estratégia de pesquisa de literaturaFizemos a pesquisa nos seguintes bancos de dados eletrônicos médicos: PubMed, Cochrane Central, Scopus e Ebsco até outubro de 2019, com os seguintes termos de busca: “(MeSH Facial surgery OR face or facial or nasal dorsum or nose or mouth or ears or lips]” AND “MeSH [Surgery, Plastic] OR [plastic next surgery or craniofacial surgery]” AND “[corticosteroid or glucocorticoid or steroid or dexamethasone or Metilprednisolona])”. Também pesquisamos a bibliografia de estudos elegíveis para encontrar artigos relevantes.
Critérios de elegibilidade e seleção de estudosForam incluídos todos os ensaios clínicos prospectivos (comparativos, não comparativos, randomizados ou não randomizados) que atendiam a todos os seguintes critérios: a) Pacientes incluídos que foram submetidos a qualquer tipo de cirurgia plástica facial; b) Estudos em que a intervenção de interesse foi a administração de corticosteroides, comparada ou não a outra intervenção ou placebo.
Excluímos: a) Estudos observacionais; b) Estudos com amostra pequena (menos de dez pacientes); c) Estudos feitos em modelos de animais; d) Revisões, relatos de casos, resumos de conferências ou séries de casos; e e) Artigos não escritos em inglês e referências duplicadas.
A triagem de elegibilidade foi feita em duas etapas, cada uma por dois revisores independentes (Saud Abdalwahab Aldhabaan e Jibril Yahya Hudise): a) Triagem de título e resumo para corresponder aos critérios de inclusão e b) Triagem de texto completo para elegibilidade para a metanálise. Os desacordos foram resolvidos através da opinião de um terceiro revisor (Amani Obeid).
Extração de dadosDois revisores independentes (Saud Abdalwahab Aldhabaan e Amani Obeid) extraíram os dados e outro revisor (Jibril Yahya Hudise) resolveu as divergências. Os dados extraídos incluíram o seguinte: a) Características gerais de cada estudo, inclusive; local do estudo, desenho do estudo, tamanho da amostra, tipo de intervenção e doses, tipo de comparador; b) características gerais dos pacientes de cada estudo, inclusive: idade, sexo, etnia; c) Características da cirurgia, inclusive: tipo de cirurgia, duração da cirurgia, período de seguimento e avaliação do edema; d) Resultados de interesse, inclusive inchaço (edema), hematomas (equimoses), sangramento intraoperatório e e) Critérios de risco de viés.
Avaliação do risco de viésPara avaliar o risco de viés no ensaio clínico incluído, dois revisores independentes (Saud Abdalwahab Aldhabaan e Jibril Yahya Hudise) usaram a ferramenta de avaliação de risco de viés Cochrane (ROB) para o ensaio clínico randomizado, claramente descrito no (capítulo 8.5) do Cochrane Handbook for Systematic Reviews of Interventions 5.1.0.17,18
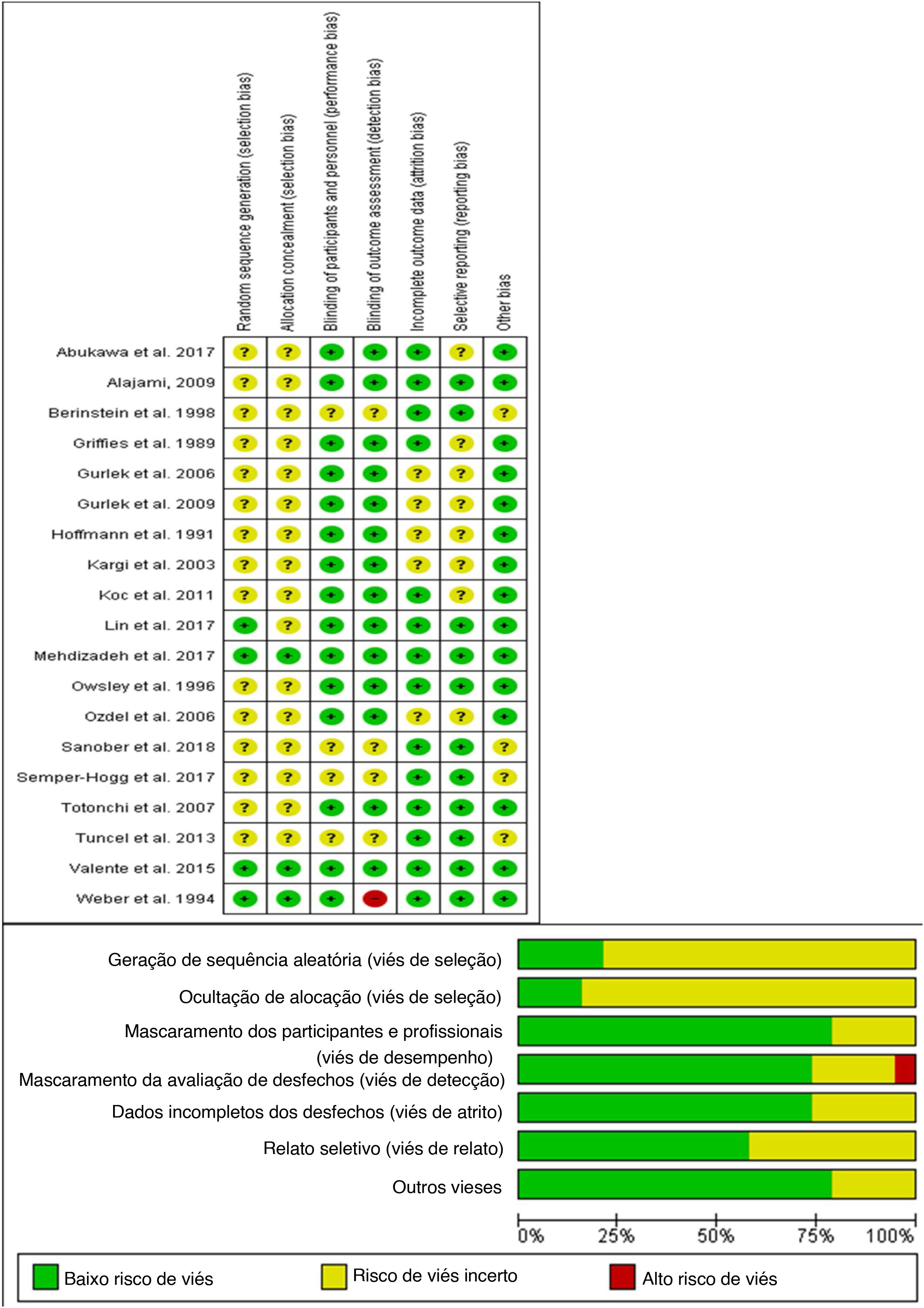
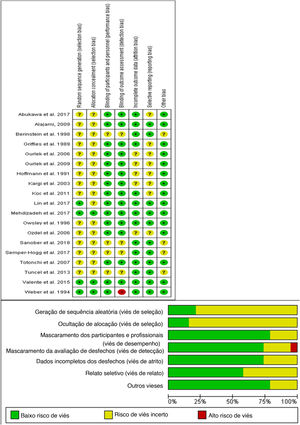
A ferramenta de avaliação de risco de viés da Cochrane inclui os seguintes domínios: Geração de sequência aleatória (viés de seleção); Ocultação de alocação (viés de seleção); Mascaramento dos participantes e profissionais (viés de desempenho); Mascaramento da avaliação de desfechos (viés de detecção); Dados incompletos dos desfechos (viés de atrito); Relato seletivo (viés de relato) e outras fontes potenciais de viés. O julgamento dos autores é classificado como de “baixo risco”, “alto risco” ou “risco incerto” de viés.
Síntese dos dadosCalculamos a média da diferença (MD) e os intervalos de confiança de 95% (IC95%), se os resultados fossem medidos da mesma maneira entre os ensaios. A diferença média padronizada (DMP) foi calculada no caso de diferença no sistema de escore.
Em alguns estudos, extraímos os dados dos gráficos com o software PlotDigitizer.19 No caso de falta de desvios‐padrão (DP), usamos os valores de p disponíveis e a calculadora disponível no software Revman para determinar o DP; se não fosse possível calcular, usávamos o maior DP relatado do estudo mais semelhante para cada resultado.
Gurlek et al., 20062 compararam três corticosteroides diferentes (betametasona, dexametasona e metilprednisolona) com placebo. Para um estudo como esse, os dados relacionados a cada esteroide versus placebo foram incluídos na metanálise como uma entrada separada designada pelo nome do estudo, seguida por uma letra maiúscula (A, B ou C).
Testamos a heterogeneidade entre os estudos incluídos pelos testes do qui‐quadrado e quantificamos sua extensão pelo teste do I‐quadrado. Na ausência de heterogeneidade clínica e estatística (I2 < 50%), o modelo de efeito fixo foi aplicado aos dados do pool de dados. Na presença de heterogeneidade estatística (I2 >50%), foi aplicado o modelo de efeitos aleatórios para metanálise. Todas as análises estatísticas foram feitas no software RevMan (versão 5.3) para Windows.
Análise de subgruposFizemos uma análise de subgrupos de acordo com os tipos e doses de preparação de corticosteroides, além de uma análise de subgrupos de uso de corticosteroides nos períodos pré‐ ou pós‐operatório.
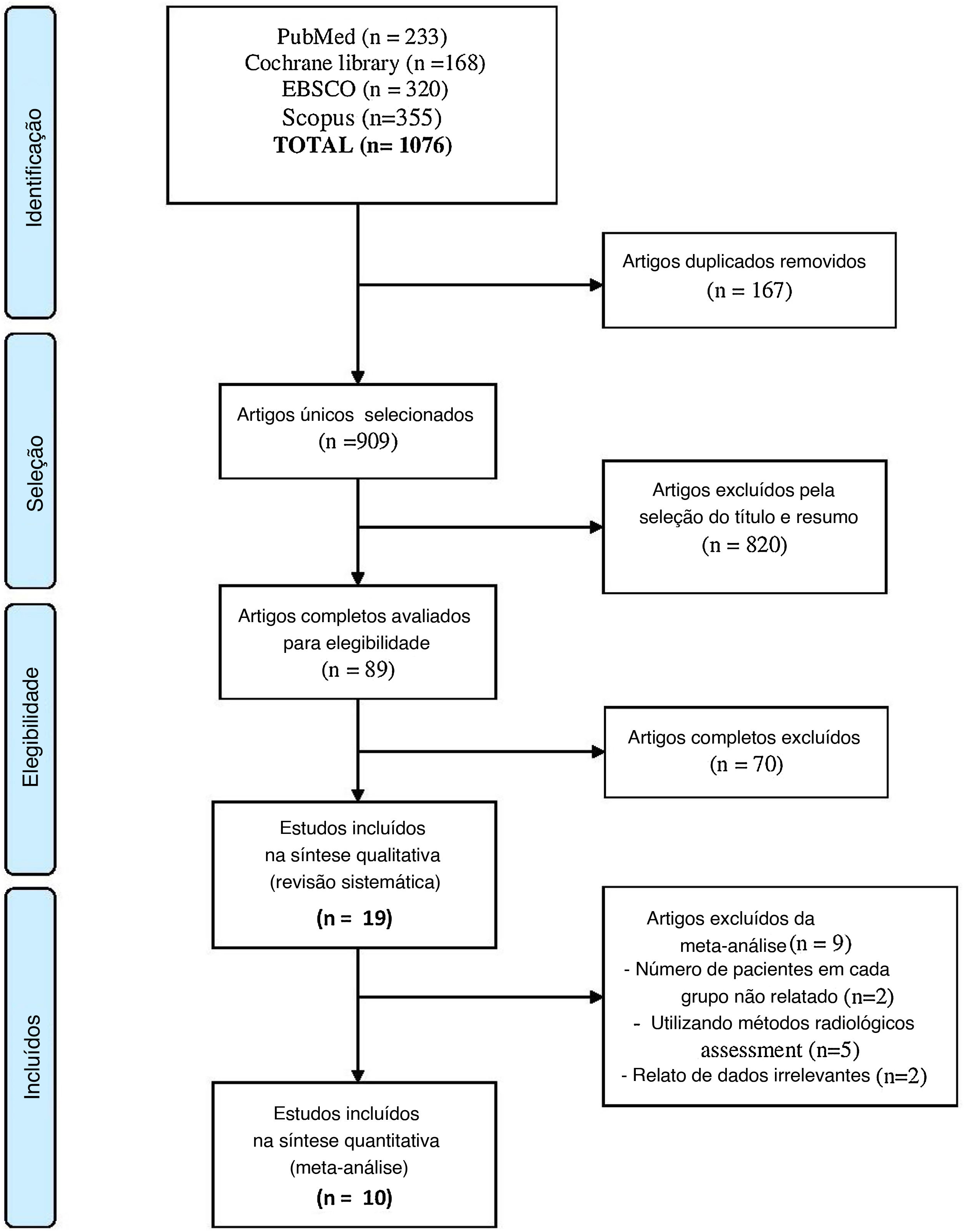
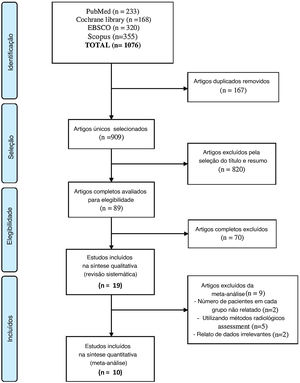
ResultadosBusca na literaturaNossa busca resultou na identificação de 1.076 estudos. Após a triagem e exclusão de duplicatas, permaneceram 89, que foram incluídos na triagem de texto completo. Finalmente, 192–4,13–16,20–30 foram incluídos nesta revisão sistemática, mas apenas 10 foram elegíveis para a metanálise2–4,13,14,16,20,21,29,30 conforme relatado no diagrama de fluxo PRISMA (fig. 1).
Avaliação de risco de viésRelatamos um baixo risco geral de viés de acordo com a ferramenta de avaliação ROB. O resumo da avaliação de risco de viés é relatado na figura 2. A maioria dos estudos incluídos não tinha informação clara sobre a geração da sequência aleatória e a alocação do paciente. Todos os estudos incluídos foram duplo‐cegos, exceto um, que era triplo‐cego.30 Todos os estudos incluídos relataram edema e equimose em diferentes dias no pós‐operatório.
Análise qualitativa de dadosResumimos as características basais de 19 estudos incluídos na tabela 1. Deles, 18 estudos eram estudos prospectivos randomizados controlados e apenas um estudo foi um ensaio clínico retrospectivo.16 Foram incluídos nesta revisão sistemática 843 pacientes com uma média de 30 a 60 por estudo. Identificamos uma diferença significante no corticosteroide usado em relação ao tipo e dose.
Características basais e resumo dos estudos incluídos, como relatado em cada estudo
| ID do Estudo | Local | Desenho do estudo | Tamanho da amostra | IntervençãoDose peri/intraoperatória | Dose pós‐operatória | Controle | Idade, ano | Sexo | Tipo de cirurgia | Duração da cirurgia, minutos | Medida de desfecho (edema e equimose) | Consultas de seguimento | Achados |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Estudos incluídos na metanálise | |||||||||||||
| Griffies et al., 1989 | EUA | Estudo prospectivo, randomizado, duplo‐cego | 30 | Pré‐operatório imediato: Dexametasona 10mg IV | Não | Placebo (solução salina) | Mediana (intervalo), 23 (18–45) | Homens 23 (76,7%), Mulheres 7 (23,3%) | Rinoplastia com osteotomia | NR | A equimose e edema periorbital foram avaliados separadamente utilizando‐se uma escala graduada de 4 pontos | Day 1 | Edema e equimose foram significantemente reduzidos no grupo que recebeu esteroides. |
| Gurlek et al., 2006 | Turquia | Estudo prospectivo, randomizado, controlado por placebo, duplo‐cego | 40 | Pré‐operatório imediato: betametasona 8mg (Grupo 1), dexametasona 8mg (Grupo 2), metilprednisolona 40mg (Grupo 3), tenoxicam 20mg (Grupo 4) | Pós‐op: mesmo que o peri‐op. ×3 dias | Placebo (Grupo 5) | Intervalo; 22–30 | NR | Rinoplastia aberta com osteotomia | NR | Foram tiradas fotografias digitais de cada paciente e o escore foi feito separadamente para edema palpebral e equimose, utilizando uma escala graduada de 0 a 4. | Dias 1, 3, e 7 | Não foram observadas diferenças nos níveis de equimose ou edema entre o grupo que recebeu esteroides, o grupo tenoxicam e o grupo controle. Os esteroides utilizados nessas doses não foram eficazes na prevenção ou redução de edema e equimoses após rinoplastia aberta com osteotomias. |
| Gurlek et al., 2009 | Turquia | Estudo prospectivo, randomizado, controlado por placebo, duplo‐cego | 40 | Pré‐operatório imediato: dose única de metilprednisolona 250mg (grupo 1), dose única de 500mg de metilprednisolona (Grupo 2), 4 doses de 250mg de metilprednisolona (Grupo 3),4 doses de metilprednisolona 5000mg (Grupo 4) | Nos grupos (3 e 4), 250 e 500mg por dia × 3 dias | Placebo | Média 24,5 (intervalo 19–35) | Homens 26 (76,7%), Mulheres 14 (23,3%) | Rinoplastia aberta com osteotomia | NR | Foram tiradas fotografias digitais de cada paciente e o escore foi feito separadamente para edema palpebral e equimose, utilizando uma escala graduada de 0 a 4. | Dias 1, 3 e 7 | Observou‐se diferença clínica e estatisticamente significante em relação à equimose e edema entre o grupo placebo e o grupo com altas doses de metilprednisolona. |
| Hoffmann et al., 1991 | EUA | Estudo prospectivo, randomizado, controlado por placebo, duplo‐cego | 49 | Intra‐op: Dexametasona 10 mg IV | Pós‐op:redução gradual em 5 dias, de 50mg de prednisona 10mg por dia | Placebo | Range; 15–70 | NR | Rinoplastia fechada ou aberta | NR | O edema palpebral superior e inferior e a equimose periorbital foram avaliados usando uma escala graduada de 0 a 4. O edema paranasal foi visualmente graduado de 0 a 4 e por palpação dos tecidos moles da face. O edema intranasal foi avaliado pelo exame rinoscópico anterior e avaliado em 0 a 4, determinando a quantidade de edema septal e do corneto e a patência das vias aéreas. | 1,4,7 dias | Menos edema palpebral pós‐operatório, edema para / intranasal e equimoses foram registrados em pacientes que receberam esteroides |
| Kargi et al., 2003 | Turquia | Estudo prospectivo, randomizado, controlado, duplo‐cego | 60 | 1 hora pré‐op: dose única de dexametasona, 8mg IV (Grupo 1 e 3); Pré‐operatório imediato: dexametasona, 8mg IV (Grupo 2 e 4) | Pós‐op: dexametasona 8mg IV 24, 48 horas (grupo 3 e 4); Pós‐op imediato: dexametasona 8mg IV, 24 e 48 horas (Grupo 5) | Nada (Grupo 6) | NR | NR | Rinoplastia fechada | NR | A equimose e o edema periorbitais foram avaliados separadamente usando uma escala de 4 pontos | Dias 1, 2, 5, 7, 10 | Verificou‐se que a administração de doses triplas é mais eficaz na redução de edema e equimoses durante os primeiros 5 a 7 dias. O edema e a equimose foram significantemente menores nos grupos que receberam esteroides durante os primeiros 2 dias em comparação com o grupo controle. No dia 5, o edema e a equimose foram significantemente menores nos grupos 3 e 4 em comparação com outros grupos, mas não houve diferença entre eles. O grupo 5 apresentou um nível significantemente maior de edema e equimose em comparação com os grupos 1 a 4 depois de 24 horas e nos dias 2, 5 e 7. |
| Koc et al., 2011 | Turquia | Estudo prospectivo randomizado controlado | 40 | Pré‐op: dose única de 1mg / kg de metilprednisolona IV (Grupo I), dose única de 3mg / kg de metilprednisolona IV (Grupo II) | Não | Nada | NR | Homens 22 (55%), Mulheres 18 (45%) | Rinoplastia aberta com Osteotomia | NR | O edema palpebral e a equimose dos tecidos moles periorbitais foram avaliados separadamente, utilizando uma escala de 0 a 4. | Days 1, 3, and 7 | Edema periorbital e equimose foram significantemente menores nos grupos dexametasona em comparação com o grupo controle. Não foram observadas diferenças clínica ou estatisticamente significativas na prevenção ou redução da equimose periorbital ou do edema periorbital entre os grupos I e II. |
| Mehdizadeh et al., 2017 | Irã | Estudo clínico prospectivo, randomizado, triplamente cego | 60 | Pré‐op:Grupo D (dexametasona 8 mg),Grupo T(ácido tranexâmico 10mg / kg), Grupo DT (dexametasona 8mg + ácido tranexâmico 10mg / kg) | Pós‐op:três doses a cada 8h dos tratamentos correspondentes | Nada (Grupo P) | Média 27,35± 6 | Homens 27 (45%), Mulheres 33 (55%) | Rinoplastia primária aberta | NR | Fotografias foram tiradas após a cirurgia e examinadas por um cirurgião plástico independente em relação ao edema e à equimose utilizando uma escala de 0 a 4 | Dias 1, 3, e 7 | Nos grupos ácido tranexâmico, dexametasona e ácido tranexâmico mais dexametasona, o edema e a equimose foram menores; não foi observada diferença na comparação do ácido tranexâmico, dexametasona e dexametasona mais ácido tranexâmico em qualquer dia pós‐operatório; não houve diferença na duração da cirurgia entre os grupos. |
| Owsley et al., 1996 | EUA | Estudo randomizado, duplo‐cego | 30 | Pré‐op: 500mg metilprednisolona | Pós‐op: dose oral com redução gradual de metilprednisolona por 6 dias | Nada | NR | NR | Cirurgia de lifting facial | NR | O edema facial foi avaliado por meio de fotografias frontais e oblíquas de 35mm, 3 × 5 polegadas, de todo o rosto, de todos os participantes no pré‐operatório e nos dias 1, 4 (ou 6) e 10 no pós‐operatório, em uma escala de 1 a 4) | Dias 1, 4 (ou 6), 10 | Não foram registradas diferenças significativas no edema facial entre o grupo de estudo em nenhuma ocasião |
| Ozdel et al., 2006 | Turquia | Estudo prospectivo, randomizado, duplo‐cego | 30 | Pré‐op imediato: Dexametasona 10mg IV | Não | Nada | Grupo de estudo (23,73 ± 4,58), Grupo controle (25,46 ± 8,70) | Homens 15 (50%), Mulheres 15 (50%) | Rinoplastia com remoção de corcunda nasal e osteotomias laterais bilaterais | NR | O edema e a equimose periorbital foram classificados e o bem‐estar psicológico foi medido em uma escala visual analógica padrão. O edema e a equimose das pálpebras superior e inferior foram avaliados separadamente em uma escala graduada de 0 a 4 (0 indica nenhum; 1+ média; 2+ até a pupila; 3+, além da pupila; 4+ até o canto lateral) | Dias 1, 2 | O edema periorbital foi significantemente reduzido nos 2 primeiros dias de pós‐operatório e a equimose da pálpebra superior no grupo dexametasona em comparação com o controle. A administração pré‐operatória de esteroides não teve influência na equimose da pálpebra inferior |
| Tuncel et al., 2013 | Turquia | Estudo randomizado retrospectivo | 60 | Pré‐op: dexametasona 10mg / kg IV, administrada no GrupoI (dose única), II (2 doses) e III (3 doses). | Pós‐op: (Grupo II), dexametasona 10mg / kg após 24 horas; (Grupo III), mesma dose de dexametasona imediatamente antes da osteotomia e após 24 horas | Nada (Grupo IV) | Média 29 (intervalo 23–35) | Homens 28 (46,7%), Mulheres 32 (53,3%) | Rinoplastia aberta com remoção de corcunda nasal e osteotomia bilateral | Grupo I (87,40 ± 11,65) min,Grupo II (84,67 ± 10,90) min, Grupo III (84,40 ± 11,18) min,Grupo IV (116,67 ± 14,84) min | O grau de edema palpebral e equimose dos tecidos moles periorbitais foram avaliados separadamente usando uma escala de 0 a 4.A perda de sangue intraoperatória foi registrada para cada paciente. Todos os pacientes dos grupos I, II e III foram operados sob hipotensão controlada, alcançada por infusão de remifentanil de 0,1 ± 0,5μg / kg / min, após bolus de 1μg / kg. | Dias 1, 2,5, 7, 10 | Nos três grupos de estudo, o edema palpebral e a equimose periorbital diminuíram significantemente nos dias 7, 10 em comparação com o grupo controle.Houve diferença estatisticamente significante entre o Grupo III e outros grupos nos dias 5 e 7 em relação ao edema palpebral inferior, equimoses palpebrais superior e inferior. O sangramento intra‐operatório foi mais reduzido nos grupos de estudo em comparação com o grupo controle. |
| Estudos não incluídos na metanálise | |||||||||||||
| Abukawa et al., 2017 | Japão | Estudo prospectivo, randomizado, controlado, duplo‐cego | 24 | Pré‐op: dexametasona 8mg (Grupo I), 16mg (Grupo II) | Não | Nada administrado | Grupo Controle (24,0± 6,0),Grupo I (27,3± 8,7),Grupo II (28,6± 9,7) | Homens 5 (20,8%), Mulheres 19 (79,1%) | Osteotomia Sagital Bilateral Mandibular (OSBM) | Grupo Controle (263,1 ± 34,9), Grupo I (262,0 ± 30,7), Grupo II (226 ± 30,4) | Foram registradas medidas de tomografia computadorizada da espessura do músculo masseter e tecido mole bucal, abertura incisal máxima, sensação do queixo e região do lábio inferior. Exames de sangue e tipos de complicações também foram registrados. | Dias 1, 2 e 2 anos | No grupo de 16mg, a taxa de aumento na espessura do músculo masseter foi menor que no grupo controle. Os níveis pré‐operatórios no número de linfócitos foram mantidos após a cirurgia; enquanto houve um número reduzido de linfócitos no grupo controle. |
| Alajami, 2009 | Kuwait | Estudo prospectivo, randomizado, controlado por placebo | 84 | Intra‐op: Dexametasona 10 mg | Pós‐op: dexametasona 10mg dada 12 horas após a cirurgia | Placebo (5mL solução salina) | Grupo de estudo (28,1± 5,7), Grupo Controle (28,9±6) | Homens 28 (33,3%), Mulheres 56 (66,7%) | Rinoplastia aberta com remoção de corcunda e osteotomias laterais bilaterais | NR | Os pacientes foram avaliados no pós‐operatório para a presença de edema periorbital ± equimose subconjuntival. Ausência de edema foi classificada como 0, edema isolado de pálpebra inferior foi classificado como 1, edema de pálpebras inferiores e superiores foi classificado como 2 e edema em toda a órbita se espalhando para o rosto ± equimose subconjuntival foi classificada como 3 | Dias 1, 2, 5, 7, 10 e 2ª e 3ª semanas | Dose pré‐operatória e uma dose 12 horas pós‐operatória de 10mg de dexametasona reduziram significantemente o edema periorbital pós‐operatório, administrada durante a rinoplastia em comparação ao grupo controle |
| Berinstein et al., 1998 | EUA | Estudo prospectivo, randomizado, duplo‐cego | 20 | Pré‐op: dexametasona 10 mg | Não | Nada | Variação; 18–45 | NR | Rinoplastia | Grupo Controle (Média 135 Min), Grupo de estudo (Média 120 Min) | As imagens de RM pré e pós‐operatórias foram obtidas e o edema pós‐operatório foi quantificado como a diferença na espessura dos tecidos moles (mm) entre as imagens pré e pós‐operatórias. | – | Pelo contrário, os pacientes submetidos à rinoplastia que receberam dexametasona apresentaram aumento do edema pós‐operatório quando comparados aos controles. |
| Semper‐Hogg et al., 2017 | Alemanha | Ensaio clínico controlado randomizado | 38 | Pré‐op: dose única de dexametasona 40 mg(Os pacientes envolvidos foram divididos em três subgrupos) | Não | Nada | Média 27,63 (variação 16–61) | Homens 27 (71,1%), Mulheres 11 (28.9%) | Cirurgia ortognática (osteotomia de LeFort I (subgrupo I), OSBM (subgrupo II), osteotomia bimaxilar (subgrupo III)) | Grupo I (97,16± 41,29), Grupo II (142,56±29,24), Grupo II (285± 63,56) | O edema facial pós‐operatório foi medido por meio de exames de superfície 3D e os distúrbios neurossensoriais foram investigados por estimulação térmica. | Dias 1, 2, 5, 14 e 90 | O edema facial diminuiu significantemente no grupo de estudo comparado ao grupo controle. A influência da dexametasona nos distúrbios neurossensoriais não foi significativa para o nervo alveolar inferior ou o nervo infraorbital. |
| Lin et al., 2017 | Taiwan | Estudo prospectivo, randomizado, controlado, duplo‐cego | 56 | Pré‐op imediato: dexametasona 15mg IV | Não | Pré‐op imediato: dexametasona 5mg IV (Grupo I) | Grupo Controle (20,9±4,8), Grupo de estudo (23,2±4,2). | Homens 28 (50%), Mulheres 28 (50%) | Cirurgia Ortognática | NR | O edema facial foi avaliado por imagens 3D gravadas em 5 momentos: pré‐operatório (T0) e pós‐operatório às 48 ± 6 horas (T1), 1 semana (T2), 1 mês (T3) e 6 meses (T4). O edema facial em T1, T2 e T3 e a redução do edema em T2 e T3 em comparação com a linha de base (T4) foram calculados. | 2o dia, 1a semana, 1o mês, 6o mês | O efeito de 5 e 15mg de dexametasona na redução do edema facial, bem como de náuseas e vômitos após cirurgia ortognática, não foi significantemente diferente entre os grupos de estudo. |
| Sanober et al., 2018 | Paquistão | Estudo controlado e randomizado | 60 | Pré‐op: dexametasona 8mg IV (Grupo I) | Pós‐op:Dexametasona 8 mg 4 horas após a cirurgia | Nada (Grupo II) | Média 26,48± 6,07 | Homens 14 (23,3%), Mulheres 46 (76,6%) | Rinoplastia aberta | NR | O edema periorbital foi avaliado em termos do primeiro dia de pós‐operatório e as imagens frontais foram obtidas e comparadas no seguimento no 7° dia e os escores foram medidos. | Dias 1 e 7 | Dexametasona pré‐operatória diminuiu o edema periorbital em 50%, enquanto no grupo controle em 33,3%. No geral, no grupo controle no 7° dia, 13,3% dos pacientes apresentaram edema de Grau III em comparação com 3,33% no grupo de dexametasona. |
| Totonchi et al., 2007 | EUA | Estudo controlado e randomizado | 48 | Intra‐op:Grupo P, dexametasona 10mg IV; Grupo A arnica 3x dia por 4 dias. | Grupo P: dose oral com redução gradual de metil‐prednisona por 6 dias | Nada (Grupo C) | Variação; 15–65 | Homens 11 (22,9%), Mulheres 37 (77,1%) | Rinoplastia primária com osteotomia | NR | A intensidade da equimose e a gravidade do edema foram classificadas por três panelistas cegados nos dias 2 e 8. Os panelistas avaliaram a extensão da equimose em uma escala de 0–5, a densidade de cores da equimose em uma escala de 0–4 e a gravidade do edema em uma escala de 0–3. | Dias 2 e 8 | Tanto a arnica quanto os corticosteroides reduziram o edema durante o período pós‐operatório inicial e a arnica não proporcionou nenhum benefício em relação à extensão e intensidade da equimose. Não houve diferenças significativas nas classificações de extensão e intensidade de equimoses entre os grupos no dia 2 do pós‐operatório, mas houve uma diferença significativa na classificação de edema, com o grupo C demonstrando mais inchaço em comparação com os grupos A e P. No dia 8 do pós‐operatório, o grupo P demonstrou maior extensão e maior intensidade de equimose em comparação aos gruposA e C e não houve diferenças na magnitude do edema no 8° dia pós‐operatório entre os três grupos |
| Valente et al., 2015 | Brasil | Ensaio clínico randomizado, duplo‐cego, controlado por placebo | 42 | Pré‐op: dexametasona 4 mg/mL IV | Não | Pré‐op: 2,5mL placebo (solução salina) | Média 23,12± 5,09 | Homens 3 (7,1%), Mulheres 39 (92,9%) | Rinoplastia | Média±DP (50,17± 6,62) | O edema e a equimose foram avaliados pela escala de Kara e Gökalan por 5 autores. A equimose foi avaliada de acordo com a área afetada da seguinte forma: 0 para nenhum, 1 para médio, 2 para até linha do centro da pupila, 3 para a linha do centro da pupila e 3 para a linha do centro da pupila e 4 para o canto lateral do olho. O edema foi avaliado da seguinte maneira: 0 para nenhum, 1 para mínimo, 2 até a íris, 3 até alcançar a pupila e 4 que causasse fechamento dos olhos. | Day 7 | A dexametasona reduziu significantemente as taxas de equimose e edema no pós‐operatório em comparação com os controles |
| Weber et al., 1994 | EUA | Ensaio clínico randomizado, duplo‐cego, controlado por placebo | 23 | Pré‐op imediato: dexametasona, 16mg IV (Grupo II),dexametasona, 16mg IV (Grupo III) | Pós‐op: 3 doses de placebo IV (Grupo II), 3 doses de 8mg de dexametasona IV (Grupo III) | Pré‐op imediato: dose única placebo IV, pós‐op: 3 doses de placebo IV em intervalos de 6 horas (Grupo I) | Variação; 15–49 | NR | Osteotomia Sagital Bilateral Mandibular (OSBM) | 186 minutos (Grupo I), 164 minutos (Grupo II), e 175 minutos (Grupo III) | O edema facial foi quantificado por varredura computadorizada de fotografias padronizadas obtidas de cada paciente com: a. Foram obtidos cinco conjuntos de dados fotográficos e laboratoriais para cada paciente: pré‐operatório, dia da cirurgia e pós‐operatório dias 1, 2 e 3. O processo inflamatório subjacente também foi medido utilizando proteína C‐reativa, taxa de sedimentação de eritrócitos e hemograma completo. | Dias 1, 2, e 3 | A administração de dexametasona reduziu significantemente o edema pós‐operatório somente no dia 1 pós‐operatório, quando medido fotograficamente. A proteína‐C reativa foi significantemente reduzida nos dias 1,2 e 3 no pós‐operatório nos dois grupos de dexametasona e não foi encontrada diferença significativa entre os dois grupos de dexametasona. |
NR, não relatado.
Dexametasona 8mg foi administrada em cinco estudos, enquanto a dexametasona 10mg foi administrada em sete estudos. Lin et al., 2017,25 e Semper‐Hogg et al., 2017,24 relataram o efeito de uma dose mais alta de dexametasona de 15mg e 40mg, respectivamente. Uma dose mais baixa de 4mg de dexametasona foi investigada por Valente et al., 2015.27 Gurlek et al., 2006,2 foi o único estudo que relatou o efeito da betametasona 8mg na redução do edema e equimose na rinoplastia. Eles compararam doses equivalentes de três corticosteroides diferentes (dexametasona 8mg, betametasona 8mg e metilprednisolona 40mg) com um placebo. Em 2009, Gurlek et al.3 investigaram o uso de doses mais altas de corticosteroides (metilprednisolona 250mg, 500mg e 5000mg).
Quatro estudos investigaram a metilprednisolona com doses diferentes. Onze estudos investigaram a eficácia dos corticosteroides pré e pós‐operatórios combinados, enquanto oito relataram apenas o uso pré‐operatório de corticosteroides. Quinze estudos relataram os resultados após a cirurgia de rinoplastia, dois após a cirurgia ortognática,24,25 um após osteotomia sagital bilateral mandibular22 e um após cirurgia de lifting facial.20 O resumo dos achados de cada estudo incluído são relatados na mesma tabela 1.
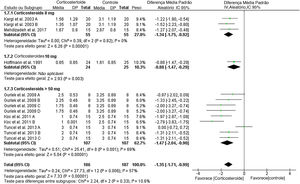
Análise quantitativa dos dadosForam incluídos na metanálise 439 pacientes de 10 ensaios clínicos. Todos esses estudos relataram a avaliação de equimose e edema palpebral superior e inferior no pós‐operatório, usaram a escala de quatro pontos. As doses mais usadas de corticosteroides foram 8mg e 10mg. As doses mais altas foram reunidas em um grupo (dose de corticosteroide > 50mg). Reunimos os resultados da equimose e edema pós‐operatórios nos dias 1, 3, 5, 7 e 10. Foram apresentados os resultados detalhados da análise de subgrupos de acordo com os tipos e doses do corticosteroide usado, bem como uma análise de subgrupos de uso de corticosteroides pré‐ e pós‐operatórios nas tabelas suplementares 1 e 2.
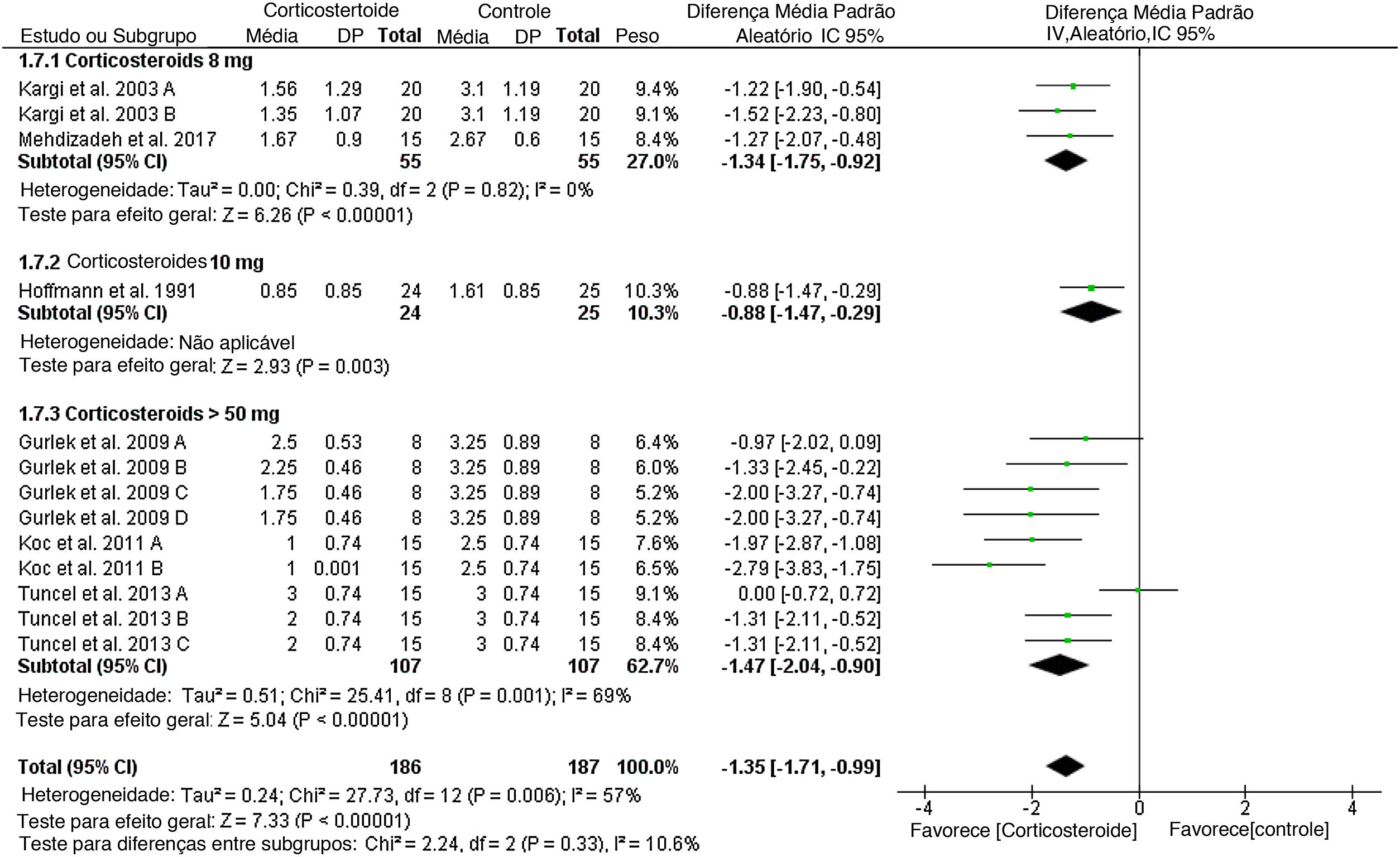
Edema da pálpebra superiorNo primeiro dia de pós‐operatório, a DMP geral favoreceu os corticosteroides e depois o placebo em termos do escore total de edema palpebral superior (DMP = ‐1,35, IC95%: ‐1,71, ‐0,99). O teste para diferenças de subgrupos entre as doses de corticosteroides de 8mg, 10mg e >50mg não foi significante, Chiy = 2,24, p = 0,33, Iy = 10,6%. Os estudos agrupados foram homogêneos para a dose de 8mg (I2 = 0%), mas heterogêneos para a dose > 50mg (I2 = 69%). A heterogeneidade foi mais bem resolvida com a exclusão do estudo de Tuncel et al. de 2013. A (dose única de 10mg/kg no grupo), Iy = 22% (fig. 3).
No 3° dia de pós‐operatório, o corticosteroide reduziu continuamente o escore do edema da pálpebra superior em comparação com o placebo (DMP = ‐1,42, IC95%: ‐1,82, ‐1,02) sem heterogeneidade (Iy = 0%), exceto o subgrupo da dose de 8mg (Iy = 87%) (fig. suplementar 1). Os mesmos resultados significantes foram obtidos no 7° dia de pós‐operatório (fig. suplementar 2). Tuncel et al. em 2013 relataram uma diferença significativa entre o uso de corticosteroide e placebo no 10° dia de pós‐operatório.
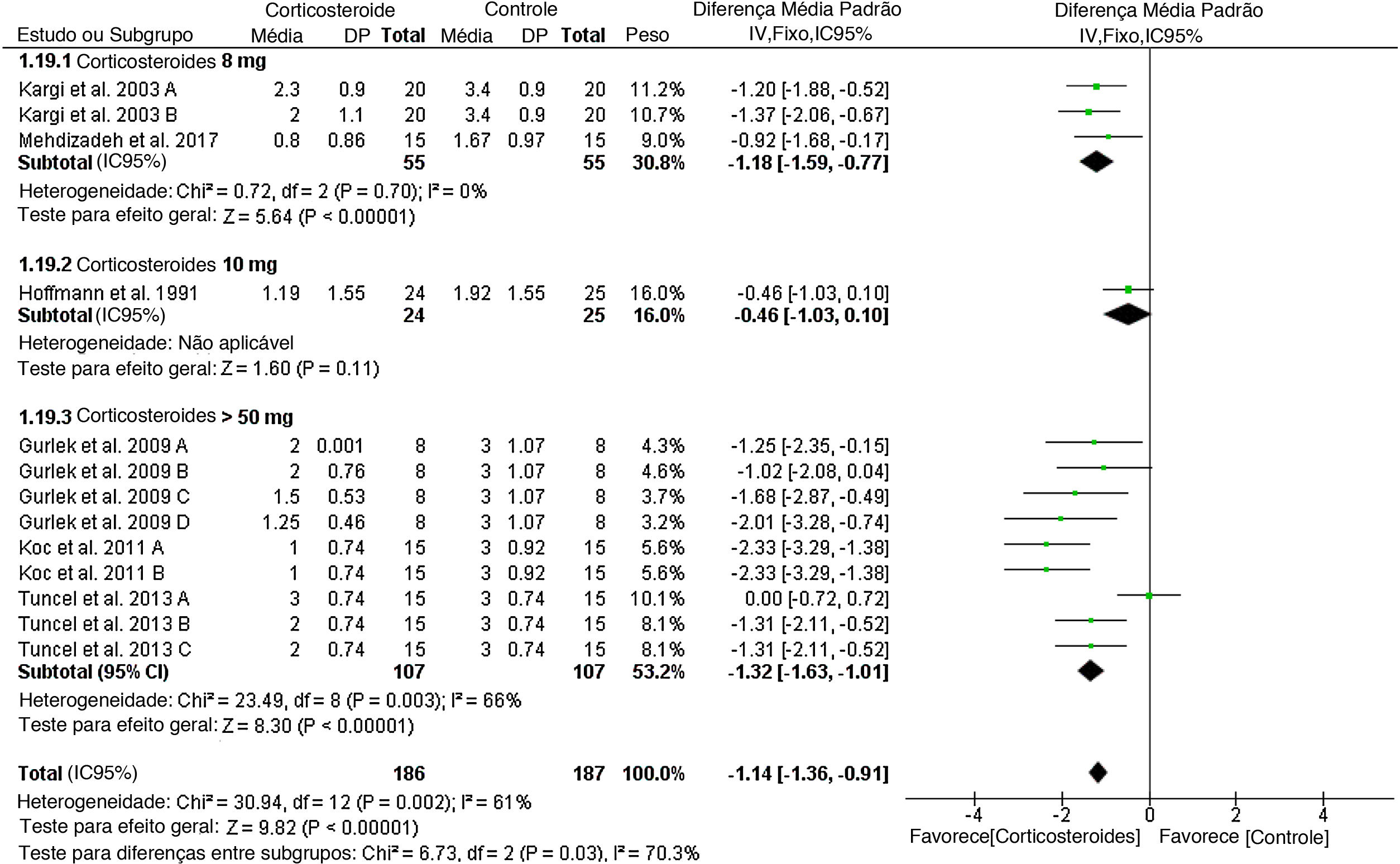
Edema de pálpebra inferiorNo 1° dia de pós‐operatório, a DMP geral favoreceu corticosteroides e, em seguida, o placebo em termos de escore total de edema da pálpebra inferior (DMP = ‐1,14, IC 95%: ‐1,36, ‐0,91). O teste para diferenças de subgrupos entre as doses de corticosteroides de 8mg, 10mg e > 50mg foi significante, Chi2 = 6,73, p = 0,03, I2 = 70,3%.
Os estudos agrupados foram homogêneos para a dose de 8mg (I2 = 0%), mas heterogêneos para a dose > 50mg (I2 = 66%). A heterogeneidade foi mais bem resolvida com a exclusão do estudo de Tuncel et al., 2013. A (dose única de 10mg/kg no grupo), I2 = 6% (fig. 4). Obtivemos a mesma significância no 3° dia; a DMP geral favoreceu os corticosteroides na dose de 8mg (DMP = ‐0,97, IC 95%: ‐1,74, ‐0,21) e > 50mg (DMP = ‐1,26, IC 95%: ‐1,66, ‐0,86). O teste para diferenças de subgrupos não foi significante: Chi2 = 0,42, p = 0,52, I2 = 0% (fig. suplementar 3). Essa diferença significante foi mantida nos dias 5, 7 e 10 do pós‐operatório, como visto nas figuras suplementares 4 a 6.
Equimose de pálpebra superiorEm comparação ao placebo, os corticosteroides reduziram significantemente o escore médio da equimose da pálpebra superior no 1° dia de pós‐operatório (DMP geral = ‐1,25, IC 95%: ‐1,71, ‐0,78). O teste para diferenças de subgrupos entre as doses de corticosteroide de 8mg, 10mg e > 50mg não foi significante, com Chiy = 0,39, p = 0,82, Iy = 0% (fig. 5). Os mesmos resultados significantes foram demonstrados para o 3°, 5°, 7° e 10° dias de pós‐operatório para a estimativa geral do efeito, conforme apresentado nas figuras suplementares 7 a 10. Tuncel et al., 2013 relataram uma diferença não significante (p = 0,32) entre corticosteroides (10mg/kg) e placebo no 5° dia de pós‐operatório.
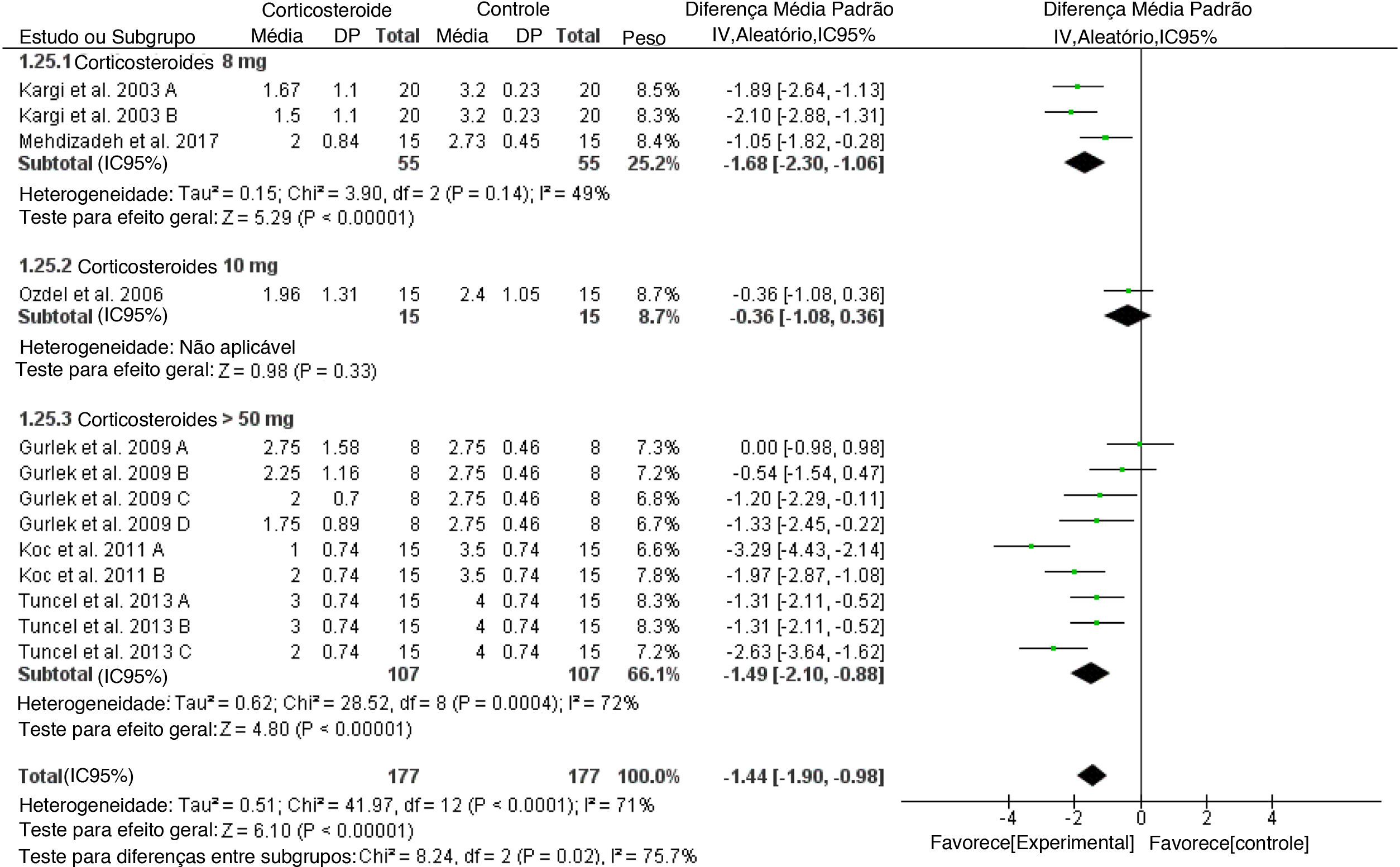
Equimose de pálpebra inferiorO escore total da equimose de pálpebra inferior diminuiu significantemente no grupo de corticosteroides em comparação com o placebo no 1° dia (DMP geral = ‐1,44, IC 95%: ‐1,90, ‐0,98). O teste para diferenças de subgrupo entre as doses de 8mg, 10mg e > 50mg de corticosteroides foi significante, com Chi2 = 8,24, p = 0,02, I2 = 75,7% (fig. 6). Os mesmos resultados significantes foram demonstrados para o 3°, 5°, 7° e 10° dias de pós‐operatório para a estimativa geral do efeito, conforme apresentado nas figuras suplementares 11‐14.
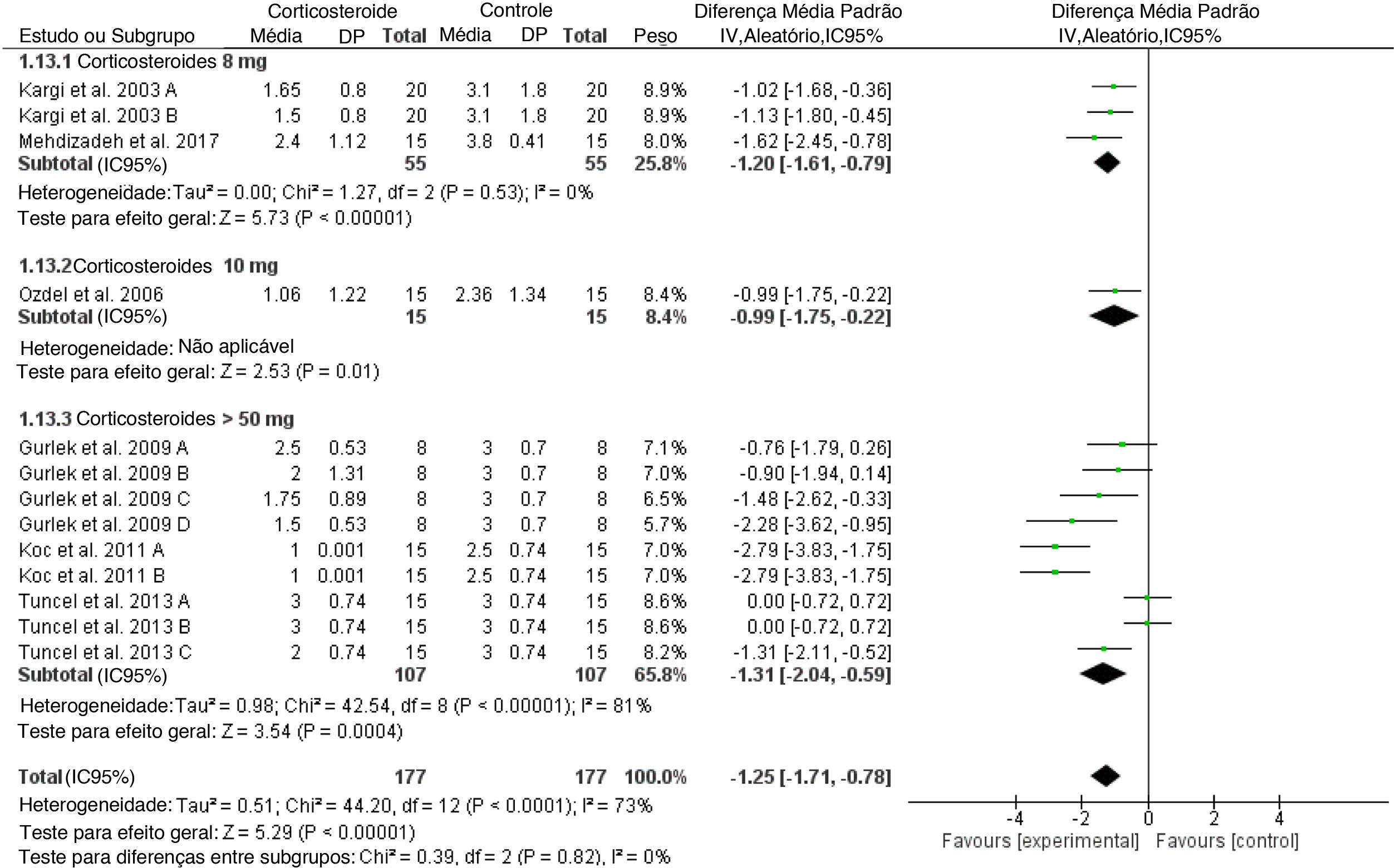
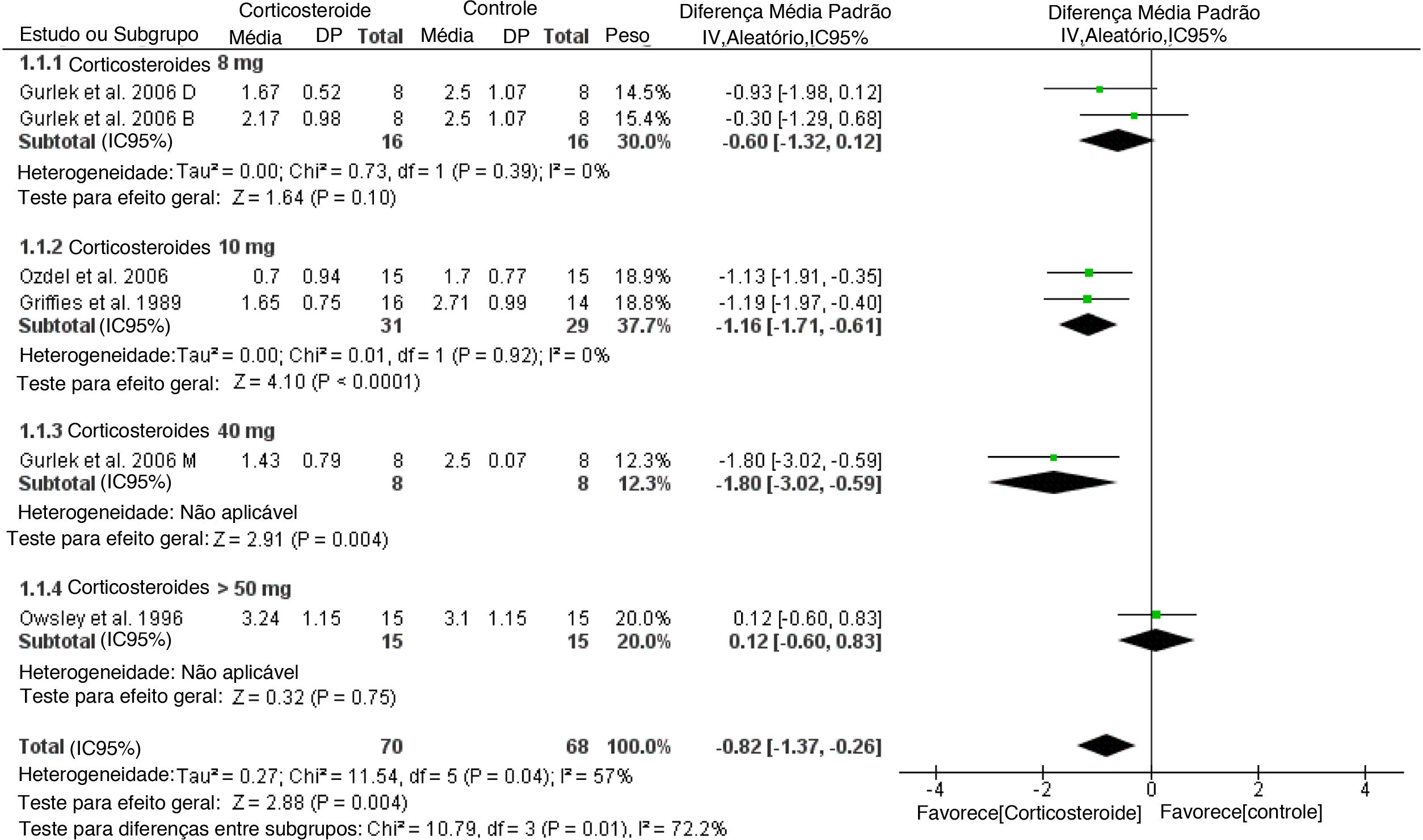
Edema inespecíficoNo primeiro dia, o tamanho geral do efeito do escore de edema revelou que o edema foi reduzido significantemente no grupo de corticosteroides em comparação ao placebo (DMP = ‐0,82, IC95%: ‐1,37, ‐0,26). Isso não foi alcançado com 8mg de corticosteroide, mas em doses mais altas, conforme apresentado na figura 7. Essa significância não foi mantida no 3° e 7° dias. (figs. suplementares 15 a 16).
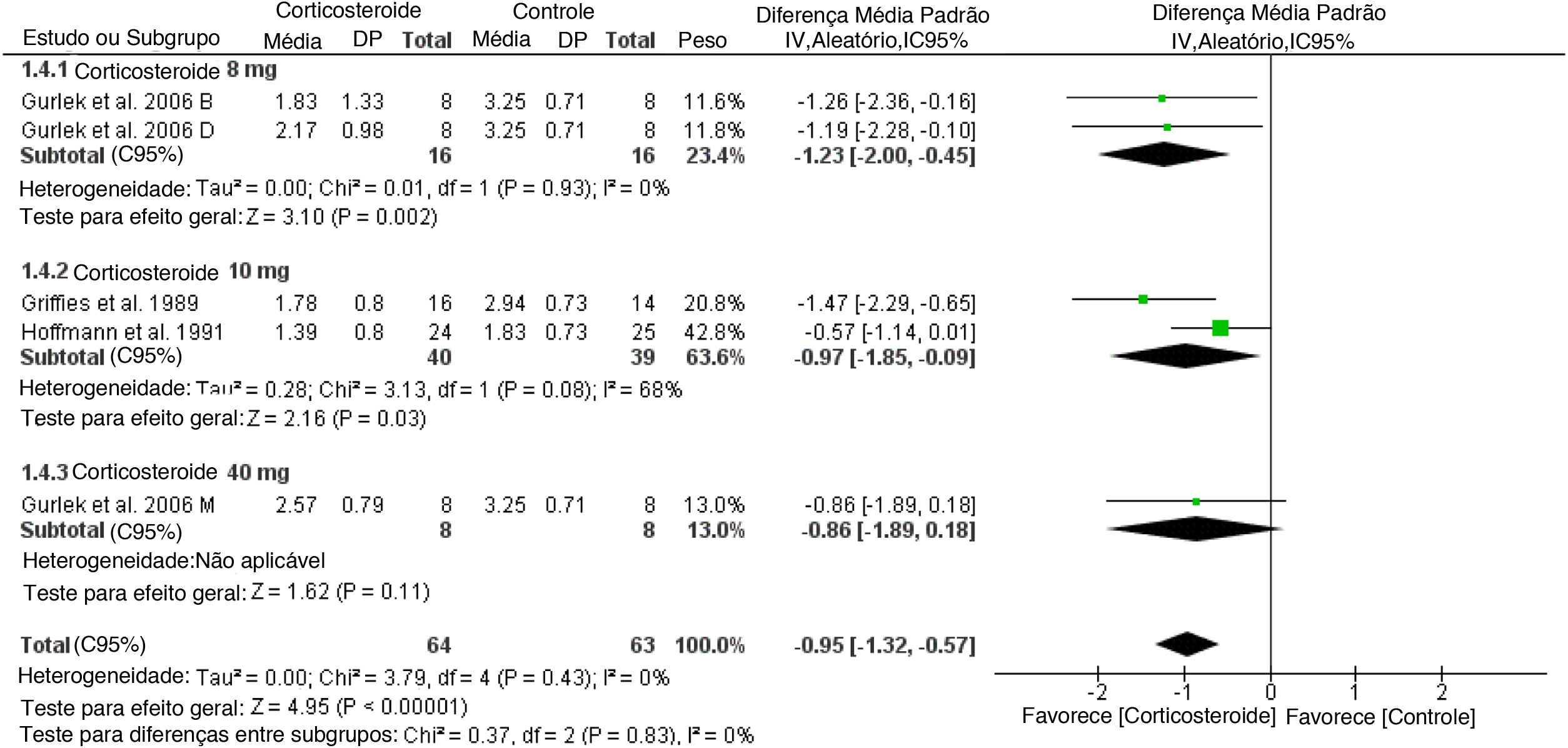
Equimose inespecíficaEm comparação com o placebo, o grupo corticosteroide reduziu a equimose pós‐operatória no primeiro dia (DMP = ‐0,95, IC 95%: ‐1,32, ‐0,57) (fig. 8), enquanto nos dias 3 e 7 os resultados não foram significantes (figs. suplementares 17 a 18).
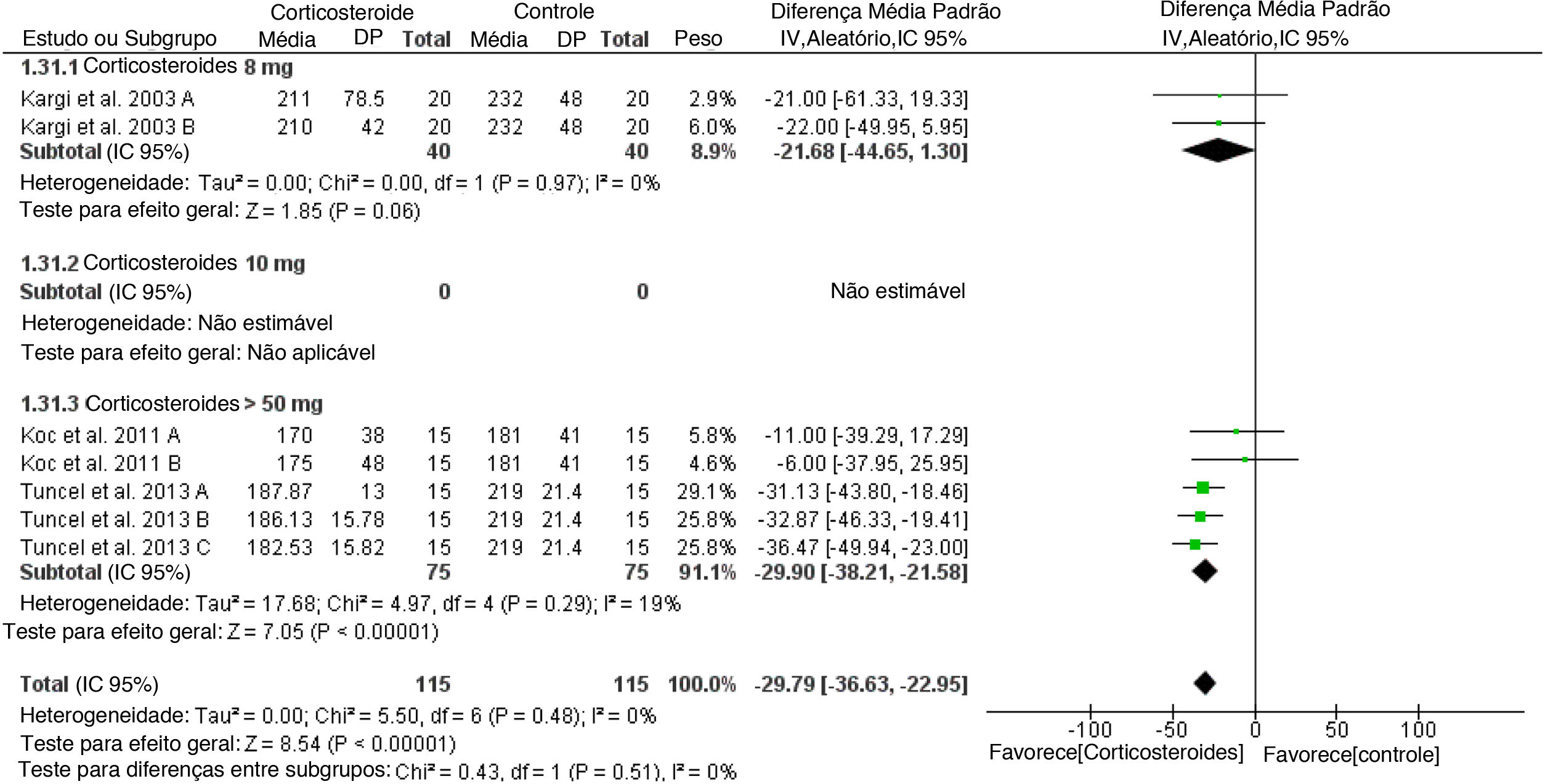
Sangramento intraoperatórioO uso de corticosteroides no período pré‐operatório reduziu significantemente o sangramento intraoperatório quando comparado ao placebo (DMP geral = ‐29,79mL, IC 95%: ‐36,63, ‐22,95) sem diferença ou heterogeneidade entre as doses de corticosteroide (teste para diferenças de subgrupo: Chi2 = 0,53, p = 0,47, I2 = 0%) (fig. 9).
DiscussãoA presente revisão sistemática incluiu 19 ensaios clínicos. Desses, apenas 10 estudos foram incluídos na síntese quantitativa das evidências. Nossa metanálise fornece evidências de Nível 1 de que os corticosteroides têm um efeito benéfico na redução do edema e equimoses no pós‐operatório. Além disso, o uso de corticosteroides no pré‐operatório diminuiu o sangramento intraoperatório. Embora o edema e as equimoses pós‐operatórios tenham ocorrido comumente após a cirurgia plástica facial e os corticosteroides sejam comumente usados, um pequeno número de estudos foi feito para estabelecer sua eficácia e determinar a dose e o tipo preferidos a serem administrados.
No primeiro dia de pós‐operatório, doses menores de corticosteroides (8mg e 10mg) foram associadas a diferenças menores no escore médio de edema e equimoses palpebrais superiores e inferiores, enquanto as doses mais elevadas foram associadas a diferenças maiores. Nenhum dos estudos incluídos relatou eventos adversos relacionados às doses mais altas ou mais baixas de corticosteroides.
Além disso, o uso de corticosteroides no pré‐operatório reduziu significantemente o sangramento intraoperatório quando comparado ao placebo para doses mais altas > 50mg por dia (p < 0,0001), mas não para doses de 8mg de corticosteroide (p = 0,06). A adição de dose de esteroide pós‐operatório ao pré‐operatório foi associada a uma diminuição maior de edema e equimoses do que no pré‐operatório isoladamente. O uso de doses mais altas de metilprednisolona pode melhorar o edema e a equimose pós‐operatórios de forma eficiente no primeiro dia de pós‐operatório, em vez de qualquer outro esteroide. O uso de doses mais altas de metilprednisolona não foi associado a evento adverso intra‐ ou pós‐operatório, mas diminuiu significantemente o sangramento intraoperatório.3,4
Nenhum dos estudos incluídos relatou os resultados de dor pós‐operatória, tempo de cicatrização, satisfação do paciente ou qualidade de vida. Os corticosteroides têm um efeito significante no controle da dor após cirurgias plásticas faciais, dentoalveolares e maxilofaciais.31
Na presente metanálise, os estudos incluídos usaram a mesma escala de 0 a 4 para avaliar o grau de edema e equimose, com diferenças mínimas na descrição de cada grau; portanto, usamos a diferença média padronizada para cada comparação.
Cinco estudos foram excluídos da metanálise devido ao uso de diferentes métodos radiológicos, mas relataram resultados importantes. Abukawa et al., em 2017,22 usaram as medidas da TC na espessura do músculo masseter e tecido mole bucal para avaliar o edema pós‐operatório e revelaram que a taxa de aumento na espessura do músculo masseter no grupo que recebeu corticosteroide foi significantemente menor do que no grupo controle. Por outro lado, Berinstein et al. em 199815 eles concluíram que os pacientes com rinoplastia que receberam dexametasona apresentaram aumento do edema no pós‐operatório quando comparados aos controles avaliados por exames de ressonância magnética que quantificaram a diferença na espessura dos tecidos moles entre os exames pré e pós‐operatório.
Com imagens de superfície em 3D, Semper‐Hogg et al. em 201724 mostraram que o edema facial diminuiu significantemente no grupo de dexametasona 40mg em comparação ao grupo controle, embora doses mais baixas de dexametasona (5 e 15mg) não tenham reduzido o edema facial após a cirurgia ortognática. Weber et al.28 quantificaram o edema facial por meio de escaneamento computadorizado de cinco conjuntos de fotografias padronizadas e revelaram que a administração de dexametasona (8 e 16mg) reduziu significantemente o edema pós‐operatório.
Alajami et al.23 relataram um método diferente de avaliação; a ausência de edema foi classificada como grau 0, o edema da pálpebra inferior sozinho foi classificado como Grau 1, o edema das pálpebras inferior e superior foi classificado como Grau 2 e o edema em toda a órbita espalhando‐se para o rosto ± equimose subconjuntival foi classificado como Grau 3. O resultado mostrou que houve diferença altamente significante na presença de diferentes graus de edema no grupo corticosteroide em todos os dias de avaliação (p < 0,001). O edema de Grau 1 estava presente no grupo corticosteroide no Dia 1 (43,2%), Dia 2 (29,5%), Dia 5 (13,6%) e estava completamente ausente no 7° dia de pós‐operatório. No grupo placebo, no 7° dia de pós‐operatório, 33,3% dos pacientes ainda apresentavam Grau 1 e 16,7% apresentavam edema de Grau 2. Além disso, 16,7% no grupo placebo continuaram apresentando edema de Grau 1 no 10° dia de pós‐operatório.
Em relação à intensidade da equimose e gravidade do edema, em 2007, Totonchi et al.26 mostraram que a dexametasona 10mg reduziu o edema durante o período pós‐operatório inicial, sem diferenças significantes nas classificações de extensão e intensidade da equimose no dia 2 do pós‐operatório, mas houve uma diferença significante na classificação do edema em relação ao grupo controle, demonstrou mais edema em comparação com o grupo dexametasona. No dia 8 do pós‐operatório, o grupo dexametasona demonstrou maior extensão e maior intensidade de equimoses em comparação com o grupo controle e não houve diferenças na magnitude do edema no dia 8 do pós‐operatório.
Tuncel et al., 2013,16 relataram que a dexametasona com hipotensão controlada reduziu consideravelmente o edema pós‐operatório e a equimose na rinoplastia, bem como o sangramento intraoperatório. A inclusão deste estudo em nossa metanálise foi associada a uma heterogeneidade significante, porque ele relatou os dados comparativos como mediana e intervalo interquartil, o que exigiu que outras transformações fossem agrupadas em outros estudos. A remoção do estudo de Tunnel da análise levou à resolução da heterogeneidade e não está associada à mudança na significância geral em todos os resultados.
A qualidade geral das evidências dos estudos incluídos é alta. A principal preocupação é o pequeno tamanho da amostra de cada artigo, apesar do grande número de cirurgias plásticas faciais. De acordo com o relatório da American Society of Plastic Surgeons de 2018, a remodelagem do nariz é um dos 5 principais procedimentos cirúrgicos cosméticos de 2018 (213.000 cirurgias em 2018).32
Embora tenhamos apresentado a primeira grande revisão sistemática abrangente (19 estudos incluídos) para investigar o efeito de corticosteroides na redução das complicações pós‐cirurgia plástica facial, relatamos um resultado consistente com a revisão anterior da Cochrane em 201433 e com outras revisões sistemáticas que investigaram o uso de corticosteroides na rinoplastia.34,35 A revisão Cochrane relatou que uma dose única pré‐operatória de 10mg de dexametasona diminuiu o edema e a equimose nos dois primeiros dias de pós‐operatório; essa diferença não foi observada após esse período, enquanto altas doses de metilprednisolona diminuíram tanto a equimose quanto o edema nos dias 1, 3 e 7 no pós‐operatório.
A maioria dos estudos incluídos foi heterogênea em relação ao número de doses pré e pós‐operatórias, bem como ao tipo de esteroides usados. Os estudos de Abukawa et al.,22 Griffies et al.,13 Koc et al.,4 e Ozdel et al.21 administraram esteroides no pré‐operatório, enquanto os estudos de Tuncel et al.,16 Mehdizadeh et al.,30 Kargi et al.,29 Hoffmann et al.14 e Alajami23 administraram doses de esteroides nos períodos pré e pós‐operatório. Portanto, fizemos análises de subgrupos para formar um pool com os grupos semelhantes em um modelo de metanálise e fornecer uma estimativa geral do efeito, como visto nas tabelas suplementares 1 a 2. A maioria dos subgrupos apresentou pouco poder de estudo e seus resultados não podem ser generalizados devido ao pequeno número de estudos incluídos. Recomendamos a feitura de ensaios clínicos randomizados bem desenhados, com tamanho grande de amostra, para investigar o efeito do tempo (pré e pós‐operatório) e da dosagem (única e múltipla) e tipo de corticosteroide administrado na cirurgia plástica facial.
Em conclusão, esta metanálise abrangente confirma um benefício estatisticamente significante do uso de corticosteroides pré‐operatórios quando comparados ao placebo. Além disso, a continuação dos esteroides no pós‐operatório está associada à redução em longo prazo de complicações, inclusive edema, equimose e sangramento intraoperatório. Finalmente, doses mais altas de corticosteroides estão associadas a uma redução mais significante de edema e equimose, mas estudos adicionais são recomendados para determinar os efeitos colaterais pós‐operatórios como infecção do sítio cirúrgico e atraso na cicatrização.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
AgradecimentosAo Dr. Hussien Ahmed da MRSclin pelo apoio editorial e estatístico.
Como citar este artigo: Aldhabaan SA, Hudise JY, Obeid AA. A meta‐analysis of pre‐ and postoperative corticosteroids for reducing the complications following facial reconstructive and aesthetic surgery. Braz J Otorhinolaryngol. 2022;88:63–82.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.