Alterações olfativas são bastante comuns na população, causam significativo impacto na qualidade de vida. A documentação da função olfatória é fundamental para o diagnóstico, tratamento e seguimento de pacientes que cursam com doenças inflamatórias das vias aéreas superiores, neurodegenerativas ou infecções virais. Entre os diferentes testes de olfato existentes, o teste do Connecticut Chemosensory Clinical Research Center (CCCRC) é barato, de fácil aplicação, mas que ainda não foi avaliado em grande escala para a população brasileira.
ObjetivoValidar o teste de olfato CCCRC com adaptação para a população brasileira, avaliar o desempenho de voluntários saudáveis e a estabilidade do teste em retestes.
MétodoNeste estudo fizemos adaptação cultural do teste CCCRC para o Brasil. Para validação e determinação dos escores de normalidade, aplicamos o teste em 334 voluntários saudáveis, com mais de 18 anos. O reteste foi ainda feito em até quatro semanas em 34 voluntários adicionais para avaliar concordância dos resultados.
ResultadosAvaliando o desempenho dos participantes, valores de normosmia e hiposmia leve foram obtidos em mais de 95% deles. Mulheres (58,4%) apresentaram melhor acurácia em relação aos homens (41,6%), p<0,02; e indivíduos acima dos 60 anos apresentaram pior desempenho (mediana: 6; percentil 75: 6,5; percentil 25: 5). O teste e reteste dos 34 voluntários demonstrou que houve concordância (coeficiente de correlação intraclasse, CCI) considerada boa em narina esquerda (CCI=0,65) e excelente em narina direita (CCI=0,77) no escore combinado.
ConclusãoO teste CCCRC adaptado para o Brasil apresentou valores de normalidade semelhantes ao teste originalmente descrito e a validações em outros países, com alta taxa de reprodutibilidade. Considerando a relação custo‐benefício altamente favorável, o CCCRC adaptado é uma ferramenta muito útil para mensuração da função olfatória na população brasileira.
O olfato é um dos cinco sentidos que permitem aos seres vivos interagir com o meio ambiente através de moléculas odoríferas. A partir desse sentido, identificamos situações de perigo quando detectamos moléculas nocivas à saúde, como presença de gases tóxicos e identificamos alimentos inapropriados para consumo.1 Além disso, graças à interação do olfato com o sistema límbico e com áreas corticais superiores, a estimulação de receptores odoríferos específicos promove respostas emocionais diversificadas, agradáveis ou não, cria memória olfatória de longa latência.2
Disfunções olfatórias podem impactar negativamente sobre a saúde física e psicológica do indivíduo, levar a uma pioria na qualidade de vida, anedonia, transtornos de humor e diminuição do apetite, além de riscos diretos, pela maior propensão a intoxicação a alimentos e a inalantes tóxicos.3
A principal causa identificável de perda do olfato são as infecções virais agudas de vias respiratórias superiores (IVAS),4 correspondem a cerca de um terço das perdas súbitas de olfato e com distribuição sazonal correspondente à das IVAS.3,5–7 Outras causas comuns são traumatismo cranioencefálico, doenças nasossinusais crônicas, neurológicas e neurodegenerativas.1,4,7,8
Por ser um sintoma com alta subjetividade entre os pacientes, a documentação quantitativa e qualitativa da função olfatória é de fundamental importância para os pacientes que se apresentam com alterações do olfato. Da mesma maneira, é de fundamental importância a documentação da função olfatória em pacientes que irão ser submetidos a cirurgias nasais, como nas cirurgias de base de crânio e cirurgias endoscópicas nasossinusais. Além disso, considerando o impacto do olfato em algumas doenças nasossinusais, como rinite alérgica e rinossinusites crônicas,7–9 esse teste seria essencial para monitorar a resposta ao tratamento, seja clínico ou cirúrgico.
Um dos testes de olfato mais usados mundialmente é o de Connecticut Chemosensory Clinical Research Center (CCCRC).10 O CCCRC testa tanto o limiar olfativo como a identificação de diferentes odores, permite a avaliação tanto quantitativa como qualitativa do olfato.10 Além disso, investiga de modo independente cada uma das cavidades nasais, pode discriminar a lateralidade da alteração olfatória. É um teste de baixo custo e que pode ser considerado para aplicação clínica em larga escala. Apesar disso, por questões de odores culturalmente mais conhecidos ou não, necessita de adequações mediante o público no qual será aplicado.
Nesse contexto, em virtude de o teste do CCCRC não ter sido amplamente empregado para indivíduos brasileiros, tivemos como objetivos neste estudo avaliar os escores de voluntários brasileiros saudáveis ao teste CCCRC, após adaptação cultural para o Brasil, assim como validar seu uso para a população brasileira.
MétodoEste estudo foi aprovado no comitê de ética em pesquisa do Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto sob número CAAE: 97227018.5.0000.5440. Todos os voluntários assinaram o termo de consentimento livre e esclarecido. Neste estudo, aplicamos um questionário não validado sobre antecedentes pessoais do paciente (tabela 1), seguido do teste do olfato de Connecticut adaptado para o Brasil (CCCRC adaptado) em indivíduos saudáveis, em dois centros distintos de coleta (Poupatempo de Ribeirão Preto e Hospital das Clínicas da Faculdade de Medicina de Minas Gerais). Como critérios de elegibilidade, selecionamos indivíduos maiores de 18 anos, que declararam olfato presente no momento da avaliação e ausência de queixas nasossinusais compatíveis com rinossinusite. Foram excluídos os indivíduos que declarassem função olfatória ausente, apresentassem infecção do trato superior recente, histórico de traumatismo cranioencefálico grave, doenças psiquiátricas ou neurológicas.
Questionário clínico aplicado antes da feitura do teste de olfato
| Não | Sim | |
|---|---|---|
| Você fuma ou já fumou? | ||
| Você sente bem cheiro? | ||
| Você tem alguma doença no nariz? | ||
| Já fez cirurgia no nariz? | ||
| Sente cheiro ruim dentro do nariz? | ||
| Alergia a remédios? | ||
| Tem asma? | ||
| Tem rinite alérgica? | ||
| Já sofreu trauma (pancada) forte na cabeça? | ||
| Tem sangramento no nariz recorrente? | ||
| Tem alguma doença? Qual? |
Para o teste de limiar olfatório, usamos o butanol (álcool n butílico) diluído em sete concentrações (4%, 1%, 0,4%, 0,1%, 0,05%, 0,01% e 0,005%), conforme descrição por Cain.10 As diferentes concentrações de butanol foram envasadas em frascos âmbar, com 60 mL de solução total. Os frascos foram numerados de 1 a 7, da maior para a menor concentração. Um frasco com água destilada (frasco 8), inodoro, foi usado como controle.
O teste de limiar foi feito com a apresentação ao indivíduo de dois frascos idênticos de 60 mL alternadamente, um com água destilada e o outro com uma solução de butanol. Com os olhos fechados, os indivíduos foram instruídos a ocluir uma das narinas enquanto era posicionado o frasco na narina pérvia, solicitou‐se ao indivíduo que inspirasse suavemente para identificar a presença do odor. Caso o indivíduo não identificasse o odor, frascos com a solução de butanol mais concentrados foram apresentados de maneira consecutiva, manteve‐se a alternância com o frasco de água destilada. A testagem foi iniciada pela exposição da menor concentração de butanol (0,005%) até a detecção do frasco com a subsequente maior concentração, com retestagem quando necessário. Dois acertos do frasco com o odorante determinaram a concentração mínima definida como limiar olfatório do indivíduo para a cavidade nasal testada. Os mesmos passos foram repetidos para a cavidade nasal contralateral. O escore variou de 0 a 7 pontos, 0 para o indivíduo que não conseguiu identificar qual era o frasco que continha o odorante em qualquer concentração e 7 para o indivíduo que identificou o odorante no frasco com a menor concentração.
Para o teste de identificação de substâncias, foram usadas 8 substâncias: café em pó, canela em pó, talco de bebê (Johnson & Johnson®), paçoca (Paçoquita®), chocolate em pó (Nescau®), sabonete neutro (Palmolive®) e naftalina. Para adaptar o teste à realidade brasileira, substituímos a pasta de amendoim contida no teste original pela paçoca, por se tratar de um produto mais reconhecido nacionalmente. As substâncias foram colocadas em potes vedados, com tampa e com rótulo preto, com proporções equivalentes (10 gramas por frasco).
Para a identificação de odores, os indivíduos receberam uma lista que continha o nome das oito substâncias presentes no teste, além do nome de oito substâncias distratoras (tabela 2). Os indivíduos, com os olhos fechados, foram instruídos a ocluir uma narina enquanto o frasco era posicionado na outra narina pérvia. Antes da abertura de cada frasco, foi feita uma suave agitação do frasco para homogeneização das substâncias odoríferas em seu interior. Para cada frasco apresentado, o indivíduo deveria citar uma das substâncias da lista. Caso houvesse dúvida pelo paciente, cada frasco poderia ser novamente apresentado, assim como a própria lista. Após testagem das 8 substâncias em uma narina, foram repetidos os mesmos passos na narina contralateral, apresentaram‐se os frascos de forma aleatória para evitar memorização da ordem. A função do nervo trigêmeo foi testada no fim do teste com a apresentação de mentol (Vick®), mas a identificação dessa substância não foi incluída no escore final. O escore do teste de identificação foi obtido através da pontuação de 0 a 7 para cada cavidade nasal, de acordo com a quantidade de odores acertados.
O escore final do teste foi calculado pela média aritmética dos acertos da identificação das substâncias (nota de 0 a 7) com a nota obtida da identificação do limiar do butanol para cada cavidade nasal. A média foi definida para cada lado, o limiar olfatório foi classificado em normosmia (escore 6 a 7), hiposmia leve (5–5,75), hiposmia moderada (4–4,75), hiposmia grave (2–3,75) e anosmia (0–1,75) (tabela 3).
Graduação de desempenho olfatório – Teste CCCRC10
| Normosmia | 6 – 7 |
| Hiposmia leve | 5 – 5,75 |
| Hiposmia moderada | 4 – 4,75 |
| Hiposmia grave | 2 – 3,75 |
| Anosmia | 0 – 1,75 |
Após a etapa de aplicação do teste para determinar os escores em indivíduos sem queixas, foi acrescentada uma nova amostra de 34 participantes para verificar o grau de concordância individual em teste‐reteste. Esse grupo, correspondente a 10,1% da amostra total, foi composto por indivíduos com os mesmos critérios de elegibilidade e que não haviam sido testados anteriormente. Nessa amostra, aplicamos o teste duas vezes, com intervalo de uma a quatro semanas entre elas, para avaliação de reprodutibilidade dos escores. Entre as aplicações, não foram revelados os limiares atingidos e nem as substâncias contidas em cada frasco. Seguimos o mesmo protocolo para avaliação de limiar e identificação de substâncias citados anteriormente.
Os dados foram analisados com o software BM SPSS Statistics v. 20. As variáveis categóricas foram expressas em frequência absoluta (n) e relativa (%). Para as variáveis numéricas, foram calculados a mediana e percentis e valores mínimo e máximo. Para a comparação dos resultados do teste de olfato, foi aplicado o teste não paramétrico de Mann‐Whitney para amostras independentes. A escolha do teste foi feita baseada nos testes de normalidade de Shapiro‐Wilk e Kolmogorov‐Smirnov que descartou distribuição normal nos grupos avaliados. Consideramos como estatisticamente significante quando p‐valor foi menor do que 5%. Para avaliação do teste‐reteste, determinou‐se o grau de concordância dos escores combinados, com análise estatística do Coeficiente de Correlação Intraclasse.
ResultadoO teste olfatório de Connecticut (CCCRC) adaptado para o Brasil foi aplicado em 334 voluntários. A idade dos participantes variou de 18 a 76 anos, com média de 39,9 (± 14,5).
O resultado das medianas dos escores combinados, em cada narina, apresentou‐se dentro do limiar de normosmia (resultados acima de 6), conforme tabela 4.
Resultados do teste CCRC adaptado para o Brasil
| Avaliação | Mediana | Mínimo | Percentil 25 | Percentil 75 | Máximo |
|---|---|---|---|---|---|
| Lado direito | |||||
| Limiar olfatório | 7,0 | 2,0 | 6,0 | 7,0 | 7,0 |
| Identificação de odores | 7,0 | 0,0 | 6,0 | 7,0 | 7,0 |
| Escore combinado | 6,5 | 2,5 | 6,0 | 7,0 | 7,0 |
| Lado esquerdo | |||||
| Limiar olfatório | 7,0 | 2,0 | 6,0 | 7,0 | 7,0 |
| Identificação de odores | 7,0 | 0,0 | 6,0 | 7,0 | 7,0 |
| Escore combinado | 6,5 | 2,5 | 6,0 | 7,0 | 7,0 |
Não se observou diferença entre os resultados de cada narina. A avaliação de integridade de receptores do nervo trigêmeo apresentou positividade em 98,5% na cavidade nasal direita e 97,3% no lado esquerdo.
A classificação final dos voluntários apresentou como resultado a normosmia em 82,6% das narinas direitas e 83,55% das narinas esquerdas (tabela 5). Se acrescentar a esse valor os testados que foram classificados como hiposmia leve, chega‐se ao patamar de 95,8% e 96,7% na narina direita e esquerda, respectivamente.
Em relação às variáveis clínicas obtidas no questionário (tabela 6), não se encontraram relações quanto ao desempenho olfatório em pacientes que apresentavam tabagismo, rinite alérgica, cirurgia nasal prévia, traumatismo cranioencefálico, asma, alergia medicamentosa e epistaxe. O único resultado significante foi em relação ao desempenho dos pacientes que alegaram comorbidades metabólicas. Ressalta‐se que as respostas positivas no questionário foram, em sua maioria, de menos de 20 participantes.
Avaliação da relação de diferentes variáveis clínicas com o desempenho do teste
| Variável | Lado direito | Lado esquerdo | ||||||
|---|---|---|---|---|---|---|---|---|
| Mediana | Percentil 25 | Percentil 75 | Valor‐p | Mediana | Percentil 25 | Percentil 75 | Valor‐p | |
| Tabagismo | ||||||||
| Sim (n=66) | 6,50 | 6,00 | 7,00 | 0,26 | 6,50 | 6,00 | 7,00 | 0,36 |
| Não (n=268) | 6,50 | 6,00 | 7,00 | 6,50 | 6,00 | 7,00 | ||
| Olfato preservado | ||||||||
| Sim (n=322) | 6,50 | 6,00 | 7,00 | 0,93 | 6,50 | 6,00 | 7,00 | 0,40 |
| Não (n=12) | 6,75 | 5,50 | 7,00 | 6,25 | 5,37 | 7,00 | ||
| Doença nasal | ||||||||
| Sim (n=12) | 6,75 | 6,00 | 7,00 | 0,57 | 6,50 | 5,75 | 7,00 | 0,78 |
| Não (n=322) | 6,50 | 6,00 | 7,00 | 6,50 | 6,00 | 7,00 | ||
| Cirurgia nasal | ||||||||
| Sim (n=10) | 6,25 | 6,00 | 7,00 | 0,70 | 6,00 | 6,00 | 6,00 | 0,92 |
| Não (324) | 6,50 | 6,00 | 7,00 | 6,50 | 6,00 | 7,00 | ||
| Alergia medicamentosa | ||||||||
| Sim (n=28) | 6,50 | 6,50 | 7,00 | 0,31 | 6,50 | 6,50 | 7,00 | 0,10 |
| Não (n=324) | 6,50 | 6,00 | 7,00 | 6,50 | 6,00 | 7,00 | ||
| Cheiro ruim | ||||||||
| Sim (n=9) | 6,50 | 6,00 | 7,00 | 0,77 | 6,00 | 5,50 | 6,50 | 0,07 |
| Não (n=325) | 6,50 | 6,00 | 7,00 | 6,50 | 6,00 | 7,00 | ||
| Asma | ||||||||
| Sim (n=10) | 6,50 | 6,00 | 7,00 | 0,72 | 6,50 | 6,00 | 7,00 | 0,81 |
| Não (n=324) | 6,50 | 6,00 | 7,00 | 6,500 | 6,00 | 7,00 | ||
| Rinite | ||||||||
| Sim (n=66) | 6,50 | 6,00 | 7,00 | 0,19 | 6,50 | 6,00 | 7,00 | 0,29 |
| Não (n=268) | 6,50 | 6,00 | 7,00 | 6,50 | 6,00 | 7,00 | ||
| Pancada na cabeça | ||||||||
| Sim (n=20) | 6,50 | 6,50 | 6,75 | 0,97 | 6,50 | 6,00 | 6,75 | 0,50 |
| Não (n=314) | 6,50 | 6,00 | 7,00 | 6,50 | 6,00 | 7,00 | ||
| Sangramento nasal | ||||||||
| Sim (n=9) | 6,50 | 6,00 | 7,00 | 0,92 | 6,50 | 6,00 | 7,00 | 0,92 |
| Não (n=325) | 6,50 | 6,00 | 7,00 | 6,50 | 6,00 | 7,00 | ||
| Doença | ||||||||
| Sim (n=49) | 5,50 | 6,50 | 6,50 | <0,01 | 5,50 | 6,50 | 7,00 | 0,01 |
| Não (n=285) | 6,50 | 6,00 | 7,00 | 6,00 | 6,50 | 7,00 | ||
Valor obtido pelo cálculo do teste não‐paramétrico de Mann‐Whitney (amostras independentes).
A distribuição etária verificada em nosso estudo foi compatível com a distribuição etária nacional, assim também como na distribuição entre homens e mulheres (relação 0,71/1). A renda familiar média na nossa amostra também apresentou correspondência quando comparada com a renda da população brasileira em estatísticas do IBGE (tabela 7).
Variáveis sociodemográficas de voluntários brasileiros submetidos ao teste CCCRC adaptado para o Brasil
| Variável | n | % |
|---|---|---|
| Sexo | ||
| Feminino | 195 | 58,4 |
| Masculino | 139 | 41,6 |
| Raça | ||
| Branco | 178 | 53,3 |
| Pardo | 105 | 31,5 |
| Negro | 49 | 14,7 |
| Amarelo | 1 | 0,3 |
| Faixa etária | ||
| 10 a 19 anos | 11 | 3,3 |
| 20 a 29 anos | 89 | 26,7 |
| 30 a 39 anos | 77 | 23,1 |
| 40 a 49 anos | 62 | 18,6 |
| 50 a 59 anos | 55 | 16,5 |
| 60 ou mais anos | 39 | 11,7 |
| Escolaridade | ||
| Ensino fundamental incompleto | 48 | 14,4 |
| Ensino fundamental completo | 18 | 5,4 |
| Ensino médio incompleto | 15 | 4,5 |
| Ensino médio completo | 122 | 36,5 |
| Ensino superior incompleto | 47 | 14,1 |
| Ensino superior completo | 84 | 25,1 |
| Renda familiara | ||
| Até 2 salários mínimos | 151 | 45,2 |
| De 2 até 4 salários mínimos | 91 | 27,2 |
| De 4 até 10 salários mínimos | 39 | 11,7 |
| De 10 até 20 salários mínimos | 13 | 3,9 |
| Acima de 20 salários mínimos | 1 | 0,3 |
| Renda não declarada ou indivíduo sem renda (dependente) | 39 | 11,7 |
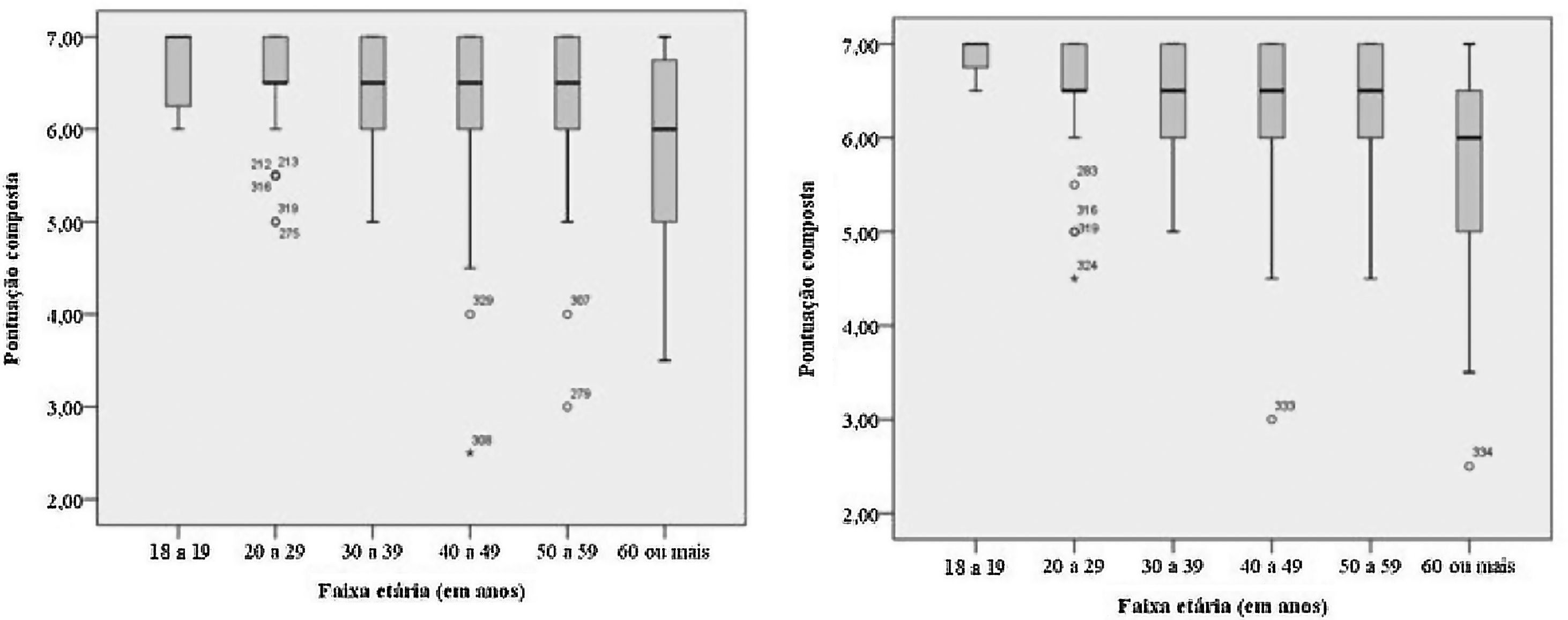
A performance olfatória foi menor nos indivíduos acima de 60 anos (mediana: 6; percentil 75: 6,5; percentil 25: 5) em relação às demais faixas etárias (mediana das faixas 20–30, 30–40, 40–50, 50–60 anos: 6,5; mediana 18–20 anos: 7), com queda nos escores (fig. 1).
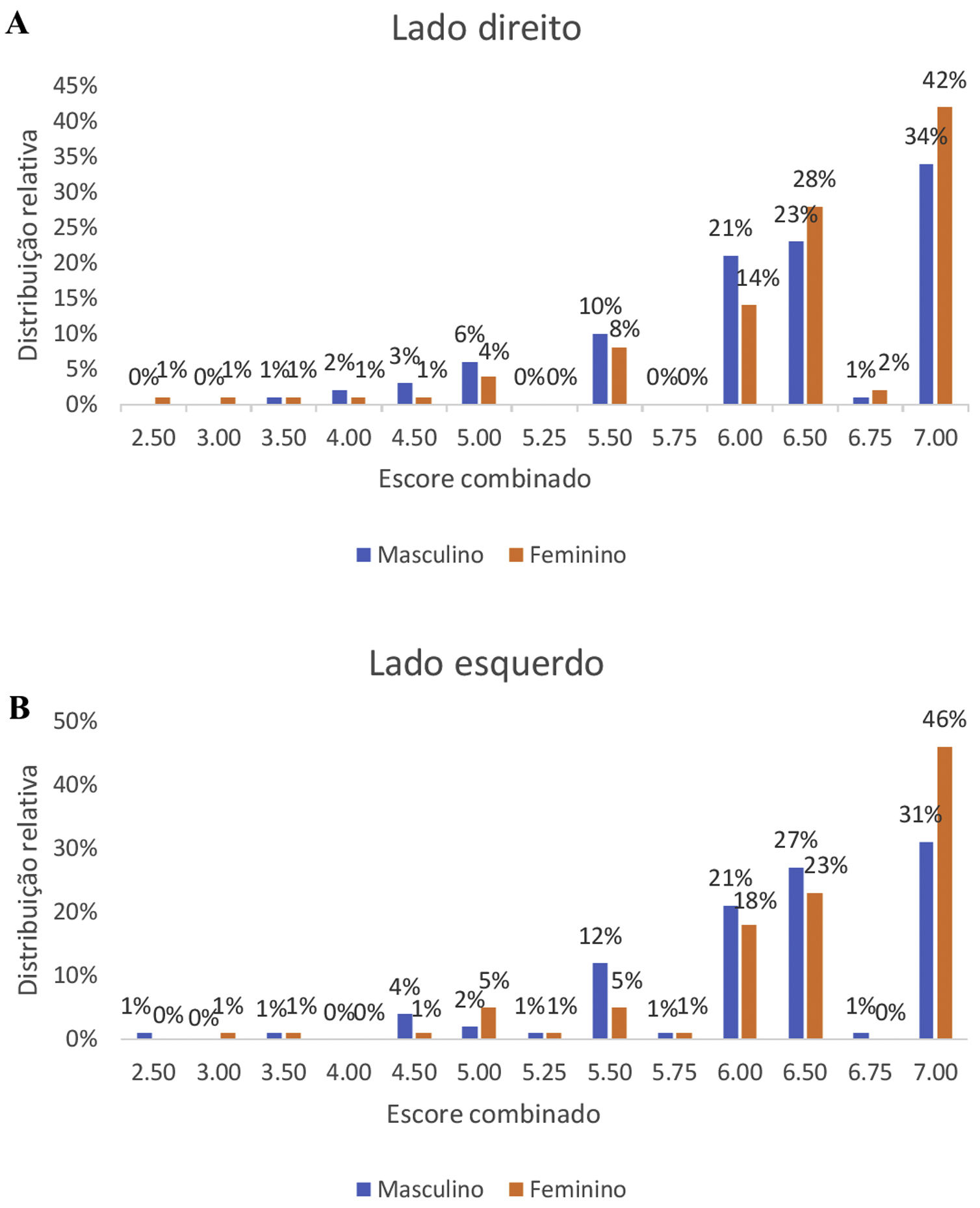
Quando comparamos o desempenho olfatório em relação ao sexo, observamos melhor performance dos voluntários do sexo feminino (mediana: 6,5) em relação ao masculino (mediana: 6,5), com p‐valor <0,02 (fig. 2).
A correlação intraclasse do teste e reteste no escore combinado foi de 0,77 (95% IC 0,54–0,88) à direita e 0,65 (95% IC 0,29–0,82) à esquerda, considerados como excelente e boa, respectivamente. A média de dias de aplicação do reteste após o teste foi de 9,9 dias (tabela 8).
Análise de concordância teste‐reteste do CCCRC entre os participantes estudo (n=34)
| Variável | Mediana teste | Mediana reteste | CCI | 95% IC CCI |
|---|---|---|---|---|
| Limiar olfatório | ||||
| Direito | 7,00 | 7,00 | 0,76 | 0,53–0,88 |
| Esquerdo | 6,50 | 7,00 | 0,69 | 0,38–0,85 |
| Identificação odores | ||||
| Direito | 7,00 | 7,00 | 0,91 | 0,81–0,95 |
| Esquerdo | 7,00 | 7,00 | 0,66 | 0,33–0,83 |
| Escore combinado | ||||
| Direito | 6,50 | 6,50 | 0,77 | 0,54–0,88 |
| Esquerdo | 6,50 | 6,50 | 0,65 | 0,29–0,82 |
CCI, Coeficiente de correlação intraclasse; 95% IC, Intervalo de confiança 95%.
Interpretação do coeficiente de correlação intraclasse
Correlação: >0,75 – Excelente; 0,6–0,75 – Boa; 0,4–0,6 – Razoável; <0,4 – Fraca.
O nariz, como estrutura anatômica de entrada do trato respiratório superior, apresenta na quimiorrecepção olfativa e na sinalização e transdução de sinal um dos seus mais intrincados mecanismos. A anatomia que envolve parede lateral, com a divisão em conchas nasais, inferior, média, superior e eventualmente suprema, septo nasal e pirâmide externa cartilaginosa, apresenta características que fazem o funcionamento nasal ser perfeito ao equilibrar a função filtrativa, umidificadora e aquecedora do ar. O epitélio olfatório é composto por neurônios receptores olfatórios (NRO), células basais, células de suporte e células microvilares. Assim, alterações anatômicas, mecânicas ou neurossensoriais podem estar relacionadas à alteração olfativa.
Atualmente no Brasil existem testes de olfato já validados. Um deles, o teste de identificação do olfato anteriormente denominado de UPSIT,11,12 é de fácil uso, autoaplicável e consistente na identificação de 40 substâncias dispostas em cartelas que, após raspagem de uma fita, eliminam partículas odoríferas microencapsuladas, necessita de uma resposta forçada entre quatro opções. Como desvantagens, o teste consta apenas com a identificação dos odores, e não o limiar, e tem custo elevado, o que dificulta a feitura em larga escala e em serviços públicos. Outro teste é o Sniffin’ Sticks,13 que avalia tanto o limiar como a identificação dos odores, e tem validação inclusive para a população pediátrica;14 no entanto, esse teste também é oneroso, o que inviabiliza o seu uso rotineiro no serviço público brasileiro.
Na busca por um teste mais viável, de baixo custo e fácil aplicação, optamos por validar o CCCRC para o Brasil. O CCCRC apresenta algumas vantagens por identificar tanto o limiar olfatório como quantificar a identificação de sete odores específicos. Ainda, permite identificar cada uma dessas características isoladamente em cada narina. Outra vantagem do CCCRC é o seu baixo custo, pode até ser reusado em outras pessoas dentro de um prazo de até 90 dias. No entanto, uma das desvantagens em relação ao UPSIT é que o CCCRC não pode ser autoaplicado, necessita de um profissional treinado para o procedimento, e leva um tempo um pouco maior para aplicação, em torno de 15 minutos.
Através da seleção aleatória de indivíduos nos locais de pesquisa, obteve‐se uma representatividade adequada de classe econômica e distribuição etária.15 Mesmo com uma representação percentual de idosos considerável, poucos foram os resultados de alteração olfatória pior do que hiposmia leve.
Consideramos previamente que diferenças sociais poderiam trazer diferenças no desempenho do teste, pois camadas economicamente privilegiadas poderiam ter maiores oportunidades de contato com maior diversidade de odores em comparação aos estratos sociais menos favorecidos. A relevância da amostragem social está relacionada com o fato de que um teste olfatório nacionalmente adequado deve prezar pela sua acurácia em relação às substâncias escolhidas. Portanto, a diversidade da amostra estudada e a representatividade em relação a sociedade brasileira, aliada ao desempenho dos voluntários, demonstram que em pessoas sem queixas olfatórias existe um alto percentual de acerto das substâncias apresentadas e da detecção do butanol, equivalente aos dados internacionais.
O valor de escore do teste CCCRC Brasil obtido na amostra é compatível com os resultados de validações do CCCRC em outras populações16,17 e similar aos demonstrados no trabalho original do teste CCCRC.10 Dessa maneira, conseguimos demonstrar que a troca da pasta de amendoim pela paçoca teve uma ótima performance para a adaptação brasileira do teste, uma vez que pasta de amendoim não é muito conhecida entre os brasileiros, principalmente os de classe social menos privilegiada. Apesar de excluir do trabalho indivíduos que apresentassem queixas olfativas, a análise de desempenho quando relacionada à idade demonstrou queda no escore daqueles com mais de 60 anos, corroborou a literature, a qual diz que pessoas idosas podem apresentar pior discriminação olfativa apesar de não terem queixa.17 Tal fato pode‐se relacionar à baixa percepção da limitação, ou talvez a pouca estimulação que a população idosa tenha na sua rotina.
No desempenho do teste relacionado ao sexo, observamos que mulheres apresentam melhor desempenho olfatório do que homens, de modo semelhante a outros estudos prévios que levantam a possibilidade da relação com a proteção hormonal e menor exposição a fatores ambientais.18
Não houve significância na correlação do desempenho no teste com o questionário aplicado, exceto no quesito comorbidades. Voluntários com comorbidades metabólicas apresentaram escore mais baixo (p <0,05). Porém, o objetivo do trabalho não foi avaliar essa população em especial, o que levou a um número de respostas positivas pequeno e pode ter influenciado nesse resultado em específico.
Com relação ao coeficiente de correlação intraclasse, as variáveis de limiar olfatório, identificação de odores e escore combinado, todas do lado direito, apresentaram correlação excelente e as do lado esquerdo foram consideradas boas, o que torna o teste confiável e reprodutível quando aplicado em torno de 10 dias após.
ConclusãoO teste CCCRC adaptado para o Brasil mostrou estabilidade em relação à retestagem. A troca de pasta de amendoim por paçoca não interferiu no resultado final esperado, em comparação com outras validações e ao trabalho original. Considerando a realidade brasileira, o teste de olfato CCCRC adaptado para o Brasil torna‐se uma útil ferramenta para testagem do olfato na nossa população.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Fenólio GH, Anselmo‐Lima WT, Tomazini GC, Compagnoni IM, Amaral MS, Fantucci MZ, et al. Validation of the Connecticut olfactory test (CCCRC) adapted to Brazil. Braz J Otorhinolaryngol. 2022;88:725–32.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.