As neoplasias mesenquimais malignas que afetam a laringe são tumores raros. O sarcoma pleomórfico indiferenciado (SPI) de alto grau, inicialmente chamado de histiocitoma fibroso maligno, é uma neoplasia maligna de alto grau, caracterizada por células tumorais com pleomorfismo difuso, na ausência de uma linha específica de diferenciação.1‐4 O processo ocorre mais comumente em homens e afeta todos os grupos etários. Uma ampla margem cirúrgica é muitas vezes indicada devido a suas altas taxas de recorrência local. No entanto, devido à sua raridade, existem escassos estudos sem poder estatístico para definir o melhor desfecho.3,5,6 Assim, os autores apresentam um novo caso de sarcoma pleomórfico indiferenciado de alto grau com origem na laringe e discutem os achados histopatológicos e o tratamento cirúrgico desse tipo raro de tumor.
Relato de casoUm paciente do sexo masculino, de 54 anos, foi avaliado em um serviço hospitalar com queixa clínica de rouquidão nos últimos nove meses. A história anterior incluía hipertensão sistêmica e tabagismo. No exame físico e/ou na laringoscopia, foi identificada uma lesão marrom‐avermelhada elevada, com área ulcerada central, que comprometia a prega vocal direita. Não foram identificados sinais de linfadenopatia cervical. O paciente foi submetido à cordectomia com laser. No exame macroscópico, a amostra consistia em alguns fragmentos acinzentados, irregulares, pesava 1g, o maior fragmento media 1cm.
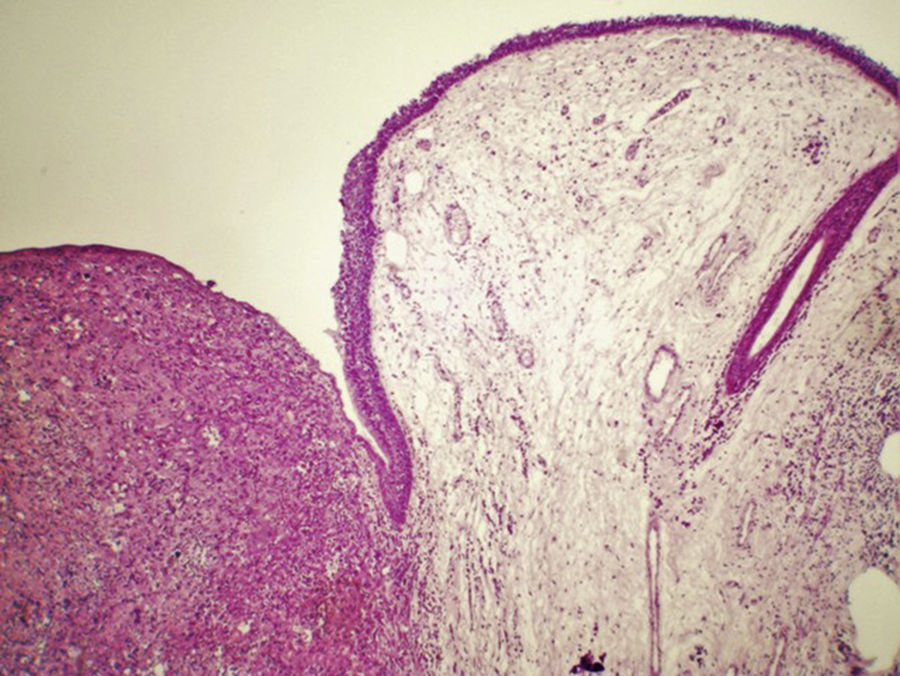
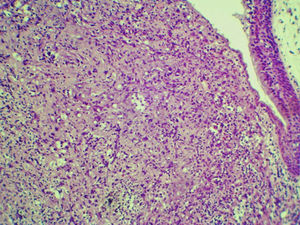
Na avaliação histológica, foi identificada uma neoplasia pleomórfica maligna de alto grau, com células fusiformes dispostas em padrão estoriforme e com alto índice mitótico. O tumor estava presente em todos os fragmentos da amostra e afetava as margens radiais. A análise revelou imunoexpressão positiva para vimentina (difusa) e actina de músculo liso (focal) e coloração negativa para actina muscular específica, calponina, AE1/AE3, S‐100, desmina, h‐caldesmona, CD31, CD34 e fator de Von Willebrand. O diagnóstico de sarcoma pleomórfico indiferenciado de alto grau da laringe (histiocitoma fibroso maligno pleomórfico estoriforme) foi estabelecido (fig. 1).
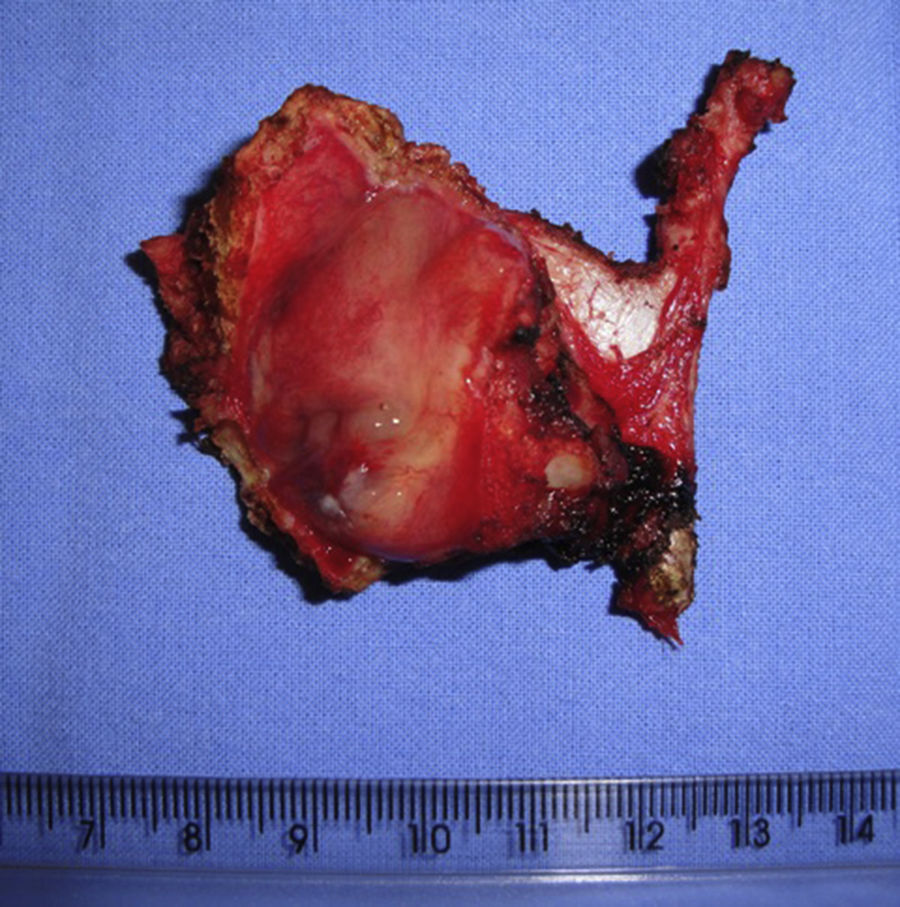
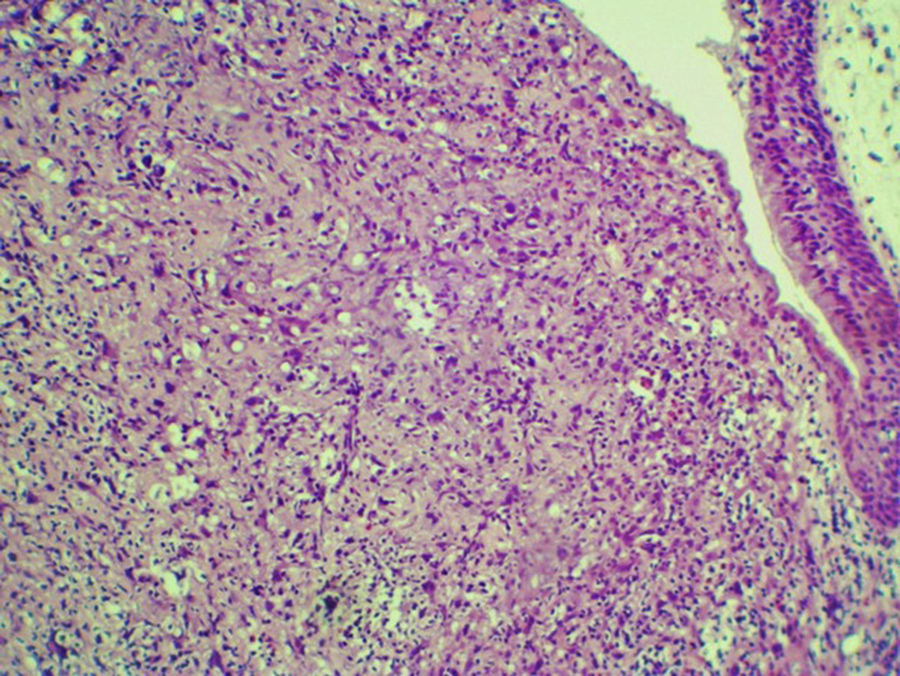
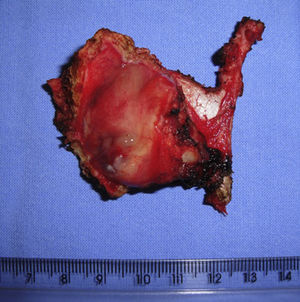
O paciente foi então submetido a uma laringectomia frontolateral direita (fig. 2), sem esvaziamento. O espécime cirúrgico mediu 5,5×4×3cm e mostrou um nódulo residual, mole, cinzento‐acastanhado, que afetava a lâmina própria da prega vocal direita (fig. 3) e que media 0,9×0,6×0,5cm. Não havia evidência de invasão vascular ou linfática. As margens cirúrgicas estavam livres de neoplasia. Após a cirurgia, o paciente apresentou escape salivar, tratado com sucesso com condutas conservadoras. Após cinco anos de acompanhamento, o paciente não apresenta sinais clínicos ou radiológicos de recorrência.
O sarcoma pleomórfico indiferenciado (SPI) de alto grau, anteriormente chamado de histiocitoma fibroso maligno, é uma neoplasia maligna de alto grau caracterizada por células tumorais com pleomorfismo difuso na ausência de uma linha específica de diferenciação. O SPI apresenta uma ampla gama de características histológicas e os padrões mais comuns consistem em uma mistura de áreas estoriformes e pleomórficas.1‐4 O SPI que se origina na laringe é um tumor incomum que caracteristicamente afeta o sexo masculino (3: 1) e ocorre em todos os grupos etários (6‐68 anos). Na laringe, a glote é o local de predileção. Os sintomas podem variar de rouquidão, comprometimento das vias aéreas, disfagia ou sensação de corpo estranho na garganta.3,5,6 Usualmente, o SPI compromete os tecidos moles somáticos como uma massa que apresenta velocidade de crescimento lenta e a coxa é a localização mais comum, seguida pelas extremidades superiores. Os SPIs retroperitoneais estão relacionadas a anorexia, mal‐estar, perda de peso e sinais de aumento da pressão abdominal. A associação entre SPI e radiação prévia já foi descrita.1‐3,6,7 Nosso paciente, no entanto, não tinha sido exposto à radioterapia.
Ao exame macroscópico, SPIs que surgem na laringe podem ser lesões sésseis a polipoides, mas geralmente firmes; frequentemente ulceradas, com uma superfície de corte amarelo‐acastanhada a cinza‐esbranquiçada. Alguns casos são vistos como uma massa nodular solitária, multilobulada, carnosa, que pode medir até 10cm de diâmetro. Na superfície de corte, as áreas mixoide, hemorrágica e necrótica são características comuns.3,5,8,9 Na avaliação microscópica, o SPI pode ser amplamente dividido em células pleomórficas, células fusiformes, células redondas e padrões epitelioides, sem uma linha identificável de diferenciação. As áreas estoriformes consistem em células fusiformes encorpadas dispostas em fascículos curtos em um padrão de roda de carroça, ou estoriforme, ao redor de vasos alinhados longitudinalmente.1,3,5,8‐10 As áreas pleomórficas contêm células fibroblásticas encorpadas, células arredondadas semelhantes a histiócitos dispostas ao acaso sem orientação específica aos vasos e um grande número de células gigantes com vários núcleos hipercromáticos irregulares. A maioria dos tumores tem uma combinação de áreas estoriformes e pleomórficas, com preponderância da última, as quais também exibem pleomorfismo mais acentuado e atividade mitótica.3,5,8‐10 As células tumorais anaplásicas dispostas aleatoriamente em camadas, são uma característica típica do SPI. Em geral, o estroma consiste em delicadas fibrilas de colágeno que envolvem células individuais. Em alguns casos, a deposição de colágeno é extensa e separa amplamente as células. Raramente, o estroma contém material metaplásico osteoide ou condroide.1,5,8‐10 O SPI que exibe numerosas células gigantes tende a ser multinodular e é composto por uma mistura de células gigantes fusiformes, arredondadas e similares a osteoclastos. Alguns exemplos de SPI têm um infiltrado xantomatoso e neutrofílico proeminente, possivelmente relacionado com o desenvolvimento de citocinas. O SPI também pode apresentar elementos mixoides e epitelioides.1,4‐7,10
O diagnóstico da SPI pressupõe ampla amostragem e avaliação de cortes corados com hematoxilina‐eosina; e a técnica de imuno‐histoquímica é uma ferramenta fundamental para excluir outros tumores pleomórficos. O SPI apresenta características de fibroblastos/miofibroblastos e pode mostrar expressão positiva para a actina de músculo liso. A expressão focal para citoqueratinas pode ser observada. As colorações para desmina e h‐caldesmona são caracteristicamente negativas.3,4,6,8,9 O diagnóstico diferencial inclui outros tumores malignos que exibem um grau comparável de pleomorfismo celular. A amostragem extensa e um painel de imunocoloração são passos fundamentais para determinar o diagnóstico do SPI. Esse tumor deve ser diferenciado de carcinoma sarcomatoide, fibrossarcoma, mixofibrosarcoma, formas pleomórficas de lipossarcoma, leiomiossarcoma, rabdomiossarcoma, osteocondrosarcoma e condrossarcoma.3,4,6,8,9
O carcinoma espinocelular (CEC) é a neoplasia maligna mais comum da laringe e as regiões supragóticas e glóticas são as localizações mais comumente afetadas.3,8
O CEC ocorre principalmente em homens adultos que abusam de tabaco e álcool. O tumor origina‐se da mucosa escamosa ou do epitélio respiratório ciliado que sofreu metaplasia escamosa, ou de qualquer grau de displasia surgida no epitélio. O CEC pode se espalhar diretamente para estruturas contíguas, ou através de vasos linfáticos e sanguíneos para os nódulos linfáticos regionais.3,8,9 As metástases hematógenas em locais mais distantes são incomuns e podem ocorrer nos estágios tardios da doença. Estadiamento TNM, margens de ressecção, índice proliferativo e invasão linfovascular e perineural são fatores clínicos preditivos. Metástase de linfonodo é o fator prognóstico mais adverso no CEC de cabeça e pescoço.3,8 Esse comportamento biológico do SPI difere significativamente daquele relacionado com CEC. O SPI é uma neoplasia mesenquimal maligna de alto grau originada do tecido conjuntivo da laringe. A disseminação hematogênica para os pulmões é frequente, sem tendência a desenvolver metástases cervicais. Fatores prognósticos favoráveis independentes relacionados à sobrevivência específica da doença em SPI são o estágio AJCC I ou II, margens cirúrgicas negativas, localização superficial, subtipo mixoide e idade inferior a 50 anos. Margens cirúrgicas amplas são geralmente indicadas por causa de suas altas taxas de recorrência local, variam de 44% a 73%.3,5,6,8,9 Parece que a ressecção radical do SPI é o método mais eficaz para melhorar a sobrevida e reduzir a recorrência. No entanto, a laringectomia parcial frontal e a microcirurgia da laringe foram previamente descritas com bons resultados. A quimioterapia pode ser usada em pacientes com lesões ressecáveis. A radioterapia não é indicada para SPI, devido à resposta tumoral ruim.3,5,6,8,9
ConclusãoO SPI laríngeo é um tumor maligno mesenquimal muito raro, afeta com maior frequência indivíduos do sexo masculino. A imuno‐histoquímica é uma ferramenta fundamental para estabelecer o diagnóstico. Até onde sabemos, este é o terceiro caso relatado de SPI de prega vocal tratado por laringectomia frontolateral na literatura de língua inglesa.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Cambruzzi E, Cruz RP, Gava VG, Pêgas KL. Undifferentiated high‐grade pleomorphic sarcoma of the larynx treated with partial laringectomy. Braz J Otorhinolaryngol. 2020;86:S14–S16.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.