O carcinoma odontogênico esclerosante é a nova adição à lista de tumores de cabeça e pescoço da Organização Mundial da Saúde em 2017. Essa lesão é pouco relatada e não há marcadores patognomônicos para o diagnóstico.
ObjetivoResumir os achados da literatura disponível para fornecer informações atualizadas sobre o carcinoma odontogênico esclerosante e analisar as características clínicas, radiológicas e histopatológicas a favor e contra sua classificação como uma lesão odontogênica maligna.
MétodoUma revisão abrangente da literatura foi feita nos bancos de dados Pubmed, Ebsco e Web of Science, de acordo com as diretrizes do Prisma. Todos os casos relatados em inglês como carcinoma odontogênico esclerosante foram incluídos. Os dados recuperados dos artigos foram sexo, idade, características clínicas, sítio do tumor, histórico médico relevante, achados radiográficos, achados histopatológicos, achados imuno‐histoquímico, tratamentos instituídos e prognóstico.
ResultadosA média de idade ao diagnóstico de carcinoma odontogênico esclerosante foi de 54,4 anos, com uma predileção muito leve pelo sexo feminino. Tumores do tipo carcinoma odontogênico esclerosante foram comumente relatados na mandíbula como um edema expansivo, que pode ser assintomático ou associado a dor ou parestesia. Eles têm aparência radiolucente com reabsorção cortical na radiografia. Histologicamente, o carcinoma odontogênico esclerosante é composto por células epitelioides em estroma denso, fibroso ou esclerótico com invasão perineural ambígua. Atipia celular leve e atividade mitótica imperceptível foram observadas. Não há um marcador imuno‐histoquímico específico para SOC. AE1/AE3, CK 5/6, CK 14, CK19, p63 e E‐caderina foram os marcadores amplamente expressos para carcinoma odontogênico esclerosante. A ressecção foi o principal tratamento feito sem recorrência na maioria dos casos. Nenhum caso de metástase foi relatado.
ConclusãoDe acordo com a literatura disponível, é justificável classificar o carcinoma odontogênico esclerosante como um tumor maligno com nenhum ou desconhecido potencial metastático, que pode ser tratado adequadamente com ressecção cirúrgica. Entretanto, não há evidências suficientes para a graduação histológica ou de malignidade desse tumor.
O carcinoma odontogênico esclerosante (SOC, do inglês sclerosing odontogenic carcinoma) foi um dos novos acréscimos à lista de tumores de cabeça e pescoço da Organização Mundial da Saúde (OMS)1 em 2017 e é definido como um carcinoma intraósseo primário da mandíbula, com citologia branda, estroma acentuadamente esclerótico e um padrão infiltrativo agressivo. Embora o primeiro relato de 3 casos tenha sido publicado em 2008 por Koutlas et al.,2 essa terminologia foi cunhada pela primeira vez por Landwehr e Allen3 em 1996, quando apresentaram seu caso no 50° Annual Meeting of the American Academy of Oral and Maxillofacial Pathology. Koutlas et al.4 apresentaram 2 casos de SOC no mesmo encontro, 9 anos depois. Após o primeiro caso relatado, apenas um pequeno número de casos foi relatado até o momento. A escassez de casos pode ser devido ao sub‐reconhecimento da lesão ou sua descrição como outras entidades, uma vez que se assemelha a muitos outros tumores, como carcinoma metastático, fibroma odontogênico central rico em epitélio, tumor odontogênico epitelial calcificante, carcinoma intraósseo primário, carcinoma odontogênico de células claras e ameloblastoma desmoplásico.1 Este artigo tem como objetivo fornecer um resumo de todos os casos relatados de SOC e analisar suas características a favor e contra sua classificação como entidade maligna.
Material e métodosEsta revisão integrativa foi feita com o intuito de resumir os achados de toda a literatura disponível para fornecer informações atualizadas sobre o SOC e analisar suas características para determinar se é justificável sua classificação como tumor maligno. Os bancos de dados PubMed, Ebsco e Web of Science (WoS) foram usadas para pesquisar artigos relevantes. A busca foi feita com “sclerosing odontogenic carcinoma”, “odontogenic sclerotic carcinoma” e “sclerotic odontogenic carcinoma”
como palavras‐chave com o operador booleano OU aplicado entre as palavras‐chave. Esta revisão incluiu todos os relatos de caso no idioma inglês encontrados nas bases de dados. Nenhum limite foi estabelecido em relação ao ano de publicação. Ambos o títulos e o resumo foram avaliados para selecionar artigos relevantes. As listas de referências dos artigos selecionados também foram verificadas para rastrear quaisquer artigos adicionais não encontrados nas bases de dados PubMed, Ebsco e WoS. Os artigos de texto completo foram recuperados através dos bancos de dados online ou pesquisas manuais. Os dados obtidos dos artigos incluíram sexo, idade, características clínicas, sítio do tumor, história médica relevante, achados radiográficos, achados histopatológicos, achados imuno‐histoquímico, tratamentos instituídos e prognóstico.
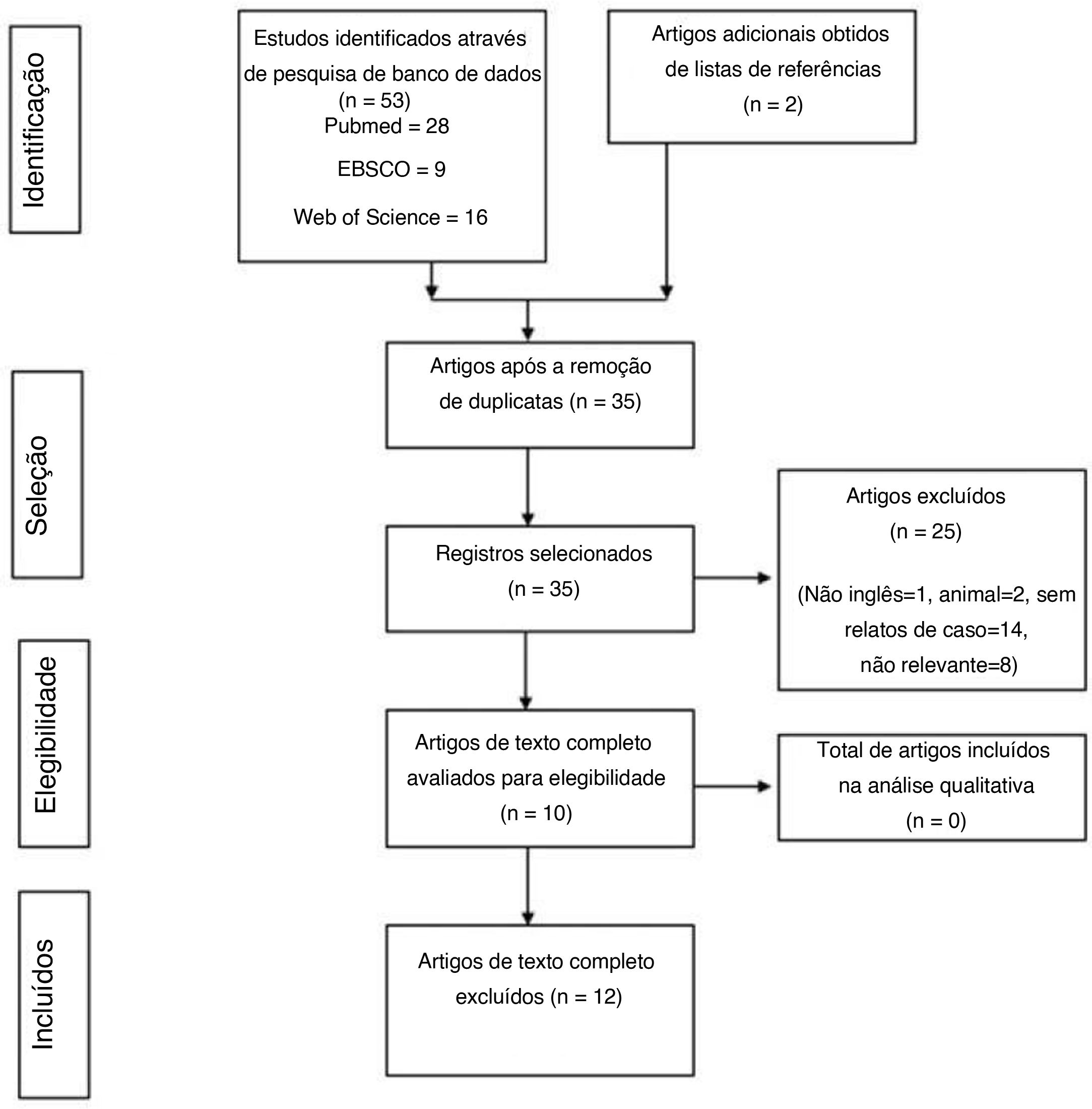
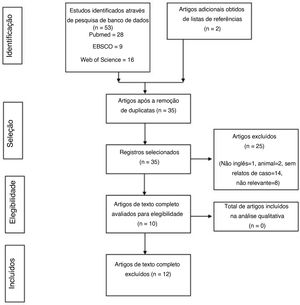
ResultadosA pesquisa bibliográfica foi feita em 9 de maio de 2020. Foram recuperados 53 títulos das bases de dados (16 artigos do WoS, 9 artigos do Ebsco, 28 artigos do PubMed). Após a remoção das duplicatas, 35 resumos foram selecionados para triagem. No processo de identificação de artigos relevantes, várias citações foram excluídas. Essas citações incluíam artigos não escritos na língua inglesa (n = 1), relatos de casos em animais (n = 2), artigos que não eram relatos de casos (n = 14) e artigos não relevantes (n = 8). Após a exclusão, 10 artigos com texto completo foram avaliados e incluídos na revisão. Dois artigos adicionais foram recuperados pela pesquisa de referências. No total, 12 artigos com 14 casos de SOC foram incluídos para revisão (fig. 1).
De acordo com os dados, foi observada uma ligeira predileção pelo sexo feminino. Oito casos foram relatados em mulheres, enquanto os 6 casos restantes foram relatados em homens. A idade dos pacientes com diagnóstico de SOC variou de 31 a 73 anos, com média de 54,4 anos. A maioria dos casos ocorreu durante a 5ª e a 7ª décadas, com preponderância feminina na 5ª década, enquanto o sexo masculino predominou na 7ª década de vida. A mandíbula parece ser o local preferido em comparação com a maxila, pois 9 casos foram encontrados na mandíbula. Dos 9 casos, 7 foram relatados na mandíbula posterior, enquanto apenas 2 casos ocorreram na mandíbula anterior. Entre os casos maxilares, 3 tumores foram relatados na maxila anterior, enquanto 2 foram relatados na maxila posterior.
Na maioria desses casos, a história médica não era digna de nota, exceto em um paciente que tinha história de carcinoma hepatocelular e outra que havia sido submetida a cirurgia para redução de mamas. Os pacientes geralmente apresentavam edema ou nódulo, com crescimento progressivo e rápido. Nem sempre dor era sintoma desse tumor, pois havia casos assintomáticos. Os tumores que afetam a mandíbula, principalmente a região posterior, podem se apresentar com parestesia, como relatado em 3 casos. Dependendo do grau de destruição óssea, os dentes dentro e ao redor do tumor podem apresentar mobilidade. Um resumo das características clínicas dos casos relatados é mostrado na tabela 1.
Características clínicas dos casos relatados de carcinoma odontogênico esclerosante
| Autores, ano | N° de casos | Idade, sexo | Apresentação Clínica | História Médica | Local | Diagnóstico inicial | Conduta | Seguimento |
|---|---|---|---|---|---|---|---|---|
| Seyiti et al., 20205 | 1 | 54, Feminino | Edema firme e progressivo, parestesia lábio inferior, dor | N/A | Mandíbula posterior esquerda | Osteomielite de Garrè | Ressecção e retalho de fíbula | N/A |
| O’ Connor et al., 20196 | 1 | 43, Feminino | Fenda entre 12 e 13, assintomática | N/A | Maxila anterior | SOC | Tratamento inicial ‐ Enucleação, seguida de ressecção (maxilectomia) | Sem recorrência; 12 meses |
| Sem quimio/radioterapia | ||||||||
| Todorovic et al., 20197 | 1 | 62, Masculino | Edema progressivo, afrouxamento dos dentes, infecção recorrente dos seios da face | Carcinoma Hepatocelular | Maxila esquerda | Lesão fibro‐óssea benigna | Maxilectomia esquerda + remoção da fossa infratemporal e base do crânio | Recorrência 5 meses após ressecção. |
| Recorrência ‐ Radioterapia (66Gy / 33 frações) | Sem recorrência 9 meses após radioterapia. | |||||||
| Kataoka et al., 20188 | 1 | 68, Feminino | Edema rápido da mandíbula anterior, sem parestesia, | N/A | Mandíbula anterior | Tumor odontogênico epitelial benigno | Ressecção | Sem recorrência; 5 anos |
| Hanisch et al., 20179 | 1 | 60, Masculino | Edema na região pré‐molar / molar da mandíbula esquerda, sem parestesia, | N/A | Mandíbulaesquerda | CEC de baixo grau | Hemi‐mandibulectomia esquerda, esvaziamento cervical radical ipsilateral | Sem recorrência; 9 meses |
| Wood et al., 201610 | 1 | 43, Feminino | Nódulo firme assintomático | Redução da mama direita | Palato duro anterior direito | Adenocarcinoma sem outra especificação ‐ NOS ‐ (not otherwise specified) | Maxilectomia | Sem recorrência; 17 meses |
| Tan et al., 201411 | 1 | 31, Feminino | Nódulo assintomático | N/A | Mandíbula anterior | Não mencionado | Enucleação | Sem recorrência; 1 ano |
| Saxena et al., 201312 | 1 | 42, Masculino | Edema firme a duro, semelhante a osso, na área parassinfisária esquerda, sem parestesia | N/A | Mandíbula esquerda | Variante rica em epitélio de fibroma odontogênico central | Hemi‐mandibulectomia, esvaziamento cervical radical, radioterapia | Sem recorrência; 10 meses |
| Hussain et al., 201313 | 1 | 54, Masculino | Edema expansível firme | N/A | Maxila anterior | Carcinoma espinocelular, provavelmente de origem metastática | Ressecção | Sem recorrência; 19 meses |
| Irié et al., 201014 | 1 | 67, Masculino | Parestesia no lábio inferior esquerdo e pele da região mentual | N/A | Mandíbula esquerda | Lesão fibro‐óssea benigna | Primeira cirurgia ‐ curetagem | Recorrência; 8 meses após curetagem. |
| Recorrência ‐ mandibulectomia segmentar esquerda, quimioterapia | Sem recorrência; 15 meses após ressecção | |||||||
| Ide et al., 200915 | 1 | 47, Feminino | Massa de 2cm na gengiva lingual inferior esquerda | N/A | Mandíbula esquerda | Carcinoma odontogênico intraósseo primário com dentinóide | Ressecção, dissecção de linfonodos cervicais | Sem recorrência; 6 anos |
| Koutlas et al., 20082 | 3 | 72, Masculino | Massa mandibular esquerda aumentada e parestesia do nervo mentual | N/A | Mandíbula esquerda | SOC | Ressecção e esvaziamento cervical | Sem recorrência; 5 anos |
| 46, Feminino | Lesão mandibular direita dolorosa | N/A | Mandíbula direita | SOC | Ressecção | Sem recorrência; 12 anos | ||
| 73, Feminino | Aumento da maxila | N/A | Maxila direita | CEC Tipo 3 pouco diferenciado | Ressecção e radioterapia | Sem recorrência; 3,5 anos |
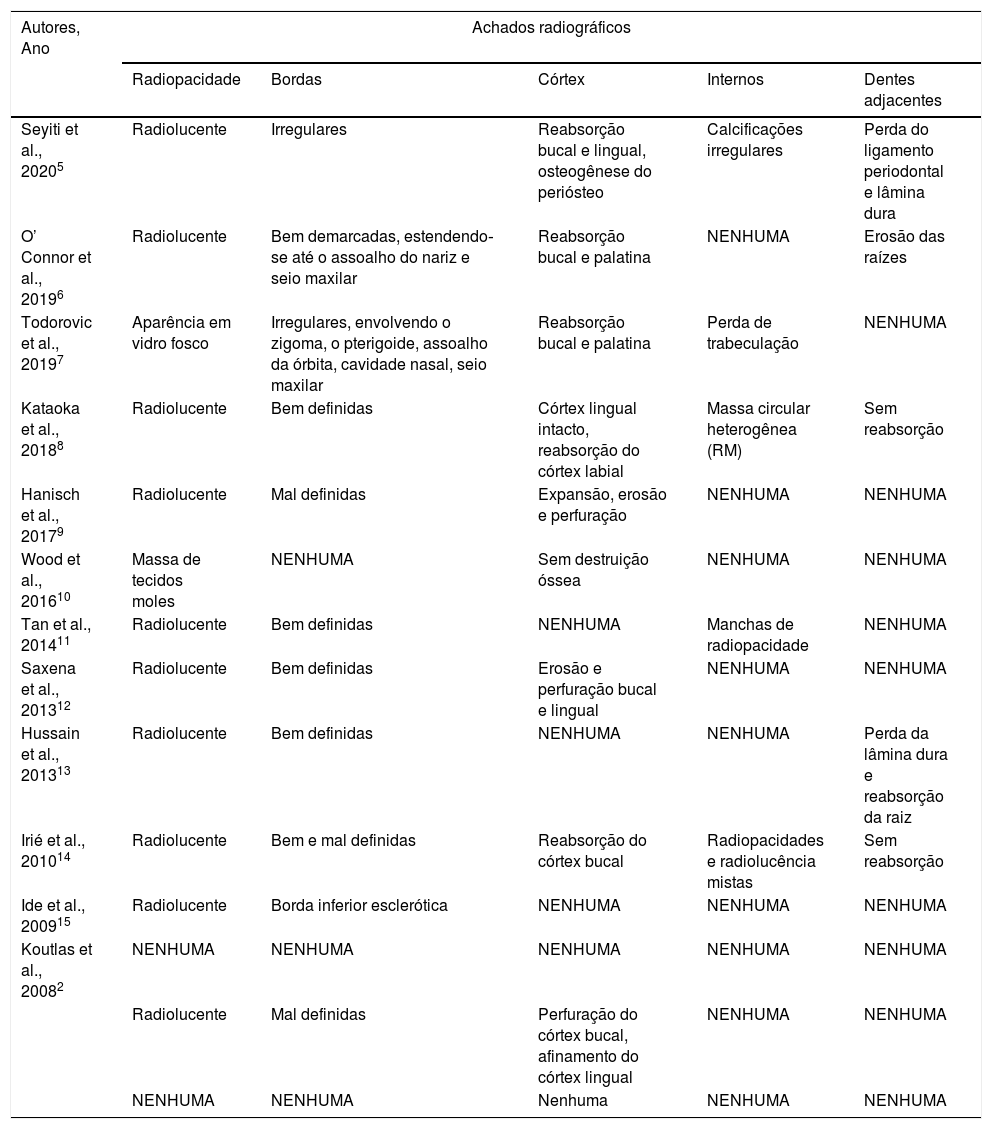
Em geral, esse tumor se apresenta como uma lesão radiolúcida na radiografia. Entretanto, foi relatado que um dos casos apresentava aspecto em vidro fosco. As margens podem aparecer como bem definidas, mal definidas ou uma combinação de ambas. Notou‐se que dois casos na maxila envolviam estruturas adjacentes, como cavidade nasal, seio maxilar, zigoma e placas pterigoides. A reabsorção de pelo menos um dos córtices bucal /labial ou palatino/lingual foi relatada em todos os casos. A reabsorção das raízes dentárias e perda da lâmina dura foram relatadas em 3 casos, embora não tal reabsorção não tenha sido observada em dois outros casos. Os demais casos não mencionaram os efeitos nas raízes dentárias. As características radiográficas dos casos relatados são apresentadas na tabela 2. Entre os casos relatados, apenas dois casos foram diagnosticados como SOC desde o início. A maioria dos casos recebeu outros diagnósticos provisórios, como osteomielite de Garrè, lesão fibro‐óssea benigna, tumor odontogênico epitelial benigno, carcinoma espinocelular, adenocarcinoma, tumor metastático, carcinoma odontogênico de células claras e carcinoma intraósseo primário.
Achados radiográficos de casos relatados de carcinoma odontogênico esclerosante
| Autores, Ano | Achados radiográficos | ||||
|---|---|---|---|---|---|
| Radiopacidade | Bordas | Córtex | Internos | Dentes adjacentes | |
| Seyiti et al., 20205 | Radiolucente | Irregulares | Reabsorção bucal e lingual, osteogênese do periósteo | Calcificações irregulares | Perda do ligamento periodontal e lâmina dura |
| O’ Connor et al., 20196 | Radiolucente | Bem demarcadas, estendendo‐se até o assoalho do nariz e seio maxilar | Reabsorção bucal e palatina | NENHUMA | Erosão das raízes |
| Todorovic et al., 20197 | Aparência em vidro fosco | Irregulares, envolvendo o zigoma, o pterigoide, assoalho da órbita, cavidade nasal, seio maxilar | Reabsorção bucal e palatina | Perda de trabeculação | NENHUMA |
| Kataoka et al., 20188 | Radiolucente | Bem definidas | Córtex lingual intacto, reabsorção do córtex labial | Massa circular heterogênea (RM) | Sem reabsorção |
| Hanisch et al., 20179 | Radiolucente | Mal definidas | Expansão, erosão e perfuração | NENHUMA | NENHUMA |
| Wood et al., 201610 | Massa de tecidos moles | NENHUMA | Sem destruição óssea | NENHUMA | NENHUMA |
| Tan et al., 201411 | Radiolucente | Bem definidas | NENHUMA | Manchas de radiopacidade | NENHUMA |
| Saxena et al., 201312 | Radiolucente | Bem definidas | Erosão e perfuração bucal e lingual | NENHUMA | NENHUMA |
| Hussain et al., 201313 | Radiolucente | Bem definidas | NENHUMA | NENHUMA | Perda da lâmina dura e reabsorção da raiz |
| Irié et al., 201014 | Radiolucente | Bem e mal definidas | Reabsorção do córtex bucal | Radiopacidades e radiolucência mistas | Sem reabsorção |
| Ide et al., 200915 | Radiolucente | Borda inferior esclerótica | NENHUMA | NENHUMA | NENHUMA |
| Koutlas et al., 20082 | NENHUMA | NENHUMA | NENHUMA | NENHUMA | NENHUMA |
| Radiolucente | Mal definidas | Perfuração do córtex bucal, afinamento do córtex lingual | NENHUMA | NENHUMA | |
| NENHUMA | NENHUMA | Nenhuma | NENHUMA | NENHUMA | |
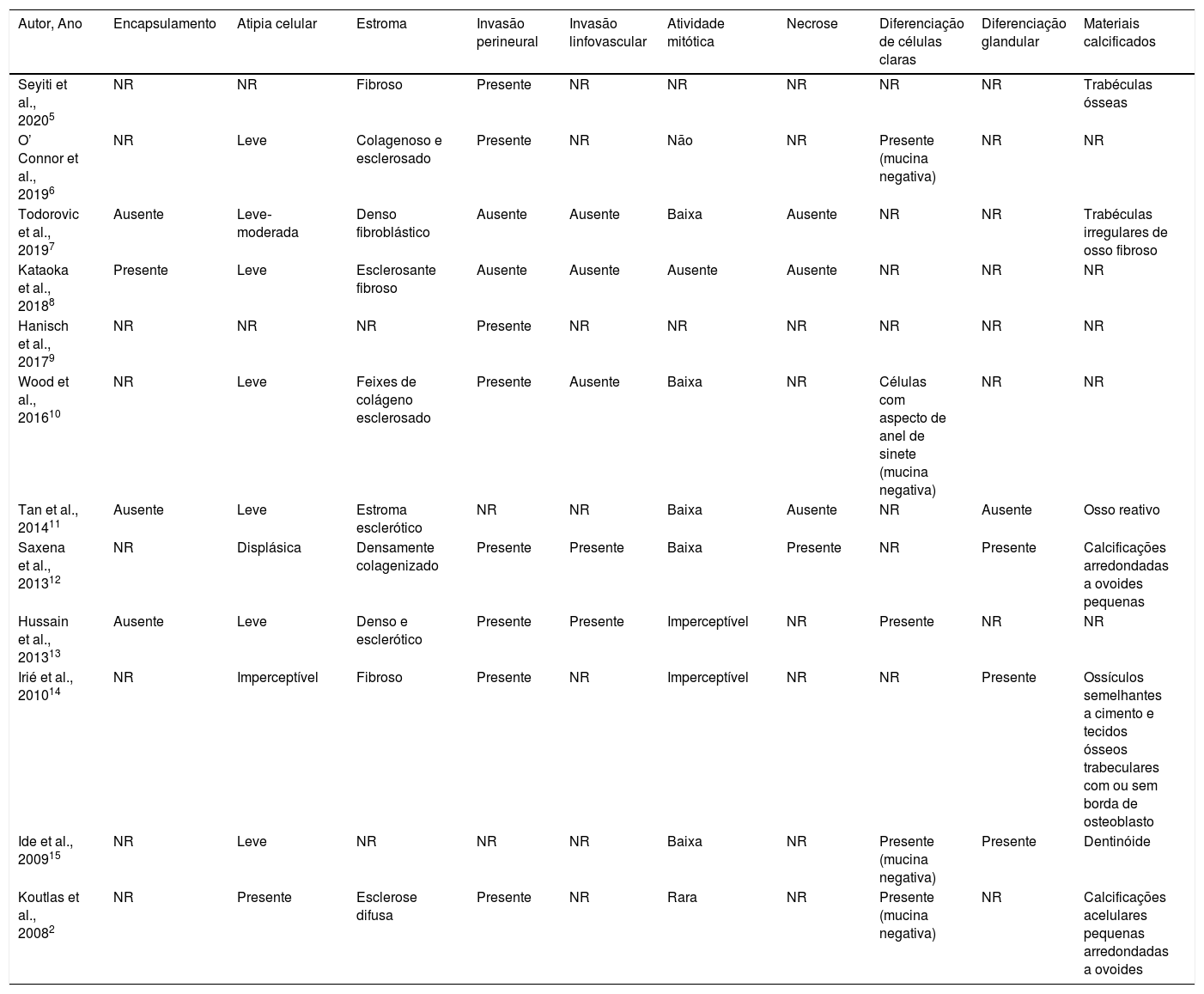
Histopatologicamente, as células neoplásicas eram compostas por cordões finos em fila única, filamentos e ilhas de células epitelioides. Houve apenas um caso documentado com cápsula fibrosa que envolvia o tumor. Os outros casos foram relatados com um padrão de crescimento tumoral infiltrativo e ausência de encapsulamento. Em geral, um grau leve de atipia celular foi observado em 10 casos. Um componente estromal denso, fibroso, colagenoso ou esclerótico foi a característica marcante observada em 12 casos. Invasão perineural ou intraneural foi relatada em 8 casos, enquanto 2 casos não relataram evidência de invasão perineural. Invasão linfovascular foi observada em 2 casos. A atividade mitótica relatada foi imperceptível ou baixa na maioria dos casos. A necrose foi evidente em um dos 14 casos relatados. Diferenciação de células claras foi observada em 5 casos e testes posteriores demonstraram a ausência de mucina nessas células. A diferenciação glandular foi relatada em 3 casos. Tecido calcificado que consistia em componentes ósseos, cementoides ou dentinoides foi documentado em 7 casos. Um resumo das características histopatológicas dos casos relatados é mostrado na tabela 3.
Achados histológicos de casos relatados de carcinoma odontogênico esclerosante
| Autor, Ano | Encapsulamento | Atipia celular | Estroma | Invasão perineural | Invasão linfovascular | Atividade mitótica | Necrose | Diferenciação de células claras | Diferenciação glandular | Materiais calcificados |
|---|---|---|---|---|---|---|---|---|---|---|
| Seyiti et al., 20205 | NR | NR | Fibroso | Presente | NR | NR | NR | NR | NR | Trabéculas ósseas |
| O’ Connor et al., 20196 | NR | Leve | Colagenoso e esclerosado | Presente | NR | Não | NR | Presente (mucina negativa) | NR | NR |
| Todorovic et al., 20197 | Ausente | Leve‐moderada | Denso fibroblástico | Ausente | Ausente | Baixa | Ausente | NR | NR | Trabéculas irregulares de osso fibroso |
| Kataoka et al., 20188 | Presente | Leve | Esclerosante fibroso | Ausente | Ausente | Ausente | Ausente | NR | NR | NR |
| Hanisch et al., 20179 | NR | NR | NR | Presente | NR | NR | NR | NR | NR | NR |
| Wood et al., 201610 | NR | Leve | Feixes de colágeno esclerosado | Presente | Ausente | Baixa | NR | Células com aspecto de anel de sinete (mucina negativa) | NR | NR |
| Tan et al., 201411 | Ausente | Leve | Estroma esclerótico | NR | NR | Baixa | Ausente | NR | Ausente | Osso reativo |
| Saxena et al., 201312 | NR | Displásica | Densamente colagenizado | Presente | Presente | Baixa | Presente | NR | Presente | Calcificações arredondadas a ovoides pequenas |
| Hussain et al., 201313 | Ausente | Leve | Denso e esclerótico | Presente | Presente | Imperceptível | NR | Presente | NR | NR |
| Irié et al., 201014 | NR | Imperceptível | Fibroso | Presente | NR | Imperceptível | NR | NR | Presente | Ossículos semelhantes a cimento e tecidos ósseos trabeculares com ou sem borda de osteoblasto |
| Ide et al., 200915 | NR | Leve | NR | NR | NR | Baixa | NR | Presente (mucina negativa) | Presente | Dentinóide |
| Koutlas et al., 20082 | NR | Presente | Esclerose difusa | Presente | NR | Rara | NR | Presente (mucina negativa) | NR | Calcificações acelulares pequenas arredondadas a ovoides |
NR, não relatado.
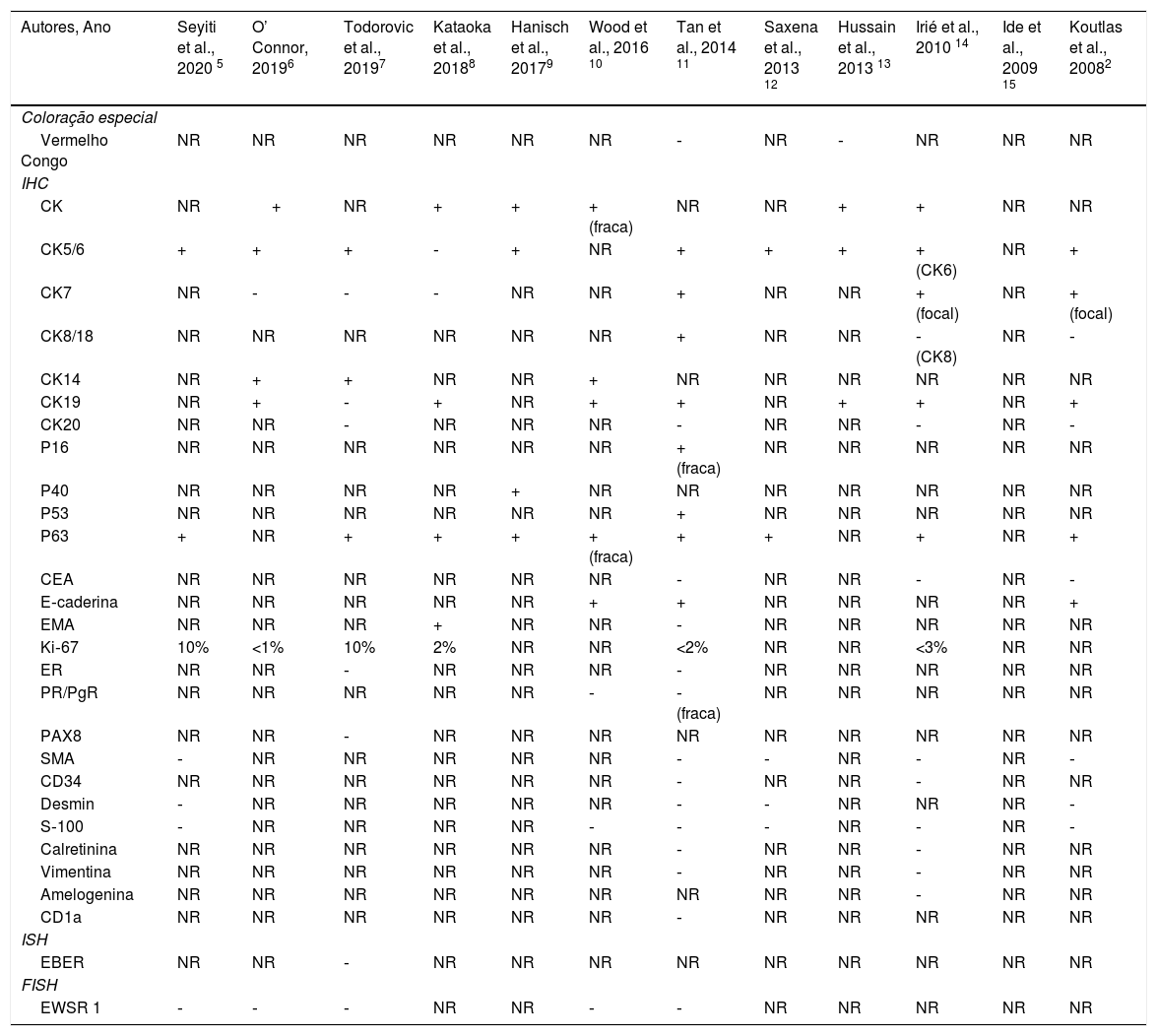
A coloração especial com vermelho Congo foi feita em 2 casos e produziu resultados negativos. Imuno‐histoquimicamente, AE1/AE3 ou pan‐CK, CK5/6, CK14, CK19, p63 e E‐caderina foram os marcadores amplamente expressos. CK8/18 e CK7 foram expressos de forma variável nos casos relatados. A coloração com Ki‐67 mostrou baixo índice proliferativo em 6 casos. A imunocoloração para p16, p40, p53, EMA e PR foi relatada como positiva em um único caso cada. A imunocoloração para CEA, ER, PAX8, SMA, CD34, desmina, proteína S‐100, calretinina, vimentina, amelogenina e CD1a produziu resultados negativos. Os estudos moleculares para o rearranjo EWSR1 foram negativos em 5 casos. A tabela 4 resume os achados imuno‐histoquímicos dos casos relatados.
Achados imuno‐histoquímicos de casos relatados de carcinoma odontogênico esclerosante
| Autores, Ano | Seyiti et al., 2020 5 | O’ Connor, 20196 | Todorovic et al., 20197 | Kataoka et al., 20188 | Hanisch et al., 20179 | Wood et al., 2016 10 | Tan et al., 2014 11 | Saxena et al., 2013 12 | Hussain et al., 2013 13 | Irié et al., 2010 14 | Ide et al., 2009 15 | Koutlas et al., 20082 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Coloração especial | ||||||||||||
| Vermelho Congo | NR | NR | NR | NR | NR | NR | ‐ | NR | ‐ | NR | NR | NR |
| IHC | ||||||||||||
| CK | NR | + | NR | + | + | +(fraca) | NR | NR | + | + | NR | NR |
| CK5/6 | + | + | + | ‐ | + | NR | + | + | + | + (CK6) | NR | + |
| CK7 | NR | ‐ | ‐ | ‐ | NR | NR | + | NR | NR | + (focal) | NR | + (focal) |
| CK8/18 | NR | NR | NR | NR | NR | NR | + | NR | NR | ‐ (CK8) | NR | ‐ |
| CK14 | NR | + | + | NR | NR | + | NR | NR | NR | NR | NR | NR |
| CK19 | NR | + | ‐ | + | NR | + | + | NR | + | + | NR | + |
| CK20 | NR | NR | ‐ | NR | NR | NR | ‐ | NR | NR | ‐ | NR | ‐ |
| P16 | NR | NR | NR | NR | NR | NR | +(fraca) | NR | NR | NR | NR | NR |
| P40 | NR | NR | NR | NR | + | NR | NR | NR | NR | NR | NR | NR |
| P53 | NR | NR | NR | NR | NR | NR | + | NR | NR | NR | NR | NR |
| P63 | + | NR | + | + | + | +(fraca) | + | + | NR | + | NR | + |
| CEA | NR | NR | NR | NR | NR | NR | ‐ | NR | NR | ‐ | NR | ‐ |
| E‐caderina | NR | NR | NR | NR | NR | + | + | NR | NR | NR | NR | + |
| EMA | NR | NR | NR | + | NR | NR | ‐ | NR | NR | NR | NR | NR |
| Ki‐67 | 10% | <1% | 10% | 2% | NR | NR | <2% | NR | NR | <3% | NR | NR |
| ER | NR | NR | ‐ | NR | NR | NR | ‐ | NR | NR | NR | NR | NR |
| PR/PgR | NR | NR | NR | NR | NR | ‐ | ‐(fraca) | NR | NR | NR | NR | NR |
| PAX8 | NR | NR | ‐ | NR | NR | NR | NR | NR | NR | NR | NR | NR |
| SMA | ‐ | NR | NR | NR | NR | NR | ‐ | ‐ | NR | ‐ | NR | ‐ |
| CD34 | NR | NR | NR | NR | NR | NR | ‐ | NR | NR | ‐ | NR | NR |
| Desmin | ‐ | NR | NR | NR | NR | NR | ‐ | ‐ | NR | NR | NR | ‐ |
| S‐100 | ‐ | NR | NR | NR | NR | ‐ | ‐ | ‐ | NR | ‐ | NR | ‐ |
| Calretinina | NR | NR | NR | NR | NR | NR | ‐ | NR | NR | ‐ | NR | NR |
| Vimentina | NR | NR | NR | NR | NR | NR | ‐ | NR | NR | ‐ | NR | NR |
| Amelogenina | NR | NR | NR | NR | NR | NR | NR | NR | NR | ‐ | NR | NR |
| CD1a | NR | NR | NR | NR | NR | NR | ‐ | NR | NR | NR | NR | NR |
| ISH | ||||||||||||
| EBER | NR | NR | ‐ | NR | NR | NR | NR | NR | NR | NR | NR | NR |
| FISH | ||||||||||||
| EWSR 1 | ‐ | ‐ | ‐ | NR | NR | ‐ | ‐ | NR | NR | NR | NR | NR |
NR, não relatado; (+), positivo; (‐), negativo.
A cirurgia radical foi a modalidade de tratamento preferida. Essas cirurgias incluíram ressecção, hemimandibulectomia e maxilectomia. Esvaziamentos cervicais concomitantes foram feitos em 4 casos. A radioterapia adjuvante foi usada em 2 casos, enquanto a recorrência foi relatada em 2 casos. A recorrência ocorreu relativamente cedo após a primeira cirurgia. Um caso apresentou recidiva após 5 meses, enquanto em outro a recidiva ocorreu no 8° mês do pós‐operatório. O primeiro caso apresentava um tumor extenso no qual foram feitas maxilectomia esquerda e remoção da fossa infratemporal e da base do crânio. Após a recorrência, foi administrada radioterapia (66Gy em 33 frações). Nenhuma recorrência foi observada após 9 meses de seguimento. Em outro caso, o tumor foi inicialmente tratado com curetagem. Hemimandibulectomia segmentar como segunda cirurgia e quimioterapia foram feitas; o paciente permaneceu livre de tumor por 15 meses após a segunda cirurgia. Nenhuma recorrência foi observada nos demais casos, inclusive um caso que foi tratado apenas por enucleação. Os períodos de seguimento variaram de 9 meses a 12 anos. Não foram relatadas metástases.
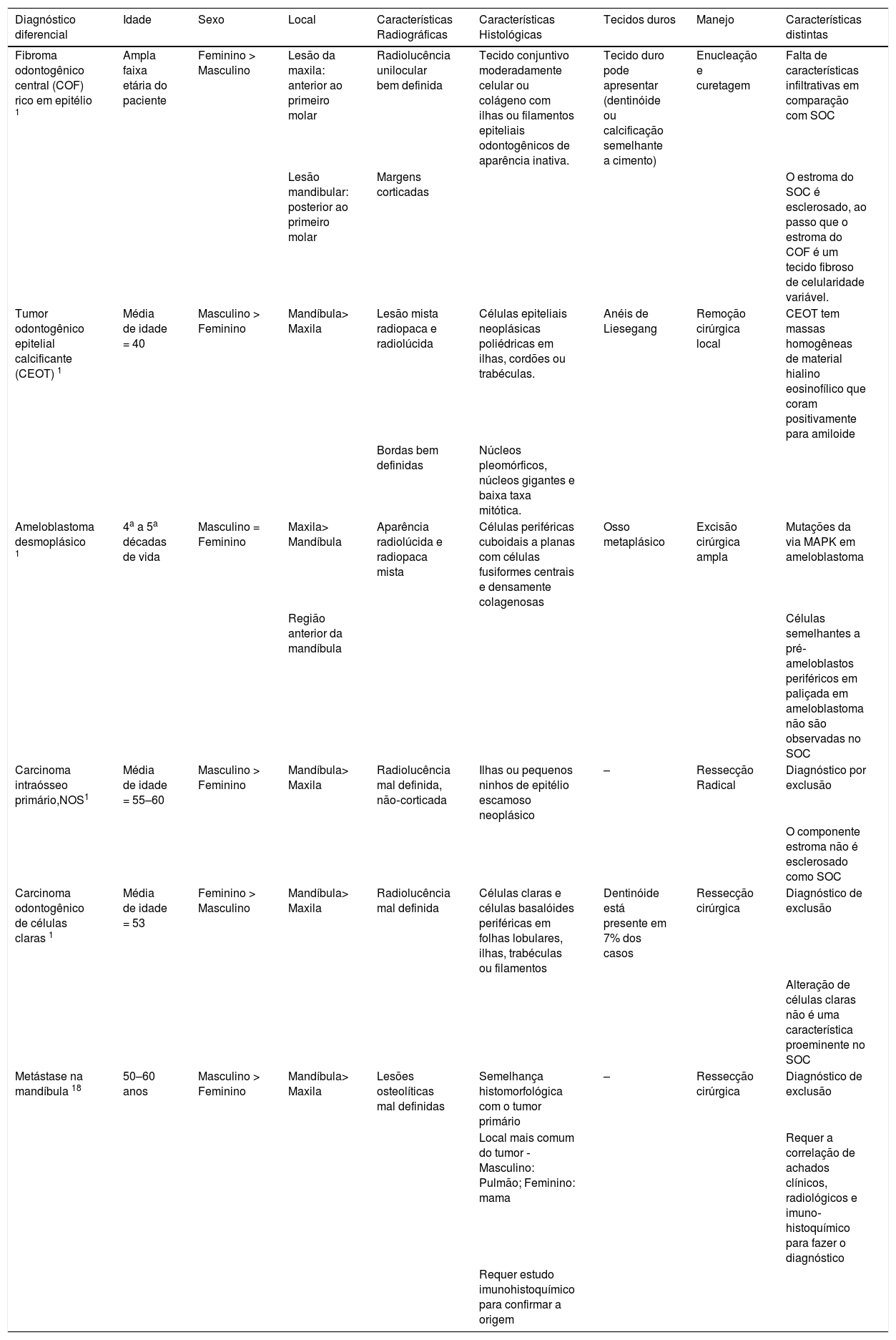
DiscussãoApesar de ser uma lesão controversa, em 2017, a OMS incluiu o SOC como um novo tumor odontogênico de cabeça e pescoço, embora alguns não estivessem convencidos de o SOC fosse uma nova entidade.16 Se o SOC é uma entidade distinta ou simplesmente um padrão histológico diferente permanece uma questão preocupante. Entretanto, a OMS foi de opinião que o SOC merecia reconhecimento como uma entidade individual.1 Entretanto, a definição de SOC pela OMS é controversa no contexto do carcinoma intraósseo primário, pois esse é uma entidade separada e distinta incluída na categoria de carcinomas odontogênicos. A definição atual levaria os leitores à ideia errônea de que o SOC é uma das variantes do carcinoma intraósseo primário. Ele deve ser identificado como carcinoma odontogênico em vez de carcinoma intraósseo primário, o qual é uma entidade separada definível na classificação. O diagnóstico de SOC é desafiador, pois compartilha algumas características com outros tumores, como fibroma odontogênico, ameloblastoma desmoplásico, tumor odontogênico epitelial calcificado, carcinoma intraósseo primário, carcinoma odontogênico de células claras e tumores metastáticos na mandíbula.1,17,18 Os diagnósticos diferenciais de SOC acima sugerem que o tumor pode ter um amplo espectro em termos de graduação de malignidade. As características desses possíveis diagnósticos diferenciais estão resumidas na tabela 5.
Características dos diagnósticos diferenciais do carcinoma odontogênico esclerosante
| Diagnóstico diferencial | Idade | Sexo | Local | Características Radiográficas | Características Histológicas | Tecidos duros | Manejo | Características distintas |
|---|---|---|---|---|---|---|---|---|
| Fibroma odontogênico central (COF) rico em epitélio 1 | Ampla faixa etária do paciente | Feminino > Masculino | Lesão da maxila: anterior ao primeiro molar | Radiolucência unilocular bem definida | Tecido conjuntivo moderadamente celular ou colágeno com ilhas ou filamentos epiteliais odontogênicos de aparência inativa. | Tecido duro pode apresentar (dentinóide ou calcificação semelhante a cimento) | Enucleação e curetagem | Falta de características infiltrativas em comparação com SOC |
| Lesão mandibular: posterior ao primeiro molar | Margens corticadas | O estroma do SOC é esclerosado, ao passo que o estroma do COF é um tecido fibroso de celularidade variável. | ||||||
| Tumor odontogênico epitelial calcificante (CEOT) 1 | Média de idade = 40 | Masculino > Feminino | Mandíbula> Maxila | Lesão mista radiopaca e radiolúcida | Células epiteliais neoplásicas poliédricas em ilhas, cordões ou trabéculas. | Anéis de Liesegang | Remoção cirúrgica local | CEOT tem massas homogêneas de material hialino eosinofílico que coram positivamente para amiloide |
| Bordas bem definidas | Núcleos pleomórficos, núcleos gigantes e baixa taxa mitótica. | |||||||
| Ameloblastoma desmoplásico 1 | 4a a 5a décadas de vida | Masculino = Feminino | Maxila> Mandíbula | Aparência radiolúcida e radiopaca mista | Células periféricas cuboidais a planas com células fusiformes centrais e densamente colagenosas | Osso metaplásico | Excisão cirúrgica ampla | Mutações da via MAPK em ameloblastoma |
| Região anterior da mandíbula | Células semelhantes a pré‐ameloblastos periféricos em paliçada em ameloblastoma não são observadas no SOC | |||||||
| Carcinoma intraósseo primário,NOS1 | Média de idade = 55–60 | Masculino > Feminino | Mandíbula> Maxila | Radiolucência mal definida, não‐corticada | Ilhas ou pequenos ninhos de epitélio escamoso neoplásico | – | Ressecção Radical | Diagnóstico por exclusão |
| O componente estroma não é esclerosado como SOC | ||||||||
| Carcinoma odontogênico de células claras 1 | Média de idade = 53 | Feminino > Masculino | Mandíbula> Maxila | Radiolucência mal definida | Células claras e células basalóides periféricas em folhas lobulares, ilhas, trabéculas ou filamentos | Dentinóide está presente em 7% dos casos | Ressecção cirúrgica | Diagnóstico de exclusão |
| Alteração de células claras não é uma característica proeminente no SOC | ||||||||
| Metástase na mandíbula 18 | 50–60 anos | Masculino > Feminino | Mandíbula> Maxila | Lesões osteolíticas mal definidas | Semelhança histomorfológica com o tumor primário | – | Ressecção cirúrgica | Diagnóstico de exclusão |
| Local mais comum do tumor ‐ Masculino: Pulmão; Feminino: mama | Requer a correlação de achados clínicos, radiológicos e imuno‐histoquímico para fazer o diagnóstico | |||||||
| Requer estudo imunohistoquímico para confirmar a origem |
As características clínicas relatadas estão no espectro de comportamento indolente a agressivo, que causa dificuldade de decidir se uma malignidade está presente no ambiente clínico de alguns dos casos. Histopatologicamente, o SOC classicamente apresenta‐se como células epiteliais citologicamente brandas dentro do estroma esclerótico.1 Essas duas características são diretrizes para o diagnóstico de um tumor benigno, em vez de uma malignidade. Dos casos relatados, o grau de atipia celular foi leve e a atividade mitótica geralmente estava ausente ou baixa. Permanece controverso se se deve ou não rotular o pleomorfismo celular e nuclear imperceptível e a atividade mitótica duvidosa como indicativo de uma malignidade para SOC. Foi documentado que a invasão perineural é uma característica do SOC.1 Essa característica, entretanto, foi relatada em 8 casos, enquanto a ausência de invasão perineural foi relatada nos demais. A presença de invasão perineural é um fator prognóstico histopatológico reconhecido no carcinoma espinocelular oral e orofaríngeo.19,20 A invasão perineural é um achado histopatológico comum para malignidade de alto grau e resulta em desfechos clínicos ruins, recorrência regional, metástase a distância e mortalidade.19 Mais casos são necessários para avaliar se a invasão perineural é uma característica histopatológica particular do SOC e para validá‐la como uma característica usada para a graduação da malignidade.
Cinco casos relataram uma população de células claras no SOC e outros testes confirmaram a presença de glicogênio intracitoplasmático. Esse achado apoia a origem odontogênica do SOC, uma vez que remanescentes da lâmina dentária e os restos de Malassez dariam origem à aparência de células claras no tecido da lesão.21 Curiosamente, um componente de tecido duro foi observado em metade dos casos relatados. A associação entre calcificações semelhantes a lesões fibro‐ósseas benignas e a presença de tecido dentário duro ainda não foi investigada. Nossa hipótese é que a formação de tecido dentário duro pode ser atribuída à origem odontogênica do SOC e sua capacidade pluripotente de sintetizar tecido dentário duro.
As células epiteliais neoplásicas em SOC foram coradas positivamente com pan‐CK, CK5/6, CK14, CK19 e p63. A citoqueratina (CK) é um marcador específico da linhagem de células epiteliais. As células epiteliais expressam diferentes subtipos de citoqueratina, depende do estágio de desenvolvimento e do estágio na sequência de diferenciação terminal.22 A literatura disponível mostra que o SOC expressou principalmente citoqueratina de alto peso molecular, a saber, CK5/6 e CK14. Esse achado é consistente com os de Crivelini et al.23 (2003). Eles documentaram que o marcador imuno‐histoquímico típico para o epitélio odontogênico é a CK14. A CK19 é uma citoqueratina de baixo peso molecular e frequentemente destaca células epiteliais próximas ao epitélio de superfície ou diferenciação escamosa.23 Esse marcador, entretanto, foi inesperadamente negativo no caso relatado por Todorovic et al.7 Mais esclarecimentos sobre a coloração do subtipo de citoqueratina seriam benéficos para identificar a expressão de citoqueratina relacionada à sua histogênese. Biomarcadores preditivos como o Ki‐67, amplamente usados para avaliar o índice proliferativo de um tumor, parecem ser um achado não significativo para SOC. Portanto, o exame histopatológico continua a ser o padrão‐ouro no diagnóstico de SOC, uma vez que nenhum marcador específico além da citoqueratina foi identificado até o momento.
O EWSR1 é o gene mais comum que pode gerar vários genes de fusão e é evidente em uma variedade de neoplasias. Os tumores que contêm rearranjos do gene EWSR1 incluem o sarcoma de Ewing, lipossarcoma mixóide, sarcomas de células claras e neoplasias mioepiteliais.24 Para a região da cabeça e pescoço, foi relatado que o carcinoma mucoepidermoide, o carcinoma de células claras e o carcinoma mioepitelial apresentam rearranjo do gene EWSR1.1 Cinco casos relatados de SOC foram submetidos ao estudo molecular FISH para rearranjo do gene EWSR1 e produziram resultados negativos. Isso poderia levar à postulação de que o SOC não exibe rearranjo do gene EWSR1.
Com base na literatura disponível, seria seguro recomendar a ressecção do tumor com uma margem de 5mm e um seguimento rigoroso após a cirurgia.13 O esvaziamento cervical não é obrigatório e a quimiorradioterapia pode não ter um papel curativo, pois a maioria dos pacientes não foi submetida a esses procedimentos, mas permaneceu livre da doença durante todo o período de seguimento. A presença de metástases não foi relatada até agora. Isso pode estar relacionado às características de baixo grau dos componentes epiteliais e estromais, inclusive sua baixa atividade mitótica.7 Saxena et al.25 também postularam que o estroma denso ao redor do componente epitelial do tumor pode ter um papel na prevenção de metástases. O papel do tratamento adjuvante não pode ser justificado no momento.
ConclusãoCom base no número limitado de casos, podemos concluir que o SOC é um carcinoma de baixo grau sem potencial metastático que pode ser tratado adequadamente com ressecção local do tumor. No entanto, são necessárias mais informações para determinar o grau definitivo de malignidade. Os autores são de opinião que o SOC deveria ser definido como um carcinoma odontogênico separado, em vez de um carcinoma intraósseo primário.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Como citar este artigo: Lim D, Tan CC, Tilakaratne WM, Goh YC. Sclerosing odontogenic carcinoma – review of all published cases: is it a justifiable addition as a malignancy? Braz J Otorhinolaryngol. 2022;88:118–29.