A apneia obstrutiva do sono é uma doença comum na infância que pode trazer consequências importantes para a saúde e qualidade de vida das crianças. O exame padrão‐ouro para o diagnóstico (polissonografia) é um exame caro, complexo e disponível em poucos centros. O pediatric sleep questionnaire, PSQ, tem demonstrado ser um bom teste de triagem para apneia obstrutiva do sono, por ser um questionário simples e com boa sensibilidade e especificidade quando comparado à polissonografia nos países em que foi validado.
ObjetivoTradução e adaptação transcultural do PSQ para o português do Brasil.
MétodoFoi feita a tradução do PSQ para o português do Brasil, de acordo com as boas práticas. O questionário validado e adaptado foi aplicado aos pais/responsáveis de 60 crianças com 2–18 anos, 40 com apneia obstrutiva do sono e 20 controles. O reteste foi feito em 30 crianças com apneia obstrutiva do sono. Foram avaliados: consistência interna, teste‐reteste, validação do conteúdo e acurácia do questionário, pela curva ROC (do inglês receiver operating characteristic curve).
ResultadosO PSQ‐Brasil apresentou alta consistência interna, pelo coeficiente Alfa de Cronbach (0,86 para o teste total; 0,83 para o subdomínio “ronco”; 0,64 para “sonolência” e 0,65 para “comportamento”. O teste‐reteste teve concordância de 0,89 para o subdomínio “ronco”; 0,93 para sonolência” e 0,86 para “comportamento”. A acurácia medida pela curva ROC foi de 0,99. O valor de 9,0 foi considerado ideal para diferenciar os pacientes com apneia obstrutiva do sono e controles, com sensibilidade de 0,92 e especificidade de 1,0.
ConclusãoA tradução e adaptação transcultural do PSQ para o português do Brasil mostrou‐se bem‐sucedida. Em locais com dificuldade de acesso à polissonografia, o PSQ pode ser uma ferramenta útil na suspeição diagnóstica e seguimento das crianças com apneia obstrutiva do sono.
A AOS (apneia obstrutiva do sono) é uma doença relativamente comum na população infantil, com prevalência entre 1% e 5%.1 Está associada a considerável morbidade, que resulta em gastos elevados com visitas médicas e tratamentos,2 além de trazer consequências negativas para a saúde e qualidade de vida dos pacientes e suas famílias.3,4 Sabe‐se que a AOS na infância pode levar a comprometimento cardiovascular (predisposição a hipertensão arterial sistêmica),5 somático (menor crescimento pondero‐estatural)6 e neurocognitivo (desatenção na escola, hiperatividade e agressividade).7,8
Atualmente o exame padrão‐ouro para a AOS da Infância é a polissonografia1 feita em laboratório de sono, assistida por técnico de polissonografia durante pelo menos 6 horas com monitoração. São avaliados durante o sono os seguintes parâmetros: eletrooculografia, eletroencefalografia, cânulas de fluxo e termistores nasal e oral, eletrocardiografia, pulso oxímetro, e eletrodos musculares. Porém, é um exame demorado, caro, que exige equipamentos e pessoal especializado e frequentemente tem longas filas de espera.9 É pouco acessível à população geral, dificulta o diagnóstico, o seguimento e a feitura de assistência de qualidade e de pesquisas sobre esse tema.
O tratamento mais feito para crianças com AOS é a adenotonsilectomia.1 No entanto, alguns estudos vêm demonstrando índices cada vez maiores de AOS residual após a cirurgia. Brietzke e Gallagner10 publicaram uma metanálise em 2006 na qual a taxa de sucesso da adenoamigdalectomia foi de 82,9%, 17,1% dos pacientes necessitaram de novo tratamento. Em 2009, Friedman et al.11 publicaram uma revisão sistemática em que mostratam uma taxa de sucesso da adenoamigdalectomia de 59,8% e, mais recentemente, Lee et al.12 em 2016 publicaram revisão sistemática de 51 estudos, com 3.413 indivíduos, que mostrou uma taxa de sucesso da adenoamigdalectomia de 51%, taxa essa que diminui para 34% entre as crianças obesas.
Esses fatos, em conjunto, reforçam a importância do diagnóstico correto de AOS na infância, mas em contrapartida evidenciam a dificuldade de acesso à polissonografia em alguns sistemas de saúde, como o brasileiro. Nesse sentido, os testes de questionários têm surgido com alguma funcionalidade de triagem para diagnóstico de AOS, por serem fáceis de serem aplicados, rápidos e com boa relação custo‐benefício.
Existem vários questionários já publicados para esse propósito. Em um estudo comparativo recente, Burghard et al.13 identificaram 4 que foram considerados práticos e úteis como triagem de AOS em crianças. Os autores reforçaram ainda que, entre os 4 testes, o pediatric sleep questionnaire (PSQ) e o sleep clinical record (SCR) tinham ainda a vantagem de seguir as recomendações do European Respiratory Society Task Force, de 2016.14
A versão de distúrbios respiratórios relacionados ao sono do PSQ (do inglês SRBD‐PSQ, também conhecido como PSQ) é um questionário validado em inglês em 2000 por Chervin et al.,15 com o objetivo de facilitar a pesquisa clínica relacionada aos distúrbios respiratórios do sono na infância e também o acesso ao diagnóstico. Esse questionário, na sua língua pátria, demonstrou ter sensibilidade entre 81% e 85% e sensibilidade de 87% em identificar crianças com AOS moderada a grave quando comparada à polissonografia. O PSQ já foi traduzido para 12 idiomas,16,17 inclusive para o português de Portugal.18 Infelizmente, a versão portuguesa traz variações linguísticas que dificultam o uso no Brasil, principalmente em populações mais carentes.
O objetivo desse trabalho é tradução e adaptação transcultural do PSQ para o português do Brasil. Essa versão servirá como triagem para o diagnóstico da AOS da Infância, assim como para avaliar a melhoria clínica após tratamento, o que será de extrema importância, principalmente em centros assistenciais sem acesso à polissonografia no Brasil, além de facilitar a pesquisa relacionada aos distúrbios respiratórios do sono na infância nessa instituição e em outras no Brasil.
MétodoO questionário originalA versão de distúrbios respiratórios relacionados ao sono do PSQ (no inglês SRBD‐PSQ, também conhecido como PSQ) validada por Chervin et al.15 tem 22 questões voltadas a crianças com 2–18 anos e com suspeita de distúrbios respiratórios do sono. O questionário pode ser respondido pelo responsável da criança e é dividido em 3 domínios: o de ronco com 9 itens, o de sonolência com 7 itens e o de comportamento com 6 itens. As questões documentam a presença ou ausência de sintomas comuns como roncos, apneias presenciadas, dificuldade respiratória durante o sono, sonolência diurna, desatenção e hiperatividade. Respostas positivas tem pontuação de 1 e respostas negativas (“não” ou “não sei”) têm pontuação de 0. De acordo com os autores americanos, um valor de 8 ou mais respostas positivas é sugestivo de apneia do sono da infância.
Tradução do PSQA tradução do questionário para o português do Brasil foi feita de acordo com a metodologia proposta por Sagheri et al.,19 composta pelos seguintes passos:
- (a)
Tradução do questionário por 2 pessoas bilíngues cuja língua nativa é o português do Brasil, de forma independente. Um dos tradutores deve ser familiarizado com a área da pesquisa e ser da área médica (especialista) e o outro não,
- (b)
Estabelecimento de uma versão consensual entre as duas versões traduzidas. Para isso, os dois tradutores discutem a melhor versão final e essa discussão deve ser gravada por um observador,
- (c)
Tradução reversa para o inglês por 2 tradutores não especialistas cuja língua nativa seja o inglês, também de forma independente, e que não são conhecedores da versão original em inglês, e
- (d)
Avaliação da versão por um comitê de especialistas, composto por profissionais de saúde, e todos os tradutores envolvidos, para desenvolvimento de uma versão pré‐final para testes em campo. O objetivo é garantir uma tradução precisa e uma adaptação cultural apropriada.
Durante a reunião do comitê, as pequenas discrepâncias entre as diferentes versões foram avaliadas, confirmando que as traduções para o português e para o inglês foram adequadas. O comitê decidiu então sobre a versão final, para testes em pacientes. A versão final considerou a tradução conceitual com a linguagem mais simples possível, para que fosse aplicada à população no geral, em diferentes níveis de escolaridade.
O presente estudo foi aprovado pelo comitê de ética em pesquisa do Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto.
Validação intercultural do PSQPara avaliar a clareza, adequação e relevância cultural da versão em português do Brasil, a versão traduzida foi aplicada aos pais/responsáveis de uma amostra de 60 crianças entre 2 e 18 anos, 40 crianças acompanhadas no Centro Especializado do Respirador Bucal do Hospital das Clínicas de Ribeirão Preto, com diagnóstico de AOS comprovado por polissonografia; e 20 crianças acompanhadas em outros ambulatórios desse mesmo hospital e cujos pais negavam espontaneamente que seu filho tivesse problemas respiratórios durante o sono. Foram excluídas do estudo crianças com acometimento físico e mental grave ou pais/responsáveis que não sabiam ler/escrever.
Em um grupo de 30 dessas crianças, o questionário foi preenchido novamente após um período médio de 15 dias, para avaliação do teste‐reteste.
Análise estatísticaPara a população estudada em si, foi feita apenas análise descritiva dos dados, não tendo sido aplicada análise estatística comparativa entre os grupos.
Sobre os questionários preenchidos, foram aplicados os seguintes testes estatísticos, para avaliar o seu desempenho:
- ‐
Consistência interna, avaliando a homogeneidade entre os diferentes itens do questionário com o questionário total, através do teste alfa de Cronbach. Valores entre de 0,5 e 0,7 representam moderada confiabilidade e iguais a ou maiores do que 0,7 representam alta confiabilidade,20
- ‐
Teste‐reteste nos pacientes que preencheram duas vezes o questionário, através de teste de concordância de Kappa, onde valores entre 0,4–0,6 mostram concordância moderada; entre 0,6–0,8 demonstram concordância alta e acima de 0,8 possuem concordância quase perfeita. Para a análise dos subdomínios, foi usado o coeficiente de correlação intraclasse (ICC – do inglês intraclass correlation coefficient), foram adotados os mesmos valores acima para a análise,
- ‐
Validação de conteúdo, medida através do teste de correlação de Pearson para cada item do questionário, comparado ao valor do escore total. Valores acima de 0,3 têm correlação moderada e acima de 0,8 correlação forte.21
- ‐
Validação do questionário, mensurou a acurácia do questionário para diferenciar as crianças com AOS das crianças controles. Para isso, foi feito o teste de curva ROC (do inglês receiver operating characteristic curve) e determinada a área sob a curva (AUC – area under the curve) – quanto mais próximo de 1,0; maior a acurácia do questionário em diferenciar os grupos. Com essa análise, obteve‐se também o melhor valor de corte para o questionário, e qual a sensibilidade, a especificidade e a acurácia para que este valor diferencie o grupo portador de AOS do grupo controle.
Em todas as análises, foi usado o programa R (versão 3.6.3). O valor foi considerado estatisticamente significante para p <0,05.
ResultadosTradução/tradução reversaO processo de tradução e de tradução reversa ocorreu com a participação de duas pessoas em cada fase, respectivamente. Após essas fases terem sido executadas, foi feita uma reunião remota entre os membros e a coordenadora da pesquisa (total de 6 pessoas), que está registrada em vídeo. Após consenso entre todos os membros, a versão final (tabela 1) foi apresentada aos responsáveis das crianças avaliadas.
Versão final do questionário PSQ, traduzido para o português – Brasil
| PSQ – versão português Brasil | Sim | Não | Não sei |
|---|---|---|---|
| Durante o sono, seu filho: | |||
| A1. ronca mais que a metade do tempo | ( ) | ( ) | ( ) |
| A2. sempre ronca | ( ) | ( ) | ( ) |
| A3. ronca alto | ( ) | ( ) | ( ) |
| A4. tem a respiração profunda ou ruidosa | ( ) | ( ) | ( ) |
| A5. Tem dificuldade em respirar ou se esforça para respirar? | ( ) | ( ) | ( ) |
| A6. Você alguma vez já viu seu filho (ou filha) parar de respirar durante o sono? | ( ) | ( ) | ( ) |
| O seu filho (ou filha): | |||
| A7. tende a respirar com a boca aberta durante o dia | ( ) | ( ) | ( ) |
| A8. acorda com a boca seca | ( ) | ( ) | ( ) |
| A9. Faz xixi na cama de vez em quando | ( ) | ( ) | ( ) |
| O seu filho (ou filha): | |||
| B1. Acorda cansado de manhã? | ( ) | ( ) | ( ) |
| B2. Tem problema de sonolência durante o dia? | ( ) | ( ) | ( ) |
| B3. Algum(a) professor(a) ou outra pessoa já comentou que seu filho parece sonolento durante o dia? | ( ) | ( ) | ( ) |
| B4. É difícil acordar seu filho de manhã? | ( ) | ( ) | ( ) |
| B5. Seu filho acorda com dor de cabeça de manhã? | ( ) | ( ) | ( ) |
| B6. Seu filho parou de crescer normalmente em algum momento desde o nascimento? | ( ) | ( ) | ( ) |
| B7. Seu filho está acima do peso? | ( ) | ( ) | ( ) |
| Seu filho com frequência: | |||
| C1. Parece não ouvir quando falam diretamente com ele | ( ) | ( ) | ( ) |
| C2. Tem dificuldade de organizar tarefas e atividades | ( ) | ( ) | ( ) |
| C3. É facilmente distraído por estímulos alheios | ( ) | ( ) | ( ) |
| C4. Fica com as mãos ou pés inquietos ou fica agitado quando sentado | ( ) | ( ) | ( ) |
| C5. Não para quieto ou frequentemente age como se estivesse ligado na tomada | ( ) | ( ) | ( ) |
| C6. Interrompe as pessoas ou se intromete em conversas ou brincadeiras | ( ) | ( ) | ( ) |
A amostra consistiu em 60 crianças, inclusive 39 do sexo masculino (65%) e 21 do sexo feminino (35%), entre 2 e 17 anos (média de 7,9±4,0 anos). Desstas, 40 crianças tinham AOS confirmada por polissonografia e 20 não apresentavam queixas respiratórias espontâneas. Um dos pais/responsável dos participantes (na maioria a mãe) concordou em responder ao questionário e consentiu TCLE previamente à aplicação. Em trinta crianças com diagnóstico de AOS, o mesmo responsável fez o reteste do questionário, com intervalo médio de 15 dias entre as entrevistas.
Em todas as 60 aplicações do teste, o responsável não referiu dificuldade em responder a qualquer pergunta do questionário. Em todos os casos, o pai/responsável levou menos de 10 minutos para preencher o teste.
Consistência internaA análise de confiabilidade do estudo (ou de consistência interna) foi feito através de coeficiente Alfa de Cronbach. Foram feitas as análises para cada subdomínio e para o questionário no total. O questionário total (PSQ – Brasil) apresentou alta confiabilidade, com Alfa de Cronbach de 0,86 (95% IC: 0,82–0,91). Os valores estão apresentados na tabela 2.
Consistência interna do PSQ traduzido para o português – Brasil, avaliado através do Alfa de Cronbach
| Variáveis | Número de itens | Alfa de Cronbach (95% IC) |
|---|---|---|
| Subdomínio Ronco | 9 | 0,83 (0,76–0,89) |
| Subdomínio Sonolência | 7 | 0,64 (0,51–0,78) |
| Subdomínio Comportamento | 6 | 0,65 (0,51–0,79) |
| Total | 22 | 0,86 (0,82–0,91) |
Para os subdomínios, “ronco” teve alta confiabilidade, com Alfa de Cronbach de 0,83 (95% IC: 0,76–0,89). Já os subdomínios “sonolência” e “comportamento” tiveram confiabilidade moderada, com respectivamente valores de 0,64 (95% IC: 0,51–0,78) e 0,65 (95% IC: 0,51–0,79).
Teste‐retesteO teste‐reteste foi avaliado pelo teste de concordância de Kappa e foi feito em 30 crianças, cujos pais/responsáveis responderam o mesmo questionário 2 dias diferentes, com intervalo médio de 15 dias entre eles.
Os valores correspondentes a cada questão estão descritos na tabela 3. As questões A2, B7 e C6 tiveram concordância quase perfeita. Já as questões A5, A8, B5 e C2 tiveram concordância moderada; todas as outras questões tiveram concordância alta.
Avaliação de fidedignidade do teste‐reteste do questionário PSQ traduzido para o português – Brasil
| Questão | Kappa | 95% IC | p‐valor |
|---|---|---|---|
| A1 | 0,61 | 0,23–0,99 | 0,0004 |
| A2 | 0,92 | 0,77–1,00 | <0,0001 |
| A3 | 0,71 | 0,35–1,00 | 0,0001 |
| A4 | 0,61 | 0,20–1,00 | 0,0010 |
| A5 | 0,49 | 0,19–0,80 | 0,0043 |
| A6 | 0,65 | 0,38–0,93 | 0,0004 |
| A7 | 0,66 | 0,31–1,00 | 0,0003 |
| A8 | 0,44 | 0,03–0,85 | 0,0171 |
| A9 | 0,78 | 0,54–1,00 | <0,0001 |
| B1 | 0,69 | 0,41–0,97 | 0,0003 |
| B2 | 0,66 | 0,39–0,92 | 0,0003 |
| B3 | 0,63 | 0,30–0,95 | 0,0006 |
| B4 | 0,78 | 0,54–1,00 | <0,0001 |
| B5 | 0,56 | 0,26–0,87 | 0,0022 |
| B6 | 0,65 | 0,02–1,00 | 0,0002 |
| B7 | 0,93 | 0,79–1,00 | <0,0001 |
| C1 | 0,65 | 0,37–0,93 | 0,0005 |
| C2 | 0,59 | 0,28–0,90 | 0,0011 |
| C3 | 0,71 | 0,33–1,00 | 0,0001 |
| C4 | 0,62 | 0,29–0,96 | 0,0008 |
| C5 | 0,66 | 0,31–1,00 | 0,0003 |
| C6 | 0,85 | 0,65–1,00 | <0,0001 |
Os subdomínios tiveram fidedignidade alta, quase perfeita (tabela 4). De acordo com as análises, o subdomínio “ronco” teve valor de ICC (intraclass coefficiency) de 0,89 (95% IC: 0,77–0,95); para “sonolência”, o valor de ICC foi de 0,93 (95% IC: 0,85–0,97); e para “comportamento”, o valor de ICC foi de 0,86 (95% IC: 0,70–0,94).
Avaliação de fidedignidade do teste‐reteste dos subdomínios questionário PSQ traduzido para o Português – Brasil
| Questão | ICC | 95% IC | p‐valor |
|---|---|---|---|
| Subdomínio Ronco | 0,89 | 0,77–0,95 | <0,0001 |
| Subdomínio Sonolência | 0,93 | 0,85–0,97 | <0,0001 |
| Subdomínio Comportamento | 0,86 | 0,70–0,94 | <0,0001 |
ICC, Intraclass correlation coefficient.
Para validação de conteúdo foi usado o teste de correlação de Pearson para cada item do questionário, comparado ao escore total. Todos as questões apresentaram concordância moderada (> 0,3 e <0,8) e forte (≥ 0,8), exceto as questões B6 (acerca de interrupção de velocidade de crescimento somático) e A9 (acerca de enurese noturna), que não tiveram correlação significante. Nenhum dos itens apresentou forte correlação (tabela 5).
Coeficiente de correlação de Pearson (r) para cada questão, assim como 95% IC e p‐valor correspondente
| Questão | r‐Pearson | 95% IC | p‐valor |
|---|---|---|---|
| A1. | 0,75 | 0,62–0,85 | <0,0001 |
| A2. | 0,63 | 0,44–0,76 | <0,0001 |
| A3. | 0,57 | 0,37–0,72 | <0,0001 |
| A4. | 0,79 | 0,66–0,87 | <0,0001 |
| A5. | 0,71 | 0,56–0,82 | <0,0001 |
| A6. | 0,58 | 0,38–0,73 | <0,0001 |
| A7. | 0,44 | 0,21–0,63 | 0,0004 |
| A8. | 0,41 | 0,18–0,61 | 0,0011 |
| A9. | 0,25 | ‐0,01–0,47 | 0,0588a |
| B1. | 0,51 | 0,30–0,68 | <0,0001 |
| B2. | 0,54 | 0,33–0,70 | <0,0001 |
| B3. | 0,51 | 0,29–0,67 | <0,0001 |
| B4. | 0,34 | 0,10–0,55 | 0,0072 |
| B5. | 0,52 | 0,31–0,69 | <0,0001 |
| B6. | 0,12 | ‐0,13–0,37 | 0,3441a |
| B7. | 0,33 | 0,08–0,55 | 0,0102 |
| C1. | 0,52 | 0,31–0,69 | <0,0001 |
| C2. | 0,65 | 0,48–0,78 | <0,0001 |
| C3. | 0,57 | 0,37–0,72 | <0,0001 |
| C4. | 0,48 | 0,25–0,65 | 0,0001 |
| C5. | 0,42 | 0,19–0,61 | 0,0008 |
| C6. | 0,39 | 0,15–0,59 | 0,0020 |
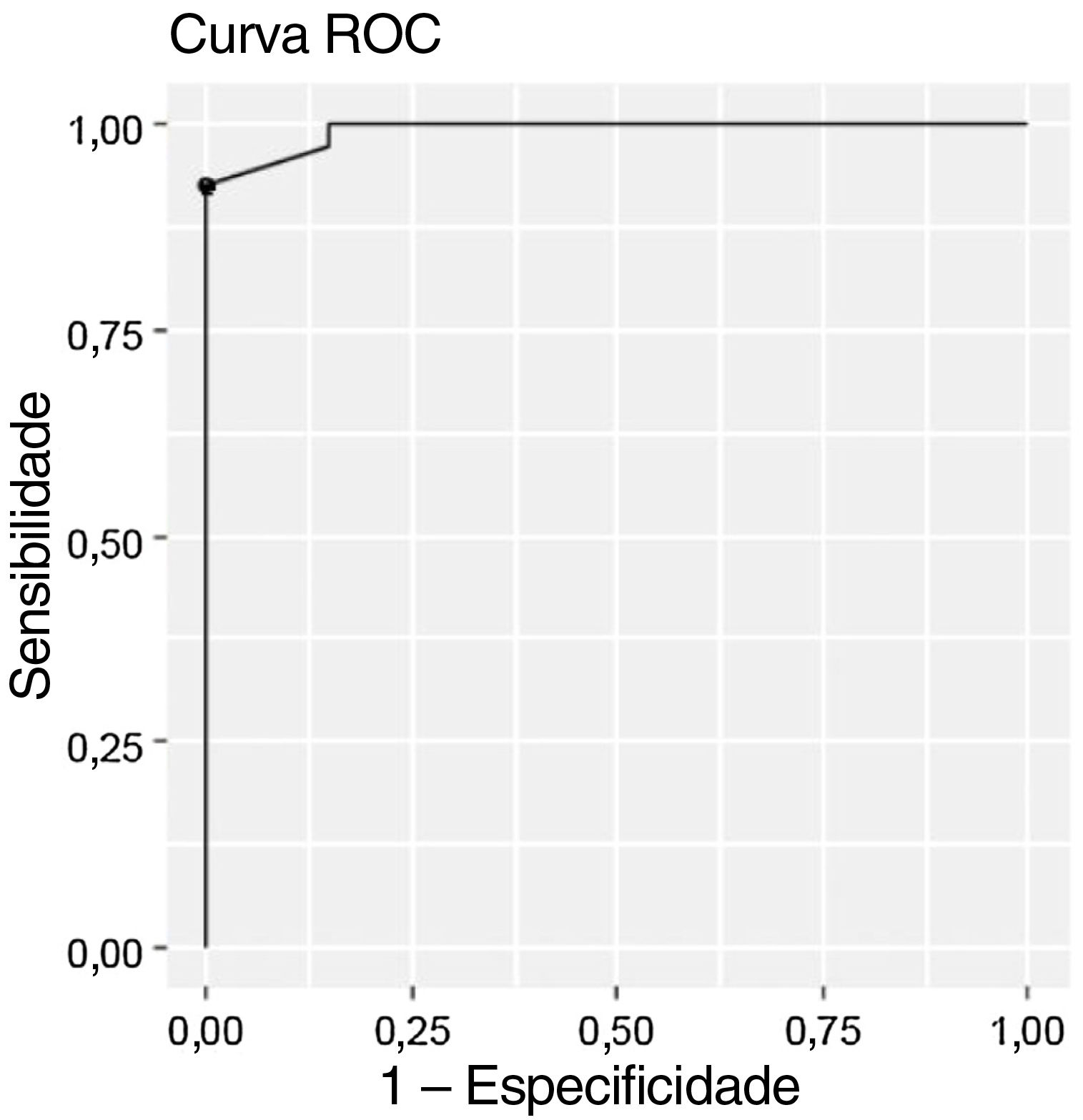
Por fim, fizemos o teste de curva ROC para observarmos a acurácia do questionário em diferenciar, na nossa coorte, as crianças com AOS e as crianças controles. O resultado do questionário foi de um AUC=0,99; ou seja, quase perfeita (fig. 1). A mesma análise também identificou o melhor valor para nota de corte, que foi considerado 9,0. Esse valor teve a sensibilidade de 0,92; especificidade de 1,0 e acurácia de 0,95, ou seja, crianças com questionário igual ou acima de 9,0 têm alta probabilidade de ter AOS, enquanto as que obtiverem valores abaixo de 9,0 possuem baixa probabilidade de apresentar distúrbio respiratório do sono.
Figura representa a acurácia do questionário PSQ traduzido para o português – Brasil, em diferenciar as crianças com AOS e controles. A curva ROC foi quase perfeita, com area under the curve (AUC=0,99), e identificou o ponto de corte ótimo como 9 pontos. Nesse ponto, a sensibilidade foi de 0,92, especificidade foi de 1,00 e acurácia foi de 0,95 para diferenciar um grupo do outro.
Os subdomínios também tiveram boa acurácia em diferenciar um grupo do outro: “ronco” teve AUC=0,94; “sonolência” teve AUC=0,85; e “comportamento” teve AUC=0,92.
DiscussãoO diagnóstico precoce, tratamento e seguimento adequados da AOS são fundamentais para evitar a morbidade associada a essa doença. No entanto, na prática clínica, esbarramos na dificuldade de feitura do exame padrão‐ouro para o diagnóstico, a polissonografia, por ser um exame caro, demorado e pouco acessível, principalmente para a população pediátrica.
Nesse contexto se fazem necessárias novas ferramentas para auxiliar no triagem da AOS na população infantil e os questionários diagnósticos emergem como alternativas simples, baratas e fáceis de serem aplicadas.
Entre os questionários existentes estão o sleep clinical record (SCR),22 que é bastante completo, porém complexo e demorado,13 o OSA‐18, que avalia o impacto dos sintomas obstrutivos na qualidade de vida, mas que como método diagnóstico apresenta baixa sensibilidade e especificidade,23 e o PSQ. O PSQ se destaca por apresentar alta sensibilidade e especificidade e por ser fácil e rápido de aplicar, não é necessária a presença de um médico ou profissional treinado.
Desde sua validação em 2000, o PSQ já foi traduzido para diversos idiomas, inclusive o português falado em Portugal.18 No entanto, a diferença linguística entre os dois países é que dificulta o entendimento de algumas questões, principalmente entre os indivíduos de menor índice socioeconômico. Um exemplo claro dessa diferença está presente no domínio A (ronco). Na versão de Portugal, a palavra “ressonar” está presente em 3 questões, enquanto no português falado no Brasil o verbo “roncar” seria a palavra equivalente de uso mais frequente. Essa dificuldade do uso autoaplicado deste questionário entre os pacientes no nosso serviço nos motivou à feitura desse estudo, que teve como objetivo a tradução e adaptação transcultural específicas para o português falado no Brasil.
Para a tradução do PSQ original validado por Chervin et al.,15 seguimos rigorosamente a metodologia proposta por Sagheri et al.19 Em seguida, foi aplicado aos pais ou responsáveis de 60 crianças entre 2 e 18 anos, entre as quais 40 eram portadoras de AOS confirmada em polissonografia e 20 eram assintomáticas. Nenhum dos pais/responsáveis referiu dificuldade em entender alguma questão, na versão apresentada por nós. Ainda, o PSQ – Brasil apresentou alta acurácia em diferenciar, entre as crianças testadas, as com AOS dos controles, como comprovado pelo teste de curva de ROC (AUC=0,99), com sensibilidade de 0,92 e especificidade de 1 quando usado o valor de corte de 9. Isso demonstra que crianças com valores de PSQ até 9 têm baixa probabilidade de apresentar AOS.
Destaca‐se também a elevada confiabilidade da versão brasileira do questionário, evidenciada pelo valor do alfa de Cronbach de 0,86, corroborou os achados da versão original e de outras versões como a francesa e a portuguesa.15,16,18
Em relação à estabilidade do teste, os subdomínios apresentaram fidedignidade quase perfeita, com valores de ICC de 0,89 para o subdomínio “ronco”; 0,93 para “sonolência”’; e 0,86 para “comportamento”.
O estudo tem algumas limitações, com o uso de crianças acompanhadas em um centro especializado de nível terciário e, portanto, podem apresentar formas mais graves e exuberantes da doença. Ainda, todas as crianças incluídas no estudo são usuárias do sistema único de saúde (SUS), podem não representar de forma adequada todas nichos socioeconômicos da população brasileira. Por fim, o Brasil é um país continental com diferenças linguísticas entre cada região e o resultado observado no nosso centro pode não ser o mesmo em outras regiões brasileiras.
Ainda assim, o estudo de tradução e a adaptação transcultural do PSQ para o Brasil mostraram valores semelhantes aos observados em outras traduções no mundo, assim como a versão original americana, e, portanto, pode ser usado como um teste de triagem confiável em crianças brasileiras com suspeita de AOS.
ConclusãoA tradução e adaptação transcultural do PSQ para o português do Brasil mostrou‐se bem‐sucedida com evidência de forte correlação com os resultados obtidos na versão original em inglês. Em locais com dificuldade de acesso à polissonografia, o PSQ pode ser uma ferramenta útil na suspeição diagnóstica e seguimento das crianças com AOS.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
Aos pesquisadores da Universidade de Michigan, que detém a nota de direito de cópia do PSQ original, em inglês, por terem nos permitido a tradução para o Português – versão brasileira.
Como citar este artigo: Martins CA, Deus MM, Abile IC, Garcia DM, Anselmo‐Lima WT, Miura CS, et al. Translation and cross‐cultural adaptation of the pediatric sleep questionnaire (PSQ*) into Brazilian Portuguese. Braz J Otorhinolaryngol. 2022;88:S63–S69.
A revisão por pares é da responsabilidade da Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico‐Facial.